Clear Sky Science · pl
Mechanizmy regulujące stabilność białka Snail: system ubikwityna–proteasom i autophagia zależna od chaperonów
Dlaczego rozprzestrzenianie się raka zależy od kruchego białka
Rak staje się naprawdę zagrażający życiu, gdy komórki odrywają się od pierwotnego guza i podróżują do odległych narządów. To rozprzestrzenianie się, czyli przerzutowanie, zależy częściowo od potężnego „głównego przełącznika” białkowego o nazwie Snail, które pomaga komórkom poluzować więzi i stać się bardziej ruchomymi. Ten artykuł wyjaśnia, jak komórki zwykle trzymają Snail na krótko, szybko go rozkładając za pomocą dwóch głównych systemów utylizacji. Zrozumienie tej równowagi daje nowe pomysły na spowolnienie lub zapobieganie przerzutom.
Z ciasno upakowanych komórek do wędrujących najeźdźców
W zdrowych tkankach komórki nabłonkowe tworzą uporządkowane, cegłopodobne warstwy, które trzymają się na miejscu i ściśle przylegają do sąsiadów. Aby komórka nowotworowa mogła uciec, często przechodzi przemianę zwaną przejściem nabłonkowo-mezenchymalnym (EMT), w trakcie której traci ciasne kontakty i zyskuje zdolność do ruchu i inwazji. Snail jest kluczowym sterownikiem tej przemiany: gdy znajduje się w jądrze komórkowym, wyłącza geny utrzymujące adhezję międzykomórkową i włącza geny sprzyjające ruchowi oraz inwazji. Wysokie poziomy Snail wiążą się z agresywnymi nowotworami i złym rokowaniem pacjentów, dlatego komórki wykształciły mechanizmy utrzymujące Snail w niskim i krótkotrwałym stanie w warunkach prawidłowych.
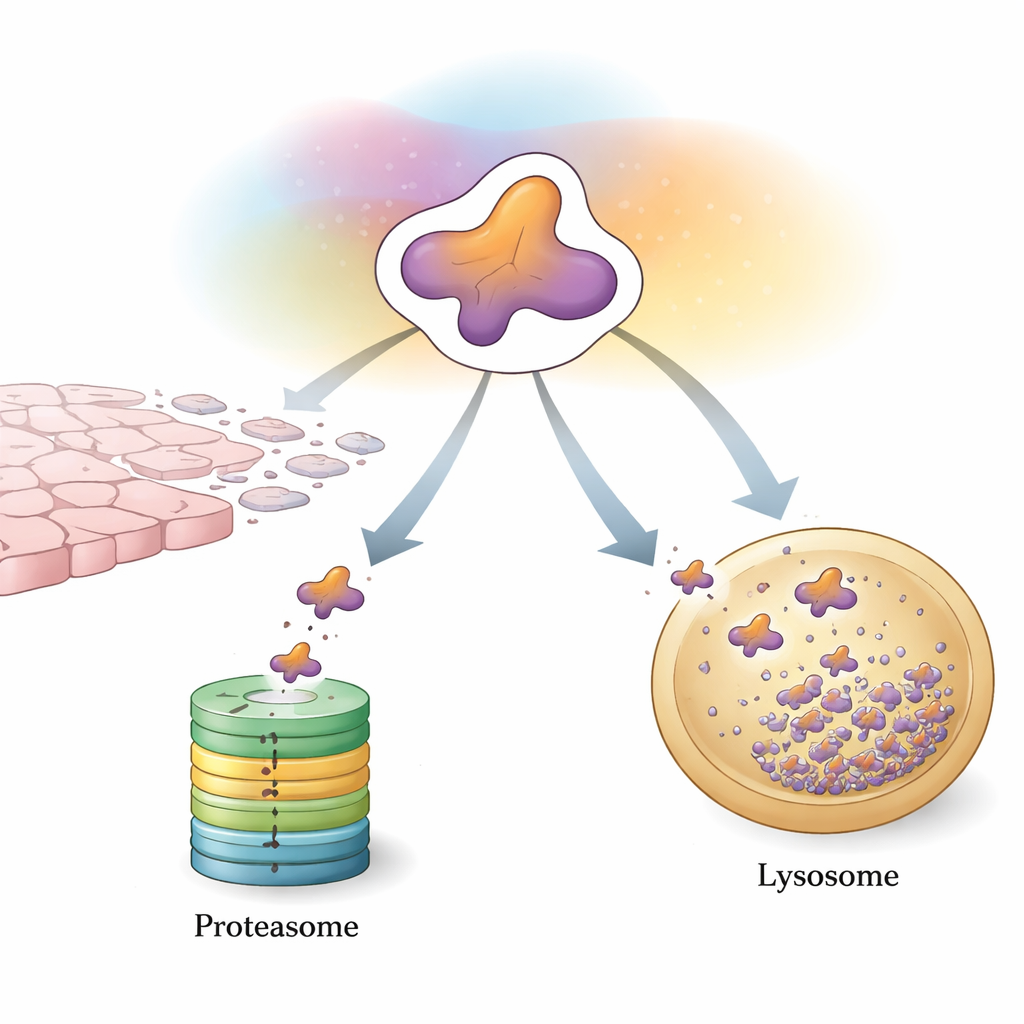
Pierwsza linia kontroli komórkowej: znaczek i rozdrabnianie
Głównym sposobem kontroli Snail jest system ubikwityna–proteasom, maszyna oznaczająca i rozdrabniająca niechciane białka. Specjalistyczne enzymy przyłączają do Snail małe „flagi” z białka zwanego ubikwityną. Gdy tych flag zbierze się odpowiednia ilość i układ, Snail zostaje skierowany do proteasomu — cylindrycznego kompleksu, który rozcina je na fragmenty. Szeroki zestaw białek wspomagających precyzuje ten proces. Niektóre enzymy dokładają łańcuchy promujące degradację, szybko wysyłając Snail do niszczarki, co pomaga ograniczać wzrost i rozprzestrzenianie się guza. Inne dodają łańcuchy, które zamiast tego stabilizują Snail lub pośrednio zwiększają jego produkcję, przechylając równowagę w stronę EMT i przerzutów. Modyfikacje chemiczne, takie jak fosforylacja i acetylacja, działają jak dodatkowe przełączniki, kontrolując, które białka pomocnicze mogą wiązać się ze Snail i czy zostanie on zniszczony, czy oszczędzony.
Usuwanie hamulców: enzymy ratujące Snail
Historia nie kończy się na oznaczaniu Snail do zniszczenia. Inna grupa enzymów, zwana deubikwitynazami, może usuwać flagi ubikwitynowe, ratując Snail przed proteasomem. Wiele z tych enzymów jest włączonych lub wzmocnionych w nowotworach, co pozwala Snail uniknąć rozpadu i utrzymywać się w jądrze. Ich działanie silnie zależy od kontekstu komórkowego: w niektórych warunkach bezpośrednio stabilizują Snail, w innych wpływają na jego lokalizację w komórce lub na interakcje z partnerami. Sygnały ze szlaków związanych z nowotworem, takich jak czynniki wzrostu i reakcje na stres, wchodzą w tę sieć, decydując, czy Snail zostanie szybko usunięty, czy też pozwolono mu napędzać program EMT.
Druga siatka bezpieczeństwa: selektywne dostarczanie do centrum recyklingu komórki
Poz poza proteasomem komórki polegają na autofagii — zbiorze szlaków transportujących białka do kwaśnych przedziałów zwanych lizosomami w celu rozkładu. Przegląd ten podkreśla wysoce selektywną formę zwaną autofagią zależną od chaperonów (CMA) jako drugą główną drogę kontroli Snail. CMA rozpoznaje krótki fragment sekwencji w Snail i, z pomocą białek eskortujących, dostarcza cytoplazmatyczne Snail do lizosomów do degradacji. W mniej agresywnych komórkach raka piersi ten system utrzymuje Snail głównie poza jądrem i podatne na usuwanie lizosomalne. W bardziej agresywnych rakach piersi trójujemnych Snail ma tendencję do akumulacji w jądrze i omijania CMA, wzmacniając swoją zdolność do wywoływania EMT i przerzutów.
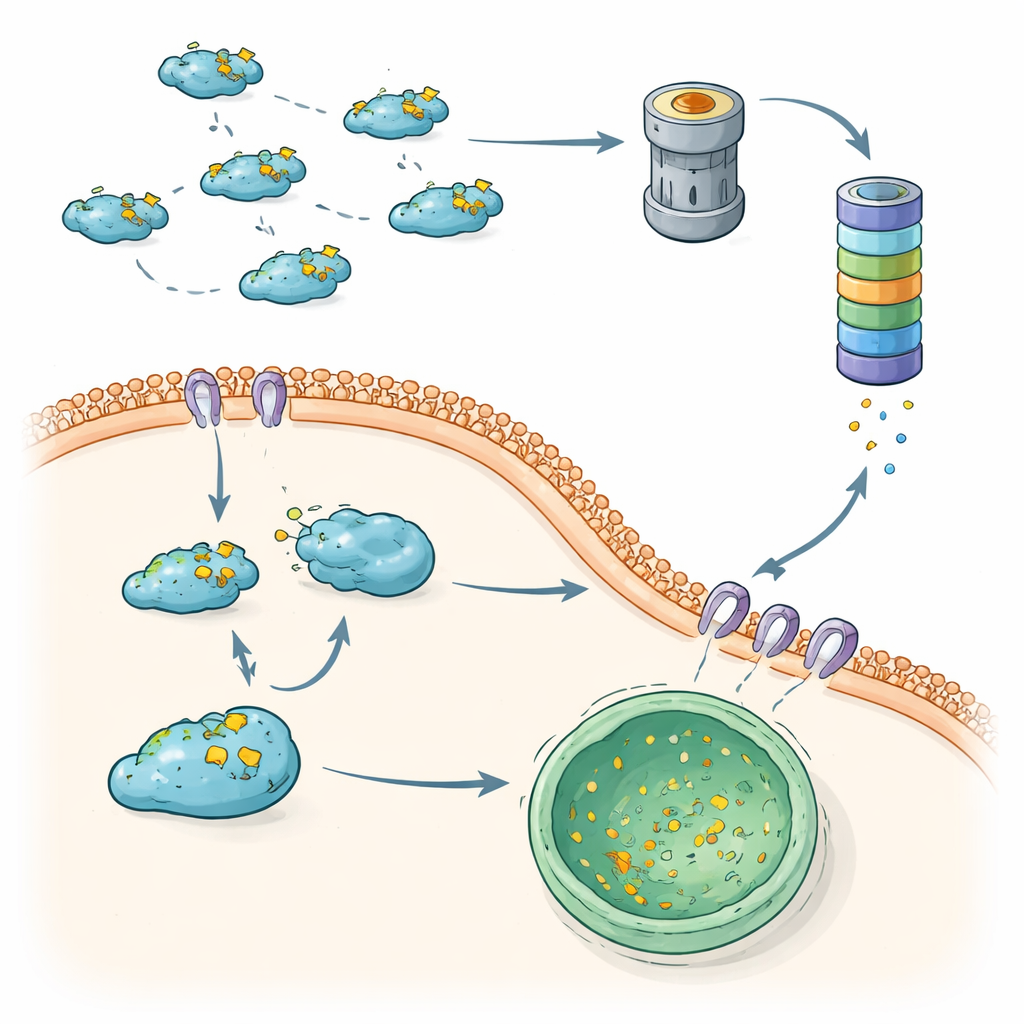
Gdy kontrola jakości zawodzi, przerzuty zyskują przewagę
Razem te ustalenia pokazują, że komórki korzystają z dwóch uzupełniających się osi „kontroli jakości”, aby ograniczyć Snail: szlaku ubikwityna–proteasom oraz degradacji lizosomalnej opartej na CMA. Gdy obie działają prawidłowo, Snail jest szybko wymieniany, co ogranicza EMT i pomaga zapobiegać rozprzestrzenianiu się komórek nowotworowych. Gdy któraś z osi jest osłabiona — przez zmiany w enzymach znakujących, deubikwitynazach lub składnikach CMA — Snail staje się bardziej stabilny, kumuluje się w jądrze i silnie promuje zachowania inwazyjne. Mapując te powiązane trasy rozkładu, artykuł wytycza nowe możliwości terapeutyczne: leki, które przywracają lub wzmacniają degradację Snail, lub które kierują Snail z powrotem w stronę CMA albo degradacji proteasomalnej, mogłyby pomóc ponownie zaciągnąć hamulec na przerzuty, nie wyłączając przy tym całkowicie tych niezbędnych systemów recyklingu białek.
Cytowanie: Kim, M., Hong, KS., Kim, T. et al. Regulatory mechanisms for Snail protein stability: ubiquitin–proteasome system and chaperone-mediated autophagy. Exp Mol Med 58, 408–415 (2026). https://doi.org/10.1038/s12276-026-01667-6
Słowa kluczowe: przerzuty nowotworowe, przejście nabłonkowo-mezenchymalne, białko Snail, degradacja białek, autofagia