Clear Sky Science · pl
Kornea–trigeminalny obwód neurozapalny zależny od receptora TRPV1 promuje neuropatię rogówki
Wrażliwe oczy i utrzymujący się ból
Wiele osób z suchymi, podrażnionymi oczami zaskakuje fakt, że ich najgorsze objawy nie wynikają z powierzchni oka, lecz z nerwów, które wykrywają podrażnienie i ból. Badanie na myszach ujawnia ukryte sprzężenie zwrotne między okiem a ośrodkiem czuciowym mózgu, które pomaga wyjaśnić, dlaczego ból oka może się utrwalać i dlaczego czasem obejmuje oba oczy, nawet gdy tylko jedno wydaje się suche. Identyfikując konkretny molekularny „strażnik” w tym obwodzie, praca wskazuje nowe możliwości łagodzenia bólu oczu bez jedynie zwiększania ilości łez.

Kiedy system alarmowy oka zawodzi
Przezroczysta przednia część oka, rogówka, jest gęsto unerwiona i nieustannie monitoruje wilgotność, temperaturę oraz skład chemiczny łez. W chorobie suchego oka łzy są zmniejszone lub zbyt zasolone, a pacjenci często odczuwają pieczenie, kłucie lub nawet wyniszczający ból. Autorzy skupili się na molekularnym sensorze włókien bólowych rogówki zwanym TRPV1, najlepiej znanym jako receptor dla kapsaicyny — związku występującego w papryczkach chili. Ten sensor reaguje na ciepło i sygnały uwalniane podczas uszkodzeń tkanek. Zespół badał, czy nadmierna aktywacja TRPV1 wskutek suchości i uszkodzeń może napędzać nie tylko miejscowe podrażnienie, lecz także głębsze zmiany w nerwach łączących oko z mózgiem.
Obwód nerwowo‑odpornościowy łączący oko z mózgiem
W modelach mysich, w których produkcja łez została chirurgicznie zmniejszona, badacze wykazali, że suche oko silnie aktywuje włókna nerwowe rogówki z ekspresją TRPV1. To z kolei zmienia aktywność genów i zachowanie układu odpornościowego w zwoju trójdzielnym, skupisku nerwowym zawierającym ciała komórek czuciowych rogówki. U normalnych myszy suchość prowadziła do wzrostu ekspresji genów związanych z zapaleniem i odpornością oraz do zmiany stanu pobliskich makrofagów — komórek odpornościowych otaczających neurony czuciowe. Jednocześnie same suche oczy wykazywały aktywowane komórki odpornościowe na powierzchni, zmniejszoną gęstość nerwów i nietypową wrażliwość: rogówka stała się mniej reagująca na dotyk mechaniczny i na niektóre chemiczne bodźce, a jednocześnie bardziej reaktywna na stymulację TRPV1, co sugeruje uwarunkowane uczulenie tego sensora.
Jak jedno chore oko wpływa na drugie
Aby odróżnić bezpośrednie skutki suchości od dalszych sygnałów pochodzących z nerwów, zespół wywołał „jednostronne” suche oko, usuwając gruczoł łzowy tylko po prawej stronie. Co ciekawe, nieleczone lewe oko pozostało normalnie wilgotne i utrzymywało zdrową barierę powierzchni, jednak z czasem rozwijało subtelne zapalenie i wyraźne oznaki dysfunkcji nerwów — przewężenie głębszych włókien nerwowych i zmienioną wrażliwość — odzwierciedlając, choć z opóźnieniem, zmiany po stronie uszkodzonej. Te przeciwnoległe zmiany zależały od TRPV1: myszy genetycznie pozbawione tego sensora były chronione zarówno w suchym, jak i w nieuszkodzonym oku. Sekwencjonowanie RNA z zwojów trójdzielnych potwierdziło, że jednostronna suchość wywołuje także po przeciwnej stronie sygnaturę zapalną i immunologiczną, wskazując na obwód rogówka–trigeminal–rogówka, który może przenosić problem z jednego oka na drugie.
Udowadnianie, że TRPV1 wystarcza do wywołania uszkodzeń
Suchość jest złożona i aktywuje wiele szlaków, dlatego autorzy zapytali, czy sam TRPV1 może uruchomić ten obwód. Nakładali kapsaicynę miejscowo na rogówkę jednego oka, stymulując TRPV1 bez wysuszania powierzchni. Leczone oko wykazywało wyraźną degenerację nerwów rogówki i zmniejszoną wrażliwość, mimo że bariera nabłonkowa pozostała nienaruszona. Co niezwykłe, nieleczone oko ponownie rozwijało łagodniejszą, ale mierzalną utratę zakończeń nerwowych i zmiany w wrażliwości, potwierdzając, że silna aktywacja TRPV1 w jednej rogówce wystarcza do wywołania uszkodzenia nerwów i zmian funkcjonalnych w oku przeciwległym przez wspólną sieć trójdzielną. Myszy pozbawione limfocytów T i B wykazały zmiany tylko w oku leczonym, co sugeruje, że pełne obustronne rozprzestrzenianie wymaga odpowiedzi adaptacyjnej układu odpornościowego oprócz aktywacji nerwów.
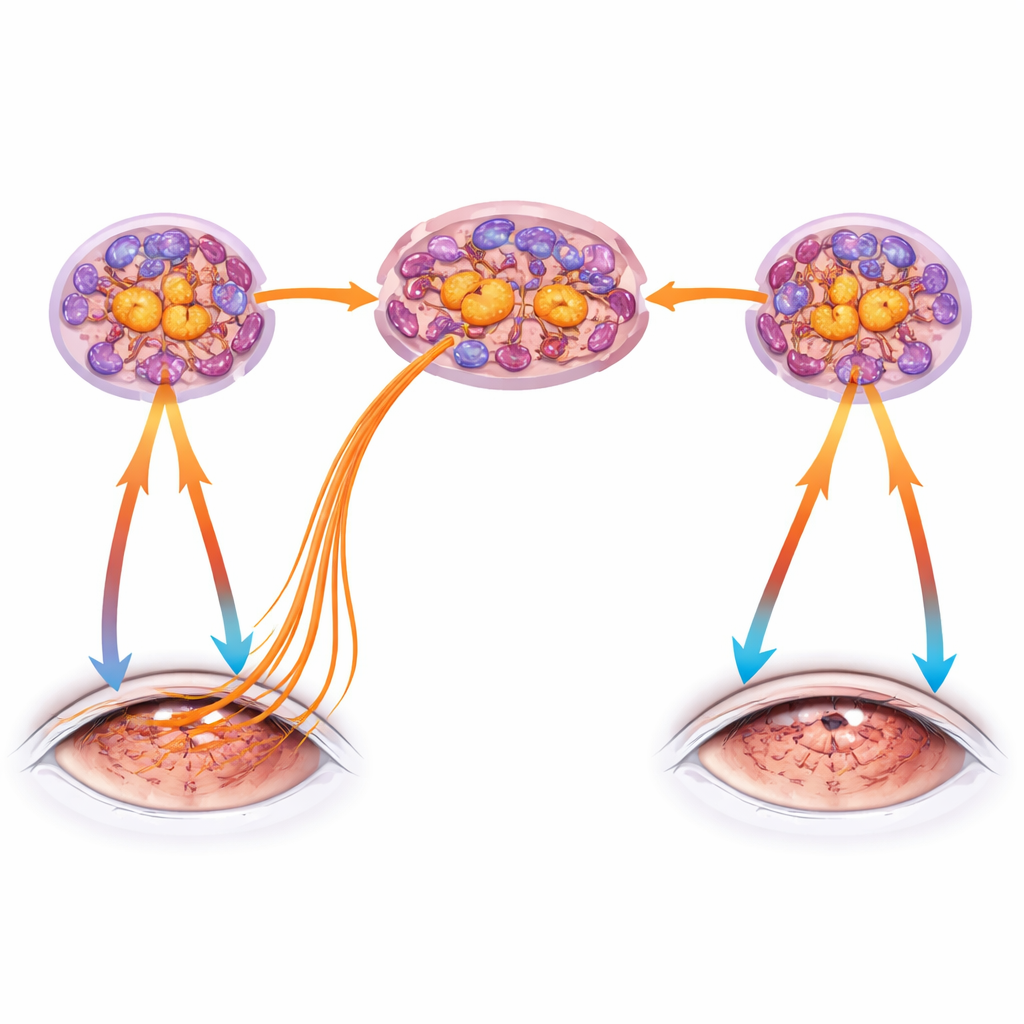
Przekaźnik nasilający ból i możliwy kierunek terapii
Badanie objęło też substancję P — neuropeptyd uwalniany z pobudzonych włókien bólowych, który może dodatkowo zapalać tkanki i wzmacniać aktywność TRPV1. Blokowanie receptorów substancji P kroplami do oka w nie‑suchym oku myszy z jednostronną suchością nie uszkodziło powierzchni rogówki, lecz istotnie zmniejszyło utratę wrażliwości dotykowej i wzmocnioną odpowiedź na stymulację TRPV1. Nie zapobiegło jednak całkowicie strukturalnej utracie zakończeń nerwowych, podkreślając, że kilka czynników współdziała w uszkadzaniu nerwów rogówki. Razem wyniki opisują błędne koło: suchość i uraz aktywują TRPV1 w nerwach rogówki, które wysyłają sygnały zagrożenia do zwoju trójdzielnego, rekrutują i przeprogramowują tam komórki odpornościowe, a następnie napędzają powrotną prozapalną aktywację nerwów i uwalnianie neuropeptydów na powierzchnię oka, pogarszając degenerację nerwów i rozprzestrzeniając dysfunkcję między oczami.
Co to oznacza dla osób z suchymi, bolesnymi oczami
Dla osób niemających specjalistycznej wiedzy kluczowe przesłanie jest takie: choroba suchego oka to nie tylko lokalny problem brakujących łez. Obejmuje samowzmacniający się obwód nerwowo‑odpornościowy łączący powierzchnię oka z ośrodkami czuciowymi w głowie i z powrotem. TRPV1 znajduje się w wejściowym punkcie tego obwodu i działa jak nadwrażliwy alarm, który po uruchomieniu pomaga podtrzymywać zapalenie i uszkodzenie nerwów, nawet jeśli pierwotna suchość jest niewielka lub jednostronna. Terapie zmniejszające aktywność TRPV1 w nerwach rogówki albo przerywające dalsze przekazywanie, np. poprzez blokadę substancji P, mogą więc robić więcej niż jedynie łagodzić suchą powierzchnię — mogą przerwać głębszy obwód bólu i chronić drobną sieć nerwową, która utrzymuje komfort i czucie oczu.
Cytowanie: Pizzano, M., Vereertbrugghen, A., Martinez Gomez, M.J. et al. A transient receptor potential vanilloid 1-dependent corneal–trigeminal neuroinflammatory circuit promotes corneal neuropathy. Exp Mol Med 58, 605–621 (2026). https://doi.org/10.1038/s12276-026-01653-y
Słowa kluczowe: choroba suchego oka, nerwy rogówki, TRPV1, neurozapalenie, substancja P