Clear Sky Science · pl
Metaboliczne rozmowy między fibroblastami związanymi z nowotworem, adipocytami i komórkami układu odpornościowego jako czynnik immunosupresyjnego mikrośrodowiska guza
Dlaczego sąsiedztwo guza ma znaczenie
Nowotwór nie rośnie w izolacji. Żyje w zatłoczonym sąsiedztwie komórek podporowych, komórek tłuszczowych i komórek układu odpornościowego, które nieustannie wymieniają między sobą składniki odżywcze i sygnały chemiczne. Ten artykuł wyjaśnia, jak „metabolizm” tego sąsiedztwa — sposób, w jaki komórki wykorzystują i dzielą się paliwem — subtelnie przechyla równowagę na korzyść guza, a przeciwko układowi odpornościowemu. Zrozumienie tej ukrytej ekonomii cukrów, tłuszczów i aminokwasów otwiera nowe możliwości poprawy terapii immunologicznych i odcięcia systemu wsparcia guza.
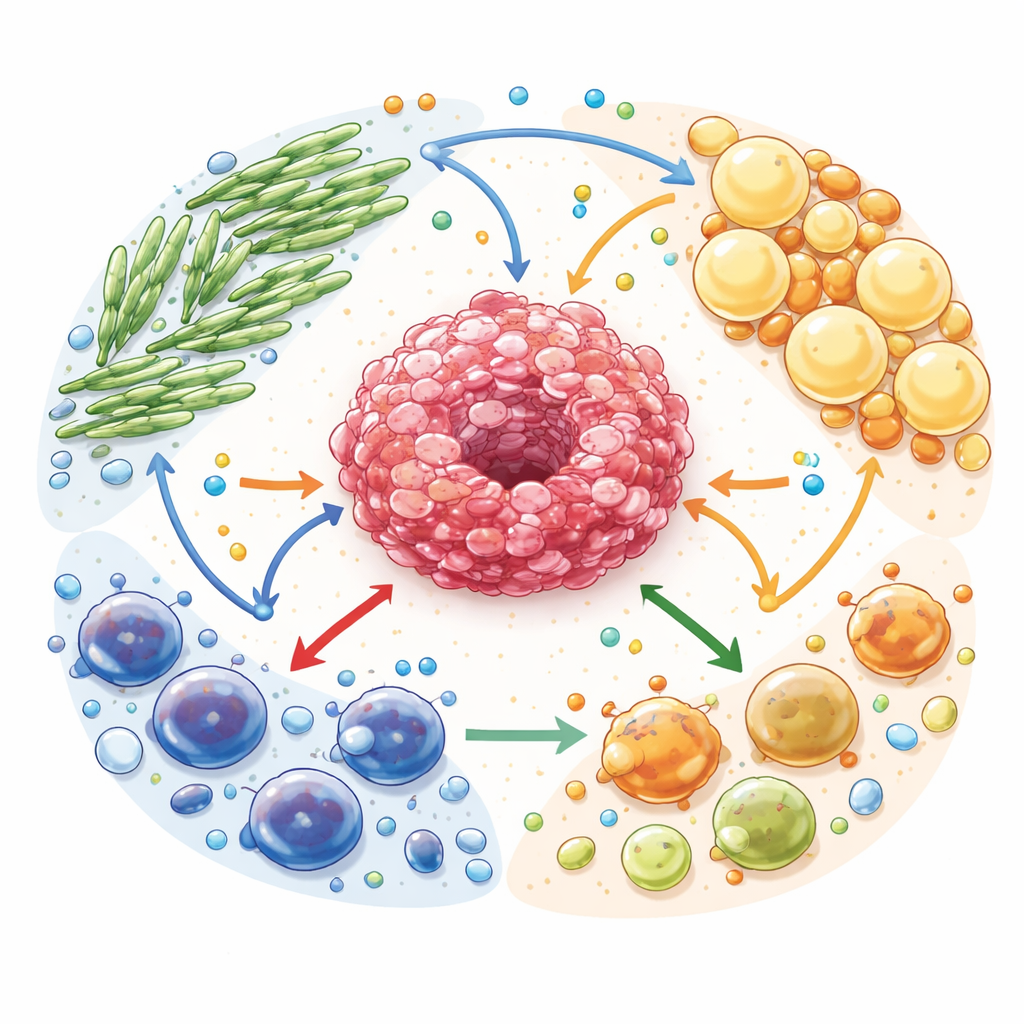
Współdzielenie paliwa w ekosystemie nowotworu
Autorzy opisują mikrośrodowisko guza jako złożony ekosystem. Komórki nowotworowe są otoczone przez fibroblasty związane z nowotworem (komórki podporowe przypominające bliznę), adipocyty związane z nowotworem (przebudowane komórki tłuszczowe) oraz liczne typy komórek odpornościowych. Wszystkie te komórki konkurują o paliwa i wymieniają się nimi — glukozą, kwasami tłuszczowymi i aminokwasami. Ta wymiana nie jest jednak neutralna: komórki podporowe zostają przestrojone tak, by rozkładać własne zapasy i eksportować wysokoenergetyczne cząsteczki, które zasilają komórki nowotworowe. Jednocześnie gromadzą się produkty odpadowe, w tym mleczan i adenozyna, które działają jako silne sygnały osłabiające komórki odpornościowe ochronne, a sprzyjające tym, które tłumią odpowiedź immunologiczną.
Jak komórki tłuszczowe wspierają guzy i utrudniają obronę
Otaczające skupiska tkanki tłuszczowej robią znacznie więcej niż tylko magazynują kalorie. Pod wpływem sygnałów z guza i niskiego poziomu tlenu zwykłe komórki tłuszczowe przekształcają się w adipocyty związane z nowotworem. Kurczą krople tłuszczowe, nasilają rozkład lipidów i uwalniają wolne kwasy tłuszczowe, cząsteczki zapalne oraz maleńkie pęcherzyki wypełnione ładunkiem. Komórki nowotworowe zachłannie pobierają te tłuszcze i spalają je w mitochondriach, zyskując elastyczne, długotrwałe źródło energii, które pomaga im przetrwać stres, szerzyć się i opierać leczeniu. Komórki odpornościowe w obszarach bogatych w tłuszcz radzą sobie gorzej: limfocyty T cytotoksyczne i komórki NK przeciążają się lipidami, doświadczają stresu oksydacyjnego i przechodzą w stan „wyczerpania” z osłabioną zdolnością niszczenia komórek nowotworowych. W przeciwieństwie do nich, komórki T regulatorowe i niektóre komórki mieloidalne dobrze wykorzystują te lipidy, stając się bardziej supresyjne i dodatkowo tłumiąc odpowiedzi immunologiczne.
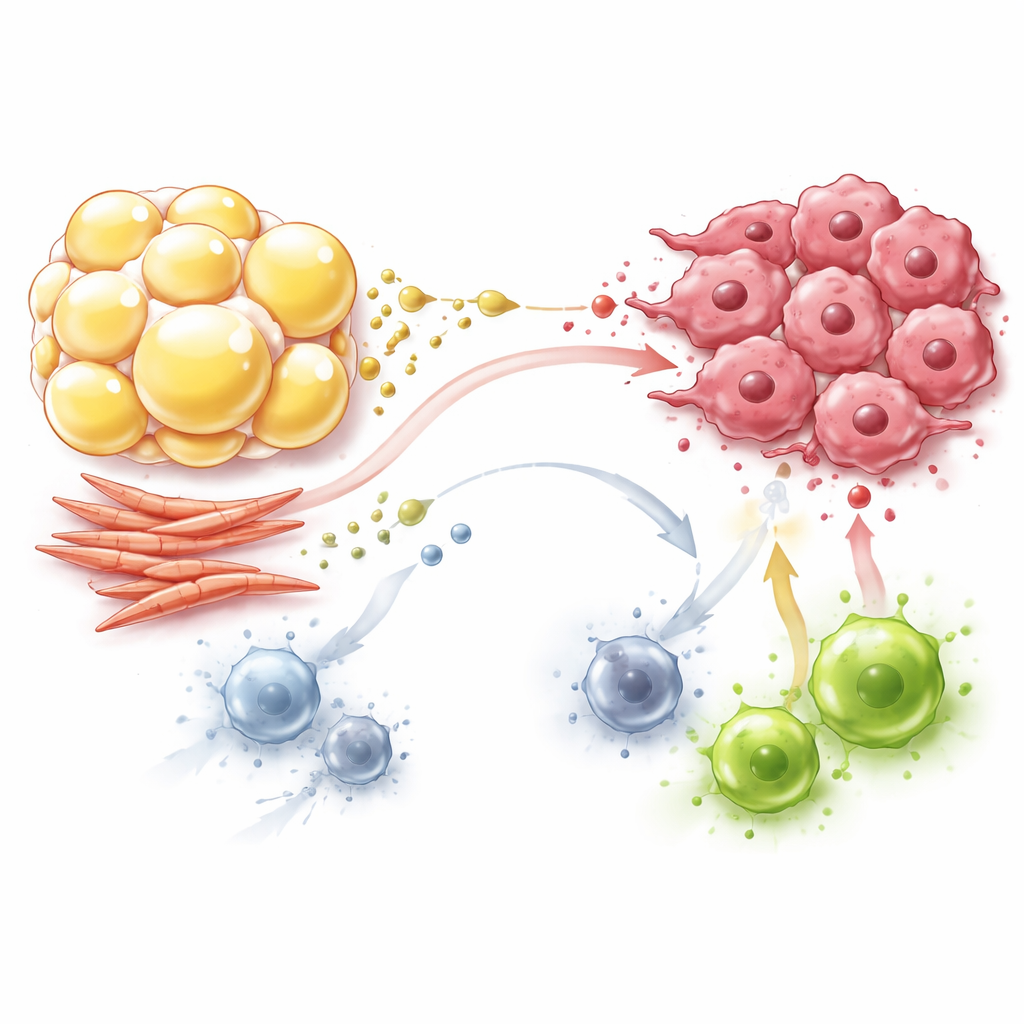
Fibroblasty: budowniczowie, którzy też przestroją metabolizm
Fibroblasty, od dawna znane jako „budowniczowie” tkanki przypominającej bliznę wokół guzów, są również aktywnymi uczestnikami tej metabolicznej dramaturgii. Fibroblasty związane z nowotworem przesuwają się w stronę zachowań łaknących cukru, przekształcając duże ilości glukozy w mleczan i pirogronian, nawet gdy tlen jest dostępny. Eksportują te produkty do otoczenia, gdzie komórki nowotworowe wykorzystują je ponownie jako paliwo dla własnych „elektrowni”, oszczędzając glukozę na wzrost. Fibroblasty także wytwarzają i wymieniają aminokwasy, takie jak glutamina, prolina i asparaginian, które wspierają zarówno strukturę guza, jak i jego wzrost w warunkach niedoboru składników. Jednocześnie fibroblasty pochłaniają kluczowe składniki odżywcze i uwalniają mleczan, wypierając komórki efektorowe T zależne od glukozy i przesuwając makrofagi oraz limfocyty T w kierunku bardziej tolerancyjnych, mniej agresywnych stanów.
Komórki odpornościowe uwięzione w metabolicznej pułapce
Układ odpornościowy wewnątrz guzów jest kształtowany równie mocno przez dostępność paliwa, co przez antygeny. Limfocyty T cytotoksyczne i komórki NK, które potrzebują szybkiego spalania cukru, by zasilić swój atak, znajdują się w krajobrazie pozbawionym glukozy i zalanym mleczanem, lipidami oraz innymi supresyjnymi metabolitami. Ich „silniki” przestają działać, mitochondria ulegają uszkodzeniu, a inhibitory „hamulce” na ich powierzchni się nasilają. Tymczasem komórki T regulatorowe i makrofagi związane z guzem są dobrze przystosowane do tego surowego środowiska. Preferują spalanie tłuszczów i metabolizm tlenowy, co pozwala im prosperować tam, gdzie inne komórki zawodzą. Wspierane przez fibroblasty i adipocyty, te komórki wzmacniają tolerancyjny stan podobny do procesu gojenia ran, który chroni guz i osłabia działanie inhibitorów punktów kontrolnych oraz innych immunoterapii.
Przekształcanie metabolizmu w cel terapii
Przegląd podkreśla rosnącą gamę eksperymentalnych leków zaprojektowanych, by zakłócić tę sieć wsparcia bez prostego trucia dzielących się komórek. Niektóre podejścia mają na celu zablokowanie uwalniania tłuszczu z adipocytów lub jego pobierania i spalania w komórkach nowotworowych. Inne celują w szlaki napędzane przez fibroblasty, które generują mleczan, przebudowują macierz lub przyciągają supresyjne komórki mieloidalne. Poprzez obniżenie poziomu mleczanu, blokowanie specyficznych transporterów paliwowych lub przeprogramowanie przełączników wrażliwych na lipidy wewnątrz komórek, te strategie dążą do przywrócenia dostępu do glukozy i zdrowia mitochondriów w wyczerpanych limfocytach T i komórkach NK. Ostatecznym celem jest nie tylko głodzenie guza, ale „przeedukowanie” jego sąsiedztwa, tak aby komórki odpornościowe ponownie rozpoznawały, docierały do i skutecznie atakowały komórki nowotworowe.
Cytowanie: Kim, T.H., Lim, S.H., Lee, H. et al. Metabolic crosstalk among cancer-associated fibroblasts, adipocytes and immune cells as an immunosuppressive tumor microenvironment driver. Exp Mol Med 58, 366–381 (2026). https://doi.org/10.1038/s12276-026-01650-1
Słowa kluczowe: mikrośrodowisko guza, metabolizm nowotworu, fibroblasty związane z nowotworem, adipocyty związane z nowotworem, immunosupresja guza