Clear Sky Science · pl
Niedobór składnika kompleksu egzocystowego Exoc5 nasila postęp włóknienia nerek
Dlaczego bliznowacenie nerek ma znaczenie
Przewlekła choroba nerek dotyka setek milionów ludzi na całym świecie, a głównym powodem jej postępu jest włóknienie — tkanka bliznowata, która stopniowo zastępuje funkcjonującą tkankę nerkową. W tym badaniu badacze przyglądają się mniej znanemu „mechanizmowi” komórkowemu, egzocystowi, oraz jednemu z jego elementów, Exoc5, aby odpowiedzieć na praktyczne pytanie: czy ten białkowy element pomaga nerkom regenerować się prawidłowo po urazie, czy raczej skłania je ku bliznowaceniu i niewydolności?
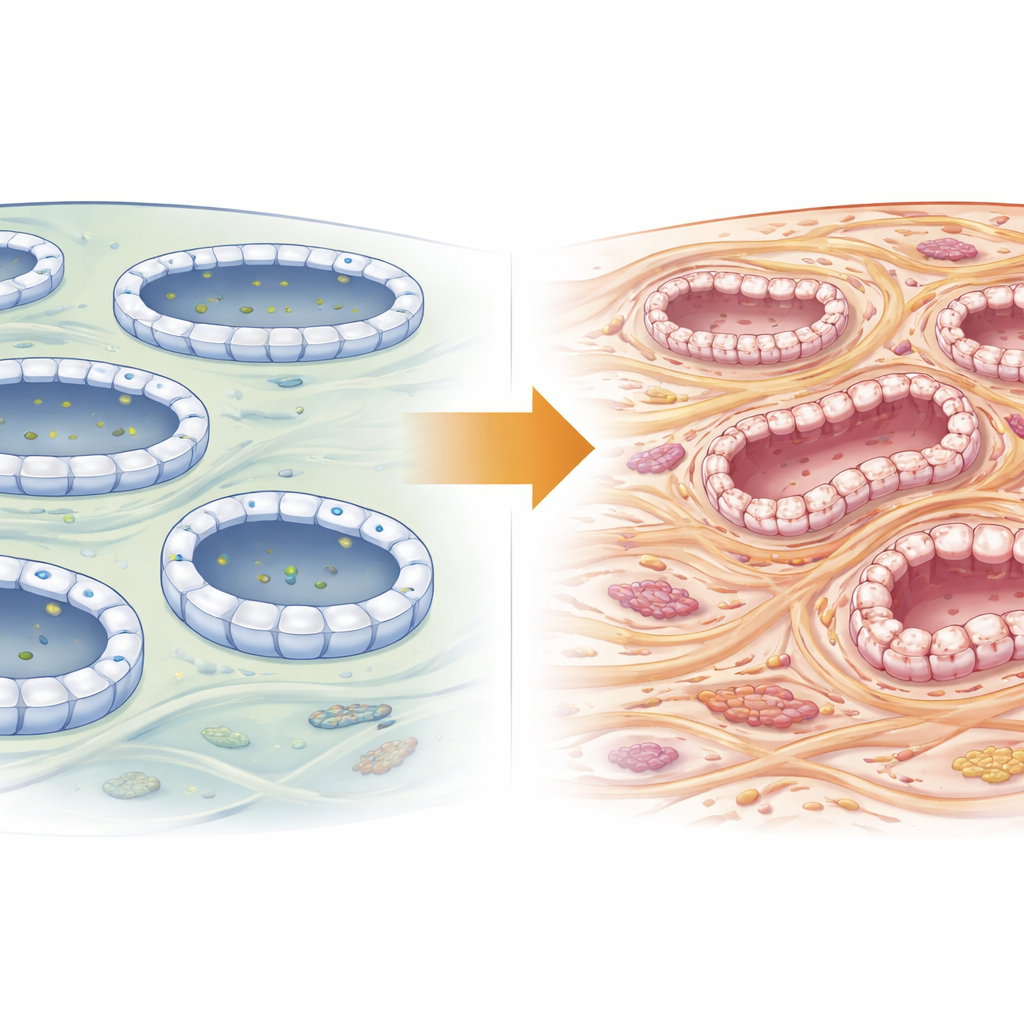
Centrum logistyczne w komórkach kanalików nerkowych
Każda komórka kanalika nerkowego jest zatłoczonym centrum logistycznym, nieustannie przemieszczającym maleńkie pęcherzyki z ładunkiem do precyzyjnych miejsc na swojej powierzchni. Ten ruch organizuje egzocyst — zespół dokujący złożony z ośmiu części. Exoc5 znajduje się w centrum tego mechanizmu, łącząc ładunek napływający z wnętrza komórki z miejscem dokowania na błonie zewnętrznej. Wcześniejsze badania wykazały, że zaburzenie Exoc5 szkodzi różnym narządom i że pomaga komórkom kanalików nerkowych utrzymać ich zwarte, uporządkowane struktury. Ponieważ zaburzona struktura jest cechą charakterystyczną włóknienia, autorzy przypuszczali, że Exoc5 może potajemnie decydować, czy uszkodzone nerki się regenerują, czy bliznują.
Badanie roli Exoc5 w nerkach myszy
Naukowcy stworzyli myszy, u których Exoc5 został usunięty jedynie w komórkach kanalików bliższych — odcinkach odpowiedzialnych w dużej mierze za filtrację i reabsorpcję w nerkach. Co zaskakujące, te myszy rozwijały się normalnie i miały prawidłową strukturę nerek, rozmieszczenie transporterów oraz funkcję w warunkach codziennych. Aby naśladować silne, miejscowe uszkodzenie, które często prowadzi do bliznowacenia, zespół zawiązał jedną moczowód — standardowy zabieg powodujący wzrost ciśnienia, zapalenie i włóknienie w zajętej nerce w ciągu tygodnia. W obu grupach, zarówno u myszy kontrolnych, jak i pozbawionych Exoc5, niedrożność obniżyła poziomy Exoc5, ale zwierzęta z delecją rozwinęły znacznie cięższe zaniknięcie cewek, odkładanie kolagenu i napływ komórek związanych z zapaleniem.
Z uporządkowanych rurek do wędrujących komórek
Zdrowe komórki kanalików są ściśle połączone, z wyraźnie zdefiniowanymi powierzchniami wierzchołkowymi i podstawowymi. W czasie włóknienia często przechodzą „przejście nabłonkowo-mezenchymalne” (EMT) — zmianę ze stanu zakotwiczonego, arkuszowego do bardziej ruchomego, włóknistego. Autorzy stwierdzili, że po niedrożności nerki pozbawione Exoc5 wykazywały silniejszą aktywację kluczowych regulatorów EMT oraz wyższe poziomy białek typowych dla komórek migrujących i produkujących włókna, a także większą utratę białek łączących, które normalnie utrzymują polaryzację komórek kanalików. Zaobserwowali także ponowne pojawienie się Pax2, regulatora rozwojowego zwykle wyłączonego po dojrzeniu kanalików nerkowych. Pax2 powracał silniej w kanalikach pozbawionych Exoc5, szczególnie w komórkach poddanych stresowi, które nie dzieliły się prawidłowo, co sugeruje, że utrata Exoc5 popycha komórki w kierunku pół-naprawionego, zdegradowanego stanu sprzyjającego bliznowaceniu.
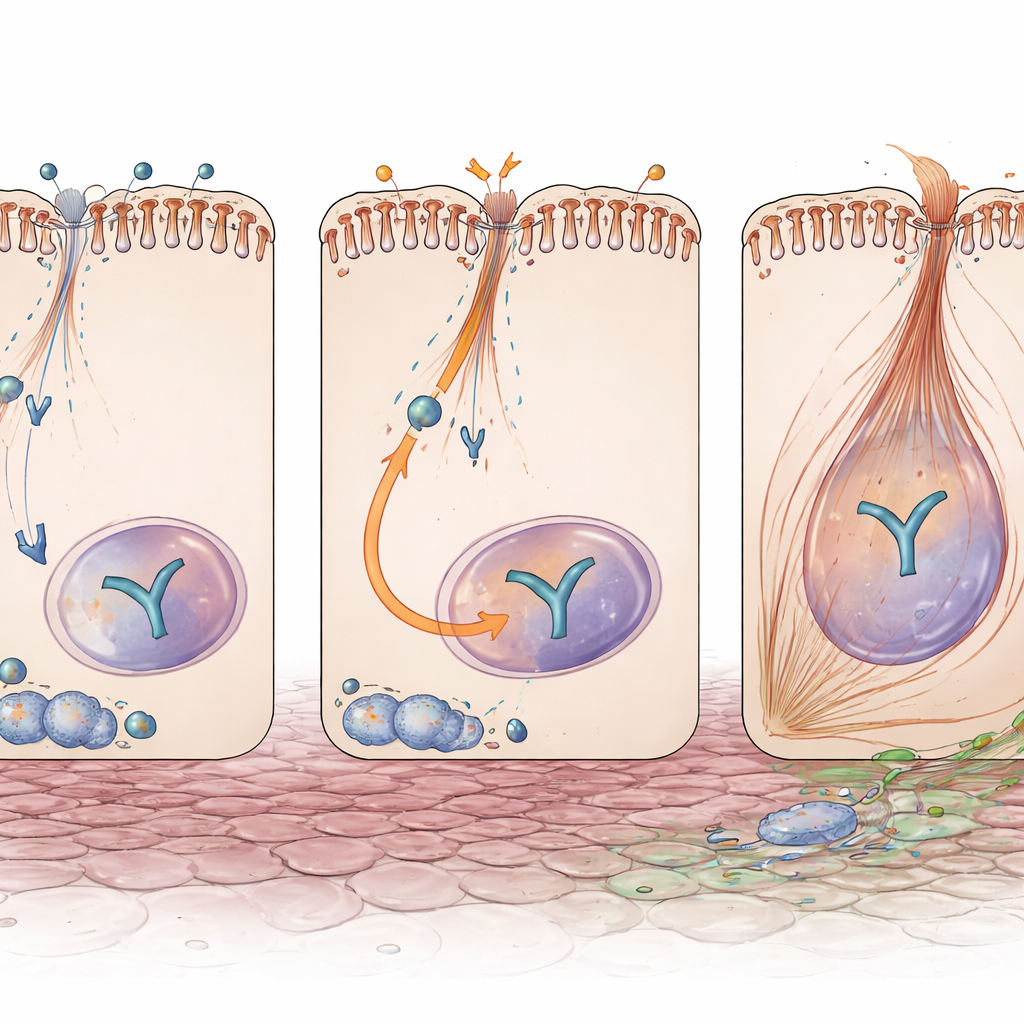
Przełącznik łączący uraz z sygnałami bliznowacenia
Innym centralnym graczem we włóknieniu jest YAP, białko reagujące na sygnały, które przenosi się do jądra, by włączać geny związane z wzrostem i produkcją macierzy. Nawet bez urazu, kanaliki pozbawione Exoc5 miały wyższe poziomy białka YAP. Po niedrożności YAP był silniej aktywowany i skoncentrowany w jądrach komórkowych w tych nerkach, a jego produkty pośrednie — cząsteczki znane z napędzania przebudowy włóknistej — były podwyższone. Co ważne, nie wynikało to z większej aktywności genu YAP, co sugeruje, że Exoc5 normalnie hamuje YAP na poziomie białka lub w transporcie komórkowym. W hodowanych ludzkich komórkach kanalików nerkowych obniżenie poziomu EXOC5 przez interferencję RNA zwiększało YAP i Pax2 oraz sprawiało, że komórki silniej reagowały na fibrogenny sygnał TGF-β, przechodząc bardziej wyraźne zmiany przypominające EMT i częściej nabywając włókienka kurczliwe typowe dla miofibroblastów.
Co to oznacza dla przyszłych terapii
Podsumowując, wyniki ukazują Exoc5 jako cichego strażnika: pod wpływem stresu pomaga komórkom kanalików zachować uporządkowaną tożsamość i powstrzymuje pro-bliznowacie sygnały, takie jak YAP i Pax2. Gdy poziomy Exoc5 spadają — czy to przez utratę genetyczną, czy przez uraz — komórki kanalików łatwiej tracą polaryzację, cofają się do stanu przypominającego rozwój i napędzają proces włóknienia. Ponieważ usunięcie Exoc5 w kanaliku bliższym nie uszkodziło zdrowych nerek, ale wyraźnie pogorszyło bliznowacenie po urazie, praca wskazuje Exoc5 i jego partnerów sygnałowych jako obiecujące cele terapii mających na celu spowolnienie lub odwrócenie włóknienia nerek, zanim przejdzie w niewydolność nerek.
Cytowanie: Lim, H.J., Han, Y.K., Noh, M.R. et al. Deficiency of exocyst complex component Exoc5 exacerbates the progression of kidney fibrosis. Exp Mol Med 58, 681–695 (2026). https://doi.org/10.1038/s12276-026-01649-8
Słowa kluczowe: włóknienie nerek, Exoc5, przejście nabłonkowo-mezenchymalne, sygnalizacja YAP, przewlekła choroba nerek