Clear Sky Science · pl
Postęp stwardnienia rozsianego związany z mikroglejem: identyfikacja celów i angażowanie terapii w ludzkich modelach in vitro
Dlaczego komórki odpornościowe mózgu mają znaczenie w stwardnieniu rozsianym
Stwardnienie rozsiane (SR) często opisywane jest jako choroba, w której układ odpornościowy atakuje mózg i rdzeń kręgowy. Wiele dostępnych leków skutecznie zmniejsza nagłe napady, czyli rzutów, ale nie zatrzymuje powolnego, cichego pogorszenia, którego doświadcza wielu pacjentów przez lata. Niniejszy przegląd wyjaśnia, jak drobne komórki odpornościowe trwale zamieszkujące mózg, zwane mikroglejem, mogą napędzać ten długotrwały spadek — oraz jak nowe, laboratoryjnie hodowane ludzkie modele mózgu pomagają naukowcom znaleźć terapie, które wreszcie spowolnią lub zatrzymają postęp choroby.
Ukryty silnik trwających uszkodzeń
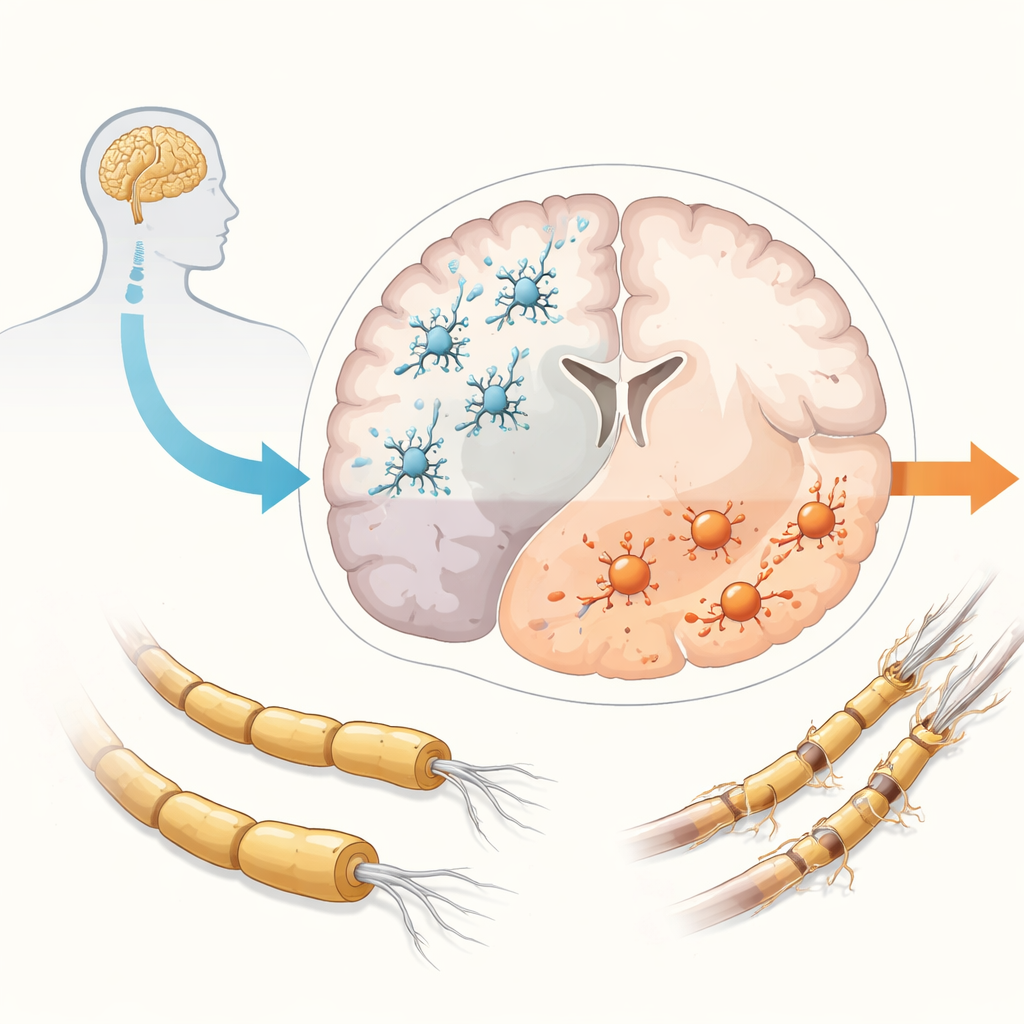
SR tradycyjnie dzielono na postać rzutowo-remisyjną i postępującą, jednak dane wskazują, że postęp zaczyna się bardzo wcześnie u niemal wszystkich chorych, nawet gdy na pierwszy rzut oka występują tylko rzuty. Podczas gdy rzuty są napędzane przez komórki odpornościowe napływające z krwi, postęp wydaje się być zasilany przez zapalenie uwięzione wewnątrz mózgu i rdzenia kręgowego. W tym odizolowanym środowisku mikroglej uczestniczy w wielu szkodliwych procesach: utrzymującym się zapaleniu, utracie izolacyjnej osłonki mielinowej włókien nerwowych w istocie białej i szarej, nagromadzeniu szkodliwych reaktywnych związków tlenowych oraz niepowodzeniu mechanizmów naprawczych. Efektem końcowym jest stopniowa utrata komórek nerwowych i ich połączeń. Mikroglej zwykle pomaga utrzymywać mózg w dobrym stanie przez usuwanie odpadów i wspieranie neuronów, ale w SR często przechodzi w bardziej agresywne stany i traci niektóre z funkcji ochronnych, co czyni go głównym podejrzanym w napędzaniu progresji choroby.
Dlaczego tradycyjne modele zwierzęce zawodzą
Przez dekady badania na myszach i innych zwierzętach były kluczowe dla opracowania leków ograniczających rzuty, lecz w dużej mierze zawiodły w dostarczeniu terapii zatrzymujących postęp choroby. Jednym z powodów jest to, że modele zwierzęce jedynie częściowo naśladują ludzkie SR i nie odtwarzają w pełni złożonego, długotrwałego zapalenia obserwowanego w mózgach pacjentów. Mikroglej gryzoni różni się także od mikrogleju ludzkiego pod względem ważnych genów i odpowiedzi. W rezultacie terapie obiecujące u zwierząt często nie działają u ludzi. Brak modeli zwierzęcych wiernie odzwierciedlających postępujące SR skłonił badaczy do tworzenia nowych systemów opartych na komórkach ludzkich w laboratoriach, gdzie można bezpośredniej badać mikroglej i inne komórki mózgu.
Budowanie ludzkich modeli mózgu na szalce
Naukowcy stosują obecnie kilka warstw modeli laboratoryjnych do badania ludzkiego mikrogleju. Komórki pierwotne pobrane bezpośrednio z tkanki mózgowej gryzoni lub ludzi zachowują wiele naturalnych cech, lecz są trudne do pozyskania, szybko zmieniają się poza natywnym środowiskiem i trudno je skalować. Aby przezwyciężyć te przeszkody, badacze sięgają po indukowane pluripotencjalne komórki macierzyste (iPS) — komórki dorosłe przeprogramowane z powrotem do elastycznego, przypominającego komórki macierzyste stanu. Komórki iPS można ukierunkować, by stały się mikroglejem, neuronami lub innymi komórkami mózgu. W prostych hodowlach dwuwymiarowych mikroglej pochodzący z iPS wykazuje wiele kluczowych cech i może być produkowany w dużych ilościach, co pozwala na szczegółowe eksperymenty i przesiewy leków. Można go nawet uzyskać od poszczególnych pacjentów z SR, ujawniając wrodzone różnice, takie jak zmieniona aktywność genów oraz zmiany w tym, jak komórki te reagują na stres i usuwają zanieczyszczenia.
Dodawanie realistycznych „sąsiedztw” mózgowych
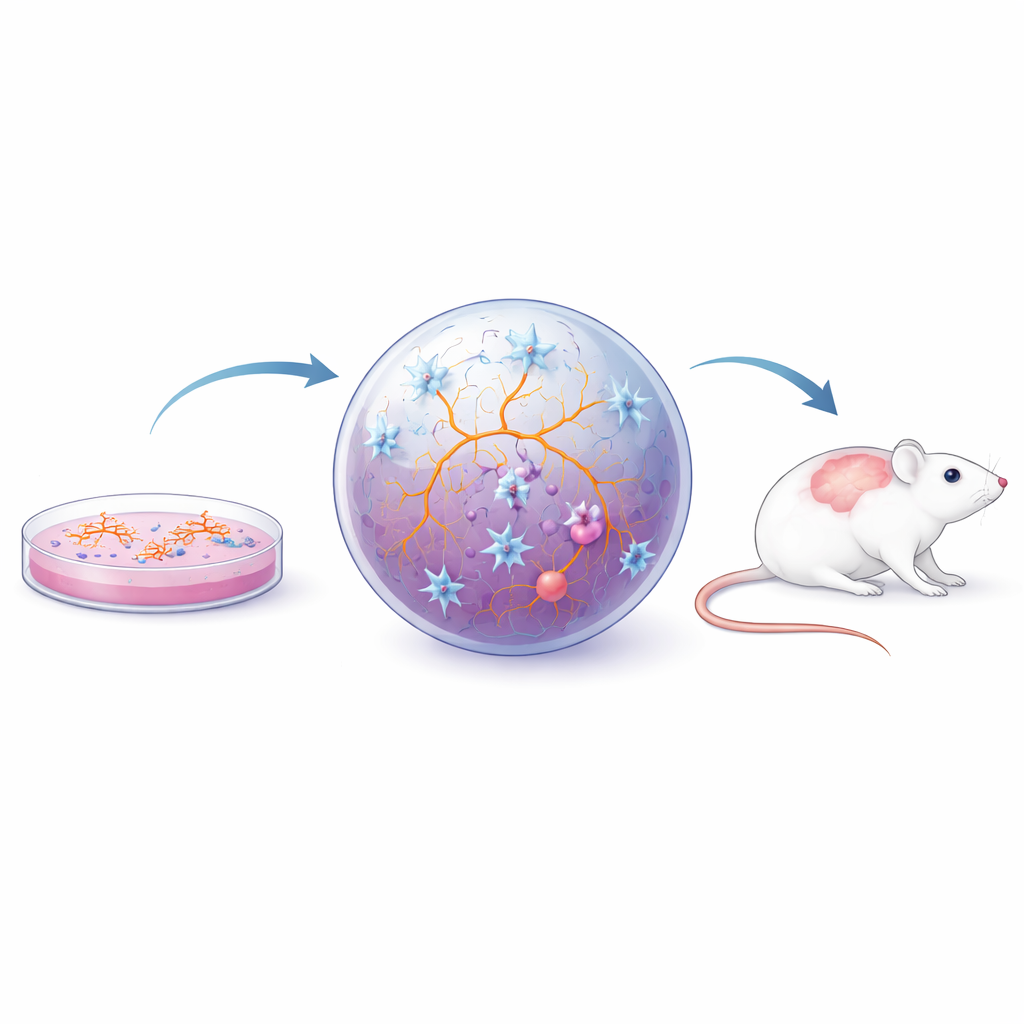
Ponieważ zachowanie mikrogleju w dużym stopniu kształtuje jego otoczenie, badacze wyszli poza pojedyncze warstwy komórkowe do bardziej realistycznych układów. W hodowlach dwuwymiarowych mikroglej rozwija się razem z neuronami i komórkami wspierającymi, co pomaga mu przyjmować bardziej naturalne kształty i zachowania oraz pozwala naukowcom badać wzajemne wpływy typów komórek. Trójwymiarowe sferoidy i organoidy — maleńkie, samoorganizujące się fragmenty tkanki przypominającej mózg — idą dalej, oferując miękkie, zatłoczone środowisko bardziej zbliżone do rzeczywistej tkanki mózgowej. Gdy mikroglej jest osadzony w tych strukturach, przyjmuje rozgałęzione kształty, reaguje na uszkodzenia, współdziała z warstwą przypominającą barierę krew–mózg i odpowiada na sygnały zapalne z płynu mózgowo-rdzeniowego osób z SR. Takie modele służyły do badania, jak przewlekłe zapalenie wywołuje w mikrogleju i astrocytach stan „zmęczony, lecz zapalny” zwany starzeniem komórkowym (senescencją), oraz jak zmiany w metabolizmie lipidów mikrogleju mogą upośledzać naprawę mieliny. Równolegle przeszczepianie ludzkiego mikrogleju lub organoidów pochodzących z iPS do mózgów myszy pozwala tym komórkom dojrzewać dalej w żywym układzie i testować je w ustalonych modelach chorób przypominających SR.
Od modeli laboratoryjnych do przyszłych terapii
W sumie te oparte na ludziach modele in vitro i chimeryczne tworzą zestaw narzędzi do rozkładania na czynniki pierwsze roli mikrogleju w postępie SR oraz do testowania nowych terapii mających na celu stłumienie szkodliwej aktywności mikrogleju przy jednoczesnym przywróceniu jego funkcji ochronnych. Chociaż żaden z modeli nie odtwarza w pełni ludzkiego mózgu, każdy wyłapuje inne fragmenty układanki, a razem wypełniają lukę między prostymi hodowlami komórkowymi a niedoskonałymi modelami zwierzęcymi. Łącząc wnioski z tych systemów, badacze mają nadzieję zidentyfikować precyzyjne cele lekowe — na przykład szlaki kontrolujące zapalenie, zmiany przypominające starzenie i metabolizm lipidów w mikrogleju — które mogłyby w końcu przełożyć się na terapie spowalniające lub zatrzymujące stopniowe upośledzenie charakterystyczne dla postępującego SR.
Cytowanie: Blenkle, A., Geladaris, A. & Weber, M.S. Microglia-associated progression of multiple sclerosis: target identification and therapeutic engagement in human in vitro models. Exp Mol Med 58, 357–365 (2026). https://doi.org/10.1038/s12276-026-01647-w
Słowa kluczowe: postęp stwardnienia rozsianego, mikroglej, komórki macierzyste indukowane pluripotencjalne, organoidy mózgowe, neurozapalenie