Clear Sky Science · pl
PAK4 w chorobach metabolicznych: regulacja przez sygnały odżywcze i implikacje terapeutyczne
Dlaczego przełącznik komórkowy ma znaczenie dla codziennego zdrowia
Otyłość, cukrzyca typu 2 i stłuszczeniowa choroba wątroby są często sprowadzane do kwestii kalorii, ale głęboko w komórkach to molekularne przełączniki decydują, czy spalamy, czy magazynujemy paliwo. Niniejszy przegląd koncentruje się na jednym z takich przełączników — białku o nazwie PAK4 — i wyjaśnia, jak reaguje ono na zmieniające się sygnały odżywcze i hormonalne, przekształcając metabolizm w tkance tłuszczowej, wątrobie i mięśniach. Zrozumienie tego ukrytego systemu sterowania może otworzyć drogę do nowych terapii, które jednocześnie będą zwalczać kilka chorób metabolicznych, zamiast leczyć pojedyncze objawy. 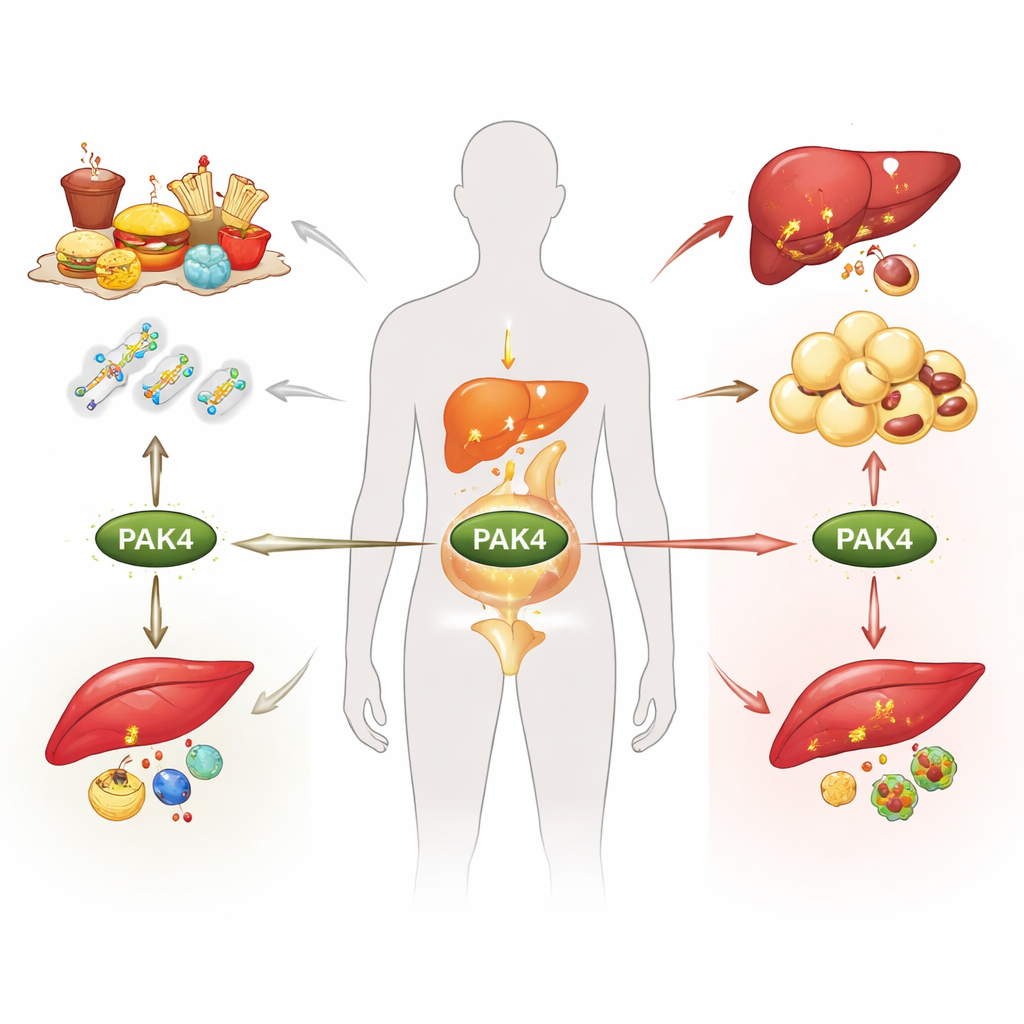
Mistrzowski przełącznik ukryty w naszych komórkach
PAK4 należy do rodziny enzymów przekazujących sygnały od małych molekularnych „kurierów” wewnątrz komórek. W warunkach zdrowych PAK4 występuje na niskim poziomie w głównych narządach metabolicznych. Gdy równowaga energetyczna zostaje zachwiana, jak w otyłości czy cukrzycy typu 2, jego poziomy rosną w tkance tłuszczowej, wątrobie i mięśniach szkieletowych. Aktywność PAK4 jest kontrolowana na kilka sposobów: przez górne sygnały, które zmieniają jego konformację, oraz przez chemiczne znaczniki dodawane lub usuwane po syntezie białka. Należą do nich grupy fosforanowe, które mogą albo aktywować PAK4, albo oznaczać je do degradacji, a także inne modyfikacje wpływające na stabilność i aktywność białka. Głodówka, karmienie, hormony i stres wpływają na te znaczniki, więc PAK4 efektywnie „wyczuwa” stan odżywienia organizmu i przekazuje tę informację do kluczowych szlaków metabolicznych.
Jak PAK4 skłania komórki tłuszczowe ku magazynowaniu
W komórkach tłuszczowych PAK4 działa jak hamulec spalania tłuszczu. Normalnie, podczas głodówki lub przy wzroście hormonów stresu, inny enzym, PKA, uruchamia kontrolowany rozkład zmagazynowanych trójglicerydów w małych kroplach tłuszczu. Przegląd opisuje, jak PAK4 przeciwdziała temu procesowi, umieszczając hamujące grupy fosforanowe bezpośrednio na lipazie wrażliwej na hormony oraz na białku wiążącym kwasy tłuszczowe, które pomaga transportować cząsteczki tłuszczu. Te modyfikacje osłabiają mechanizmy uwalniania tłuszczu ze złogów. PAK4 wspiera też tworzenie nowych komórek tłuszczowych we wcześniejszych etapach życia, ułatwiając białkom cyklu komórkowego przekształcanie prekursorów w dojrzałe komórki magazynujące tłuszcz. Gdy PAK4 jest usunięty lub zablokowany w modelach zwierzęcych, komórki tłuszczowe spalają więcej paliwa, wykazują cechy „brązowienia” zwiększające wykorzystanie energii, a zwierzęta są chronione przed przyrostem masy ciała wywołanym dietą. 
Rola PAK4 w stłuszczeniu wątroby i gospodarce cukrowej mięśni
W wątrobie PAK4 ponownie faworyzuje magazynowanie nad spalaniem. Podczas głodówki lub na diecie ketogennej poziomy PAK4 spadają, co pozwala hepatocytom zwiększyć rozkład tłuszczów i produkcję ketonów, które dostarczają energii innym tkankom i mogą nawet hamować wzrost nowotworów. Gdy PAK4 jest obfity, przyłącza grupy fosforanowe do jądrowego korepresora, który następnie tłumi aktywność PPARα — głównego regulatora utleniania tłuszczów i tworzenia ketonów. W efekcie więcej tłuszczu zostaje uwięzione w wątrobie, a we krwi pojawia się mniej ochronnych ketonów. W mięśniu szkieletowym PAK4 zakłóca działanie AMPK, centralnego sensora energetycznego, który sprzyja zarówno pobieraniu glukozy, jak i aktywności mitochondrialnej. Poprzez modyfikację AMPK w sposób uniemożliwiający jego aktywację, PAK4 obniża ilość transporterów glukozy na powierzchni komórek mięśniowych i przyczynia się do insulinooporności. Usunięcie PAK4 specyficznie w mięśniach myszy odwraca te efekty, poprawiając kontrolę glikemii nawet w warunkach otyłości.
Stres, ochrona i powiązania z innymi przełącznikami komórkowymi
Przegląd podkreśla także wpływ PAK4 poza codziennym metabolizmem. Podczas epizodów zmniejszonego przepływu krwi i nagłego przywrócenia perfuzji w organach takich jak wątroba, PAK4 osłabia obronę antyoksydacyjną, modyfikując i destabilizując Nrf2 — kluczowego strażnika przeciw stresowi oksydacyjnemu. Równocześnie inny członek rodziny, PAK1, często odgrywa role wspierające w mięśniu sercowym, mięśniach szkieletowych i komórkach wydzielających insulinę w trzustce, pomagając utrzymać prawidłową gospodarkę glukozową. Ten kontrast między szkodliwym sygnałem PAK4 w chorobach metabolicznych a na ogół korzystnymi działaniami PAK1 podkreśla potrzebę wysoce selektywnych leków, które wyłączą PAK4, nie zaburzając pokrewnych białek niezbędnych dla zdrowia serca i układu hormonalnego.
Przekształcanie odkrycia w terapię
Ponieważ PAK4 jest nadaktywny w nowotworach i zaburzeniach metabolicznych, projektanci leków poszukiwali małych cząsteczek blokujących jego aktywność, jak również nowych leków „degradujących”, które oznaczają samo białko PAK4 do usunięcia. Wczesne inhibitory PAK4 wykazywały potencjał przeciwnowotworowy, ale napotykały problemy ze specyficznością i farmakokinetyką. Bardziej precyzyjne molekuły opracowane ostatnio dały uderzające wyniki u otyłych myszy: zmniejszenie masy ciała bez ograniczenia apetytu, zdrowsze wątroby, bardziej aktywne mięśnie i poprawa kontroli glikemii. Leki degradowalne idą krok dalej, fizycznie eliminując PAK4, a wczesne badania na zwierzętach sugerują, że mogą chronić przed utratą masy mięśniowej i przed niektórymi nowotworami. Razem te wyniki wspierają obraz, w którym zmniejszenie aktywności PAK4 mogłoby jednocześnie łagodzić otyłość, cukrzycę i stłuszczeniową chorobę wątroby, przekształcając niegdyś mało znany przełącznik komórkowy w obiecujący cel przyszłych terapii metabolicznych.
Cytowanie: Bang, I.H., Park, BH. & Bae, E.J. PAK4 in metabolic diseases: regulation by nutrient signals and therapeutic implications. Exp Mol Med 58, 416–424 (2026). https://doi.org/10.1038/s12276-026-01645-y
Słowa kluczowe: PAK4, choroba metaboliczna, otyłość, stłuszczenie wątroby, oporność na insulinę