Clear Sky Science · pl
Białko wrażliwe na redoks HMGB1: role wewnątrz- i zewnątrzkomórkowe
Dlaczego zmieniające kształt białko ma znaczenie dla zdrowia
W prawie każdej komórce twojego ciała znajduje się niewielkie białko o nazwie HMGB1, które zachowuje się trochę jak wielofunkcyjne narzędzie. W spokoju pomaga uporządkować DNA. Gdy jednak komórki są zestresowane lub uszkodzone, HMGB1 może opuścić jądro, przejść do otaczającej tkanki i działać jak sygnał alarmowy dla układu odpornościowego. Ten przegląd wyjaśnia, jak drobne zmiany chemiczne wywołane utlenianiem przekształcają HMGB1 w bardzo różne biologiczne „osobowości” — takie, które mogą chronić tkanki, napędzać zapalenie lub nawet przyczyniać się do chorób przewlekłych. Zrozumienie tego molekularnego „pierścienia nastrojów” może otworzyć nowe możliwości łagodzenia nadmiernego zapalenia bez całkowitego wyłączenia układu odpornościowego.
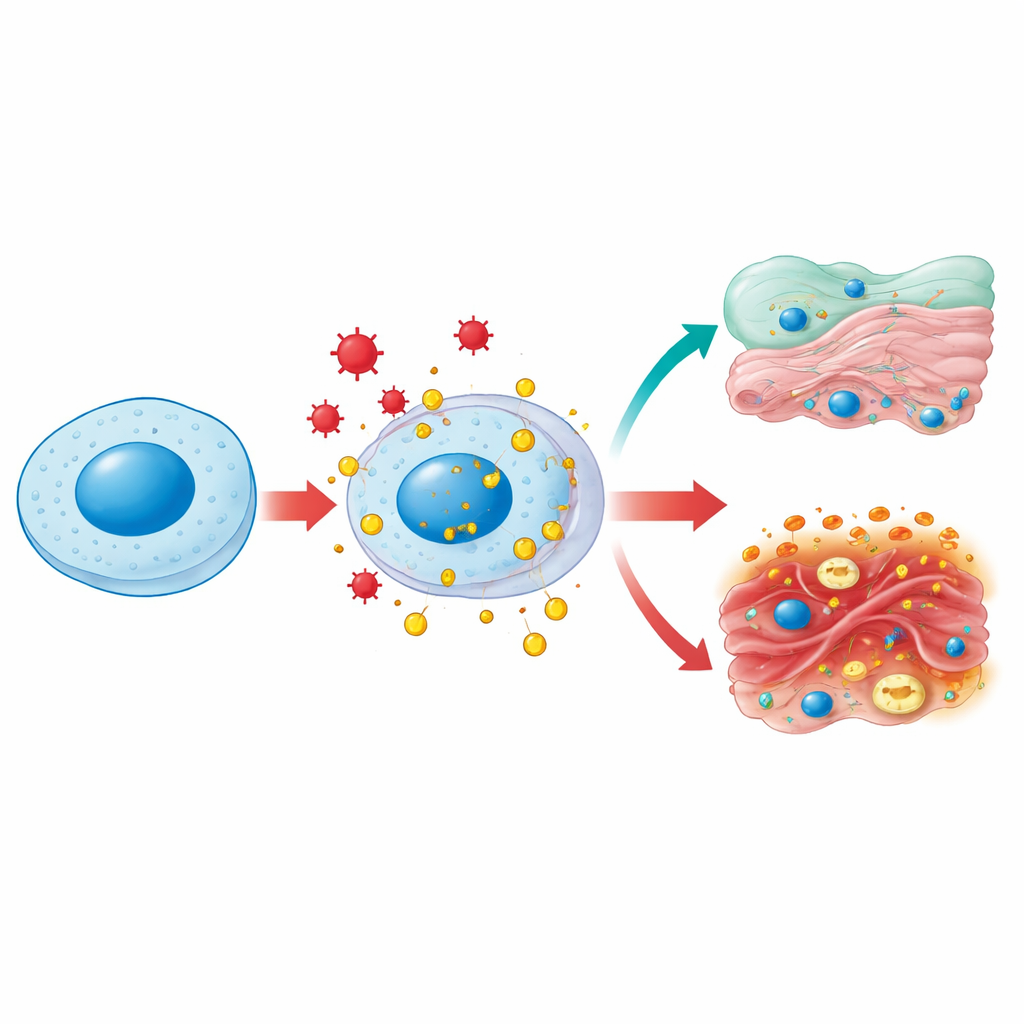
Jedno białko, wiele miejsc działania
HMGB1 na co dzień przebywa w jądrze komórkowym, gdzie zaginając i rozluźniając DNA ułatwia kopiowanie i naprawę genów. Pod wpływem stresu — takiego jak infekcja, wysoki poziom cukru czy uszkodzenie toksyczne — może ulegać modyfikacjom chemicznym i być eskortowane do wnętrza komórki, a następnie na zewnątrz. W cytoplazmie HMGB1 pomaga utrzymywać mitochondria, elektrownie komórki, w dobrym stanie, sprzyjając procesowi oczyszczania zwanemu autofagią i zapobiegając nadmiernemu fragmentowaniu tych organelli. Po uwolnieniu na zewnątrz HMGB1 staje się klasycznym „sygnałem niebezpieczeństwa”: komórki odpornościowe rozpoznają go jako znak uszkodzenia tkanek i przybywają na miejsce. To samo cząsteczka zatem pełni rolę ekipy porządkowej wewnątrz komórek i strażnika alarmowego poza nimi, w zależności od lokalizacji i chemicznego „strojenia”.
Jak utlenianie przepisuje jego zachowanie
Głównym tematem tego przeglądu jest to, jak utlenianie — reakcje napędzane przez reaktywne formy tlenu (ROS) — przekształca HMGB1. Białko zawiera trzy siarkowe reszty, które działają jak małe przełączniki. W stanie w pełni zredukowanym HMGB1 sprzyja przetrwaniu komórek i rekrutacji komórek naprawczych. Łagodne utlenianie może połączyć dwie z tych reszt wewnątrz tej samej cząsteczki, tworząc formę „mostkową” (disiarczkową), która szczególnie dobrze wiąże się z receptorami odpornościowymi, takimi jak receptory Toll-podobne i RAGE na powierzchni komórek. Ta wersja silnie stymuluje produkcję mediatorów zapalnych. Silniejszy stres oksydacyjny może przesunąć cząsteczkę dalej, do postaci nadutlenionej, która nie jest już w stanie skutecznie wiązać DNA ani receptorów; ta „wypalona” forma staje się immunologicznie cicha i wiąże się z fazą ustępowania zapalenia oraz programami śmierci komórkowej, które nie wywołują ataku odpornościowego.
Od sygnałów śmierci komórki do czynników chorobotwórczych
HMGB1 jest ściśle powiązane z wieloma sposobami, w jakie komórki umierają. Podczas gwałtownych form śmierci, takich jak nekroza, nekroptoza, ferroptoza i pyroptoza, HMGB1 wycieka lub jest aktywnie transportowane na zewnątrz komórek, niosąc ze sobą sygnaturę redoks odzwierciedlającą otaczające warunki oksydacyjne. We wczesnej nekrozie przeważa forma zredukowana, podczas gdy przedłużający się stres przesuwa ją w kierunku stanów bardziej utlenionych. Po wydostaniu na zewnątrz zredukowane HMGB1 może sprzyjać ochronnej autofagii w niektórych komórkach nowotworowych, pomagając im przetrwać chemioterapię, podczas gdy formy bogate w mostki disiarczkowe i zdimeryzowane wzmacniają kaskady zapalne i aktywację dopełniacza, co może pogłębiać uszkodzenie tkanek. HMGB1 może również działać zwrotnie, promując określone ścieżki śmierci — na przykład przez współdziałanie z lipidami bakteryjnymi w celu uruchomienia nekroptozy lub poprzez wywoływanie zależnej od żelaza śmierci komórek wspierających mózg po udarze. W ten sposób HMGB1 zarówno oznacza, jak i modyfikuje równowagę życia i śmierci w tkankach.
Powiązania z zapaleniem, autoimmunizacją i rakiem
Ze względu na wysoką wrażliwość na utlenianie, różne warianty HMGB1 pojawiają się w odmiennych wzorcach w chorobach. HMGB1 bogate w mostki disiarczkowe jest silnie związane z przewlekłym zapaleniem: występuje w zapalnych stawach w reumatoidalnym zapaleniu stawów, w zwłókniałej wątrobie, w uszkodzeniach płuc, w uszkodzeniach niedokrwienno-reperfuzyjnych po operacji oraz w sepsie, gdzie jego poziomy we krwi korelują z ciężkością i ryzykiem zgonu. Z kolei zredukowane HMGB1 często wiąże się z migracją komórek i przebudową tkanek, jak przemieszczanie się fibroblastów serca czy monocytów kierowanych przez chemokinę CXCL12. Nadutleniona, immunologicznie cicha forma HMGB1 jest wzbogacona w sytuacjach takich jak późne etapy apoptozy, gdzie organizm chce usunąć umierające komórki bez wywoływania ataku. W guzie forma disiarczkowa wspiera tłumiące, sprzyjające wzrostowi środowisko immunologiczne, podczas gdy blokowanie HMGB1 może zmniejszać guzy i zwiększać skuteczność terapeutycznych inhibitorów punktów kontrolnych immunologicznych.
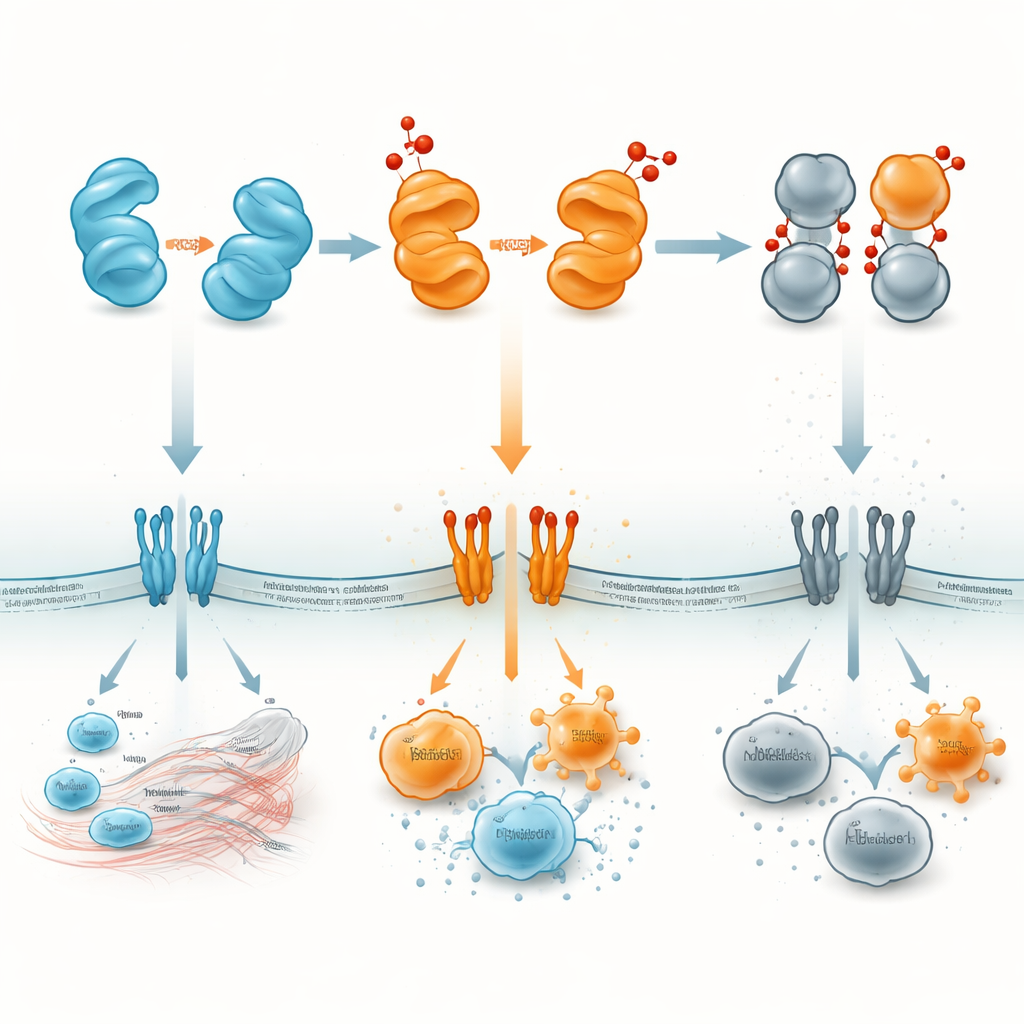
Przekształcanie molekularnego alarmu w cel terapeutyczny
Dla laika HMGB1 można uważać za niewielki białkowy alarm, którego głośność i przekaz zmieniają się wraz ze stanem chemicznym. Zredukowane HMGB1 zwykle wzywa ekipy naprawcze; formy disiarczkowe i dimerowe mogą rozlegać ostry alarm, który napędza szkodliwe zapalenie; a w pełni utleniona forma w praktyce milknie, pomagając wygasić zapalenie. Mapując, gdzie i kiedy pojawia się każda wersja — wewnątrz jąder, w cytoplazmie, we krwi czy w określonych narządach — badacze mają nadzieję projektować leki, które blokują formy szkodliwe lub stabilizują te korzystne. Takie strategie mogą pozwolić lekarzom leczyć sepsę, choroby autoimmunologiczne, udar, uszkodzenia płuc czy raka, celując nie tylko w samo HMGB1, lecz także w oksydacyjny „ściemniacz”, który kontroluje, jak to białko komunikuje się z układem odpornościowym.
Cytowanie: Kwak, M.S., Jung, S.F., Park, I.H. et al. The redox-sensitive protein HMGB1: intracellular and extracellular roles. Exp Mol Med 58, 345–356 (2026). https://doi.org/10.1038/s12276-026-01640-3
Słowa kluczowe: HMGB1, zapaleni e, stres oksydacyjny, śmierć komórki, choroba autoimmunologiczna