Clear Sky Science · pl
Mechanotransdukcja przez receptory limfocytów T: konsensus, kontrowersje i perspektywy na przyszłość
Jak komórki odpornościowe wyczuwają świat
Nasz układ odpornościowy robi więcej niż wykrywa sygnały chemiczne; on także odczuwa siły fizyczne. Ten przeglądowy artykuł bada, jak limfocyty T — białe krwinki polujące na wirusy i komórki nowotworowe — mogą wykorzystywać niewielkie pchnięcia i pociągnięcia na swoich receptorach powierzchniowych, aby zdecydować, czy zaatakować. Zrozumienie tego „zmysłu dotyku” na skali molekularnej może zmienić sposób, w jaki myślimy o szczepionkach, immunoterapii przeciwnowotworowej i chorobach autoimmunologicznych.
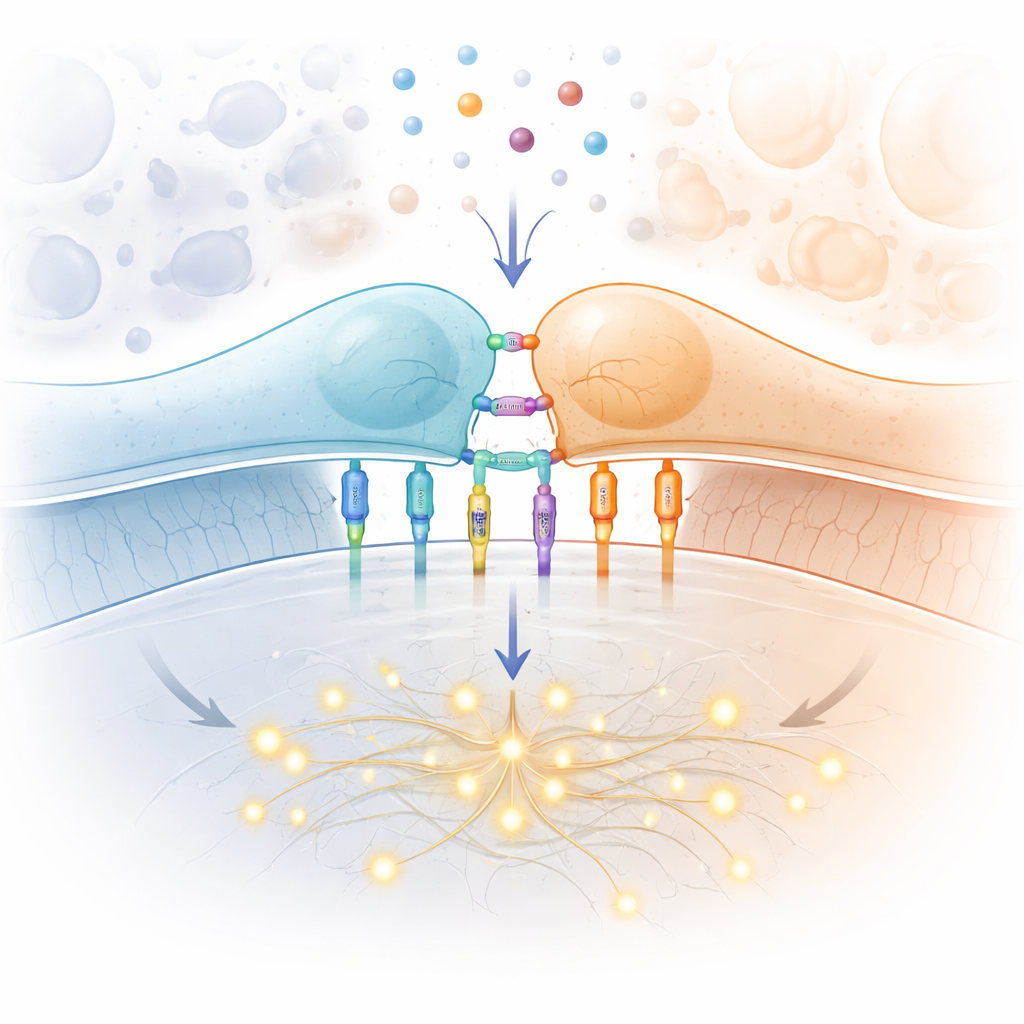
Szczególna rola receptora limfocytu T
W centrum tej opowieści znajduje się receptor limfocytu T, molekularna maszyna na powierzchni komórki T, która inspekcjonuje fragmenty białek prezentowane przez inne komórki. Gdy znajdzie właściwy fragment, limfocyt T może przejść do akcji, mnożyć się i zabijać zainfekowane lub nowotworowe cele. Receptor musi sprostać trudnym wymaganiom: reagować na znikome ilości obcych fragmentów, ignorować morze nieszkodliwych własnych fragmentów, działać szybko podczas patrolowania organizmu i robić to dla milionów różnych wariantów receptorów u każdej osoby. Klasyczne okablowanie szlaku sygnałowego wewnątrz komórki — obejmujące kinazy białkowe, białka szkieletowe i czynniki transkrypcyjne — jest dobrze zmapowane. To, co pozostaje tajemnicą, to pierwszy krok: jak proste związanie fragmentu na powierzchni komórki przełącza receptor z ciszy w aktywność.
Konkurujące idee dotyczące pierwszego zapłonu
Naukowcy zaproponowali kilka modeli opisujących, jak receptor limfocytu T najpierw się włącza. W jednym ujęciu sygnalizacja zaczyna się, gdy receptory zbierają się w małe skupiska, zwiększając lokalne stężenie i umożliwiając wydajniejsze przebiegi reakcji sygnałowych. Inna koncepcja podkreśla zmiany kształtu: związanie może skręcić lub rozluźnić części kompleksu receptora, uwalniając ukryte fragmenty wewnątrz komórki, aby enzymy mogły je modyfikować. Trzeci model zwraca uwagę na zagęszczenie w strefie kontaktu między komórkami. Tutaj krótkie pary receptor–ligand upakowują się w ciasne obszary, które fizycznie wykluczają obszerne enzymy zwykle wyłączające sygnały, przechylając bilans na korzyść aktywacji. Każdy model ma wsparcie eksperymentalne i wyjaśnia część zagadki, lecz żaden z nich samodzielnie nie tłumaczy w pełni ekstremalnej czułości receptora i jego zdolności do rozróżniania bardzo podobnych fragmentów białkowych.
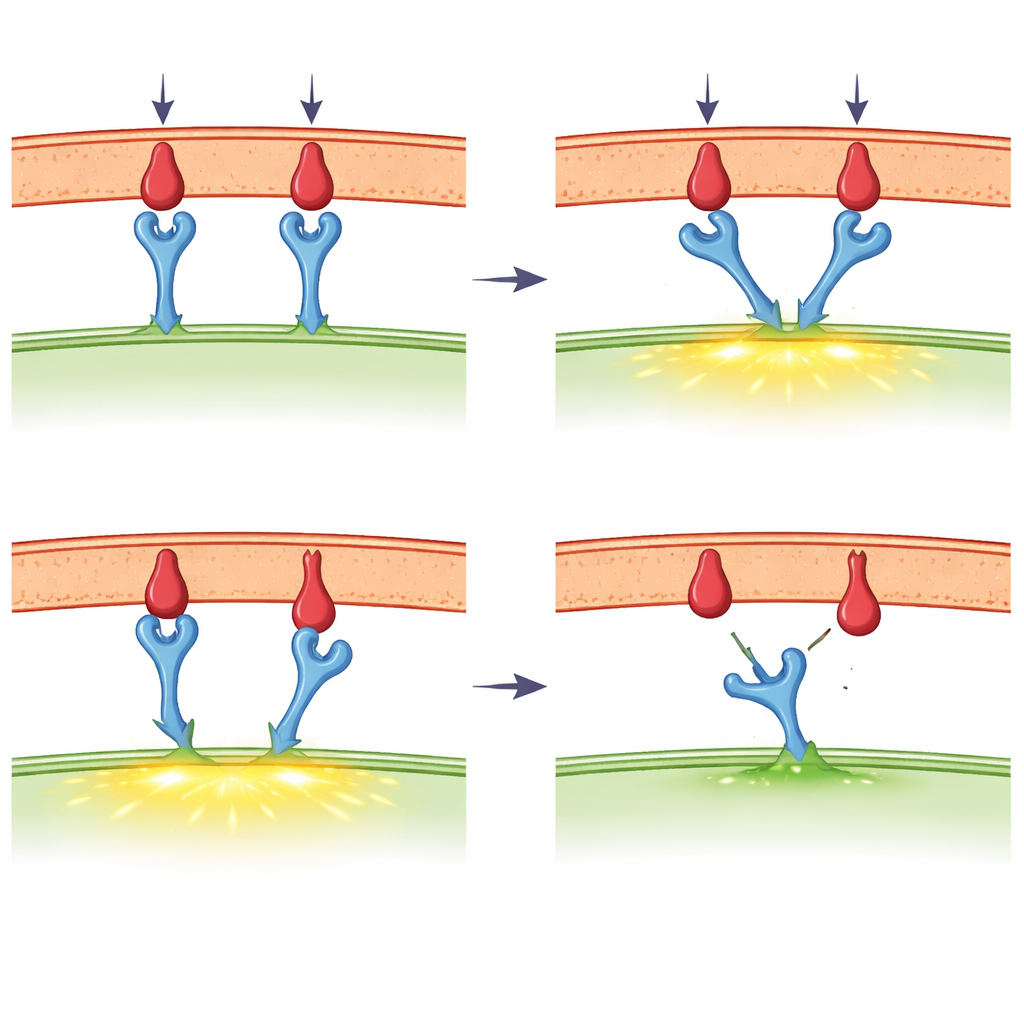
Gdy do gry wchodzą dotyk i siła
Główny nacisk przeglądu kładzie się na pojawiający się pomysł, że receptor limfocytu T zachowuje się jak mechanosensor — urządzenie reagujące na siłę. Przy użyciu ultrasensytywnych instrumentów naukowcy ciągnęli za pojedyncze wiązania receptor–ligand z siłami bilion razy mniejszymi niż ciężar jabłka. Stwierdzili, że dla silnych obcych fragmentów umiarkowane pociągnięcie może wydłużyć czas trwania wiązania, zachowanie znane jako reakcja typu „catch”. Słabsze lub własne fragmenty wykazują zamiast tego zachowanie „slip”: rozrywają się szybciej pod naciskiem. Same limfocyty T generują takie siły za pomocą wewnętrznego szkieletu z filamentów aktynowych i białek motorycznych, szczególnie w ciasnej strefie kontaktu zwanej synapsą immunologiczną. Nowe molekularne sondy napięcia pokazują, że siły w zakresie, w którym pojawia się zachowanie typu catch, rzeczywiście występują podczas wczesnej aktywacji limfocytów T, choć różne metody eksperymentalne czasem raportują odmienne wartości i wzbudziły żywą debatę.
Rozróżnianie siebie od nie-siebie w czasie
Artykuł ponownie omawia również, jak limfocyty T mogą zamieniać hałaśliwe, krótkotrwałe kontakty w wiarygodne decyzje. Dawno utrzymywany pomysł, zwany kinetic proofreading (sprawdzaniem kinetycznym), sugeruje, że sygnalizacja przebiega przez sekwencję kroków wymagających czasu; tylko fragmenty utrzymujące receptor wystarczająco długo pozwalają łańcuchowi osiągnąć punkt bez powrotu. Autorzy dyskutują, jak efekty mechaniczne mogą wyostrzyć ten filtr czasowy: siły pociągające wydłużają żywotność produktywnych wiązań i skracają nieproduktywnych, poszerzając różnicę między silnymi a słabymi bodźcami. Rozważają też, jak limfocyty mogą integrować wiele krótkich kontaktów zamiast polegać na jednym długim, oraz jak sprzężenia zwrotne w obrębie sieci sygnałowej mogą przechowywać rodzaj molekularnej „pamięci” niedawnych spotkań. Te udoskonalenia pomagają wyjaśnić, jak limfocyty T osiągają jednocześnie szybkość i dokładność w złożonych środowiskach tkankowych.
Wspólne zasady w różnych receptorach odpornościowych
Chociaż receptor limfocytu T stawia wyjątkowo wysokie wymagania, wiele jego zasad projektowych pojawia się także w innych receptorach odpornościowych. Receptory komórek B i receptory przeciwciał na komórkach odpornościowych wrodzonych dzielą podobne motywy sygnałowe i często działają w strefach bliskiego kontaktu, gdzie zagęszczenie, skupianie i siły cytoszkieletu mają znaczenie. Reakcje przypominające catch na siłę zostały już zgłoszone dla kilku takich par receptor–ligand. Sugeruje to, że odczuwanie wskazówek mechanicznych może być ogólną strategią, jaką układ odpornościowy wykorzystuje, aby sprawdzić, czy cel jest mocno zakotwiczony, prawidłowo zaprezentowany i wart reakcji.
Dlaczego to ma znaczenie dla zdrowia i terapii
Dla czytelnika niebędącego specjalistą wniosek jest taki, że limfocyty T nie tylko „wąchają” obecność obcych cząsteczek — one także testują, jak te cząsteczki zachowują się pod pociągnięciem. Łącząc chemię, fizykę i biologię komórki, ten przegląd argumentuje, że receptory odpornościowe przekształcają subtelne różnice zarówno w wiązaniu, jak i w działaniu sił w decyzje o życiu lub śmierci komórek. Głębsze zrozumienie tych zasad mechanobiologicznych może ukierunkować projekt lepszych terapii opartych na limfocytach T, precyzyjniejszych szczepionek oraz nowych leczeń, które regulują odpowiedzi immunologiczne, zmieniając nie tylko to, do czego receptory się wiążą, ale także jak są mechanicznie angażowane.
Cytowanie: Travaglino, S., Jeon, Y., Kim, Y. et al. Mechanotransduction through T cell receptors: consensus, controversies and future outlooks. Exp Mol Med 58, 319–335 (2026). https://doi.org/10.1038/s12276-026-01639-w
Słowa kluczowe: receptor limfocytu T, mechanotransdukcja, wiązania typu catch, synapsa immunologiczna, sprawdzanie kinetyczne