Clear Sky Science · pl
UBE2M jako most łączący neddylację i regulację cyklu komórkowego w gruczolakorakach jelita grubego
Dlaczego to badanie ma znaczenie dla raka jelita
Rak jelita grubego jest jednym z najczęstszych i najgroźniejszych nowotworów na świecie, głównie dlatego, że komórki nowotworowe uczą się dzielić bez ograniczeń. To badanie ujawnia wcześniej nieznany przełącznik kontrolny, który pomaga komórkom raka jelita szybko przechodzić przez krytyczny punkt kontrolny podziału. Pokazując, jak ten przełącznik działa na poziomie molekularnym — oraz że istniejący lek przeciwgrzybiczy może mu przeszkodzić — praca wskazuje potencjalnie nowy sposób spowolnienia lub zatrzymania wzrostu guza.
Ukryta warstwa regulacji wewnątrz komórek nowotworowych
Komórki nie dzielą się przypadkowo; przechodzą uporządkowany cykl z punktami kontrolnymi, które sprawdzają, czy bezpiecznie można skopiować DNA i rozdzielić komórkę na dwie. Komórki nowotworowe często modyfikują te punkty kontrolne. Autorzy skupili się na chemicznym procesie znakowania białek zwanym neddylacją, który subtelnie zmienia białka po ich syntezie. Wcześniejsze badania sugerowały, że neddylacja jest bardziej aktywna w wielu nowotworach, lecz sposób jej powiązania z cyklem podziałowym komórek raka jelita był niejasny. Wykorzystując obszerne dane pojedynczych komórek z ludzkich guzów oraz zbiorcze dane ekspresji genów od ponad 1800 pacjentów, zespół odkrył, że aktywność neddylacji jest szczególnie wysoka w złośliwych komórkach jelita znajdujących się w fazie G2/M — ostatniej bramie przed podziałem komórki.
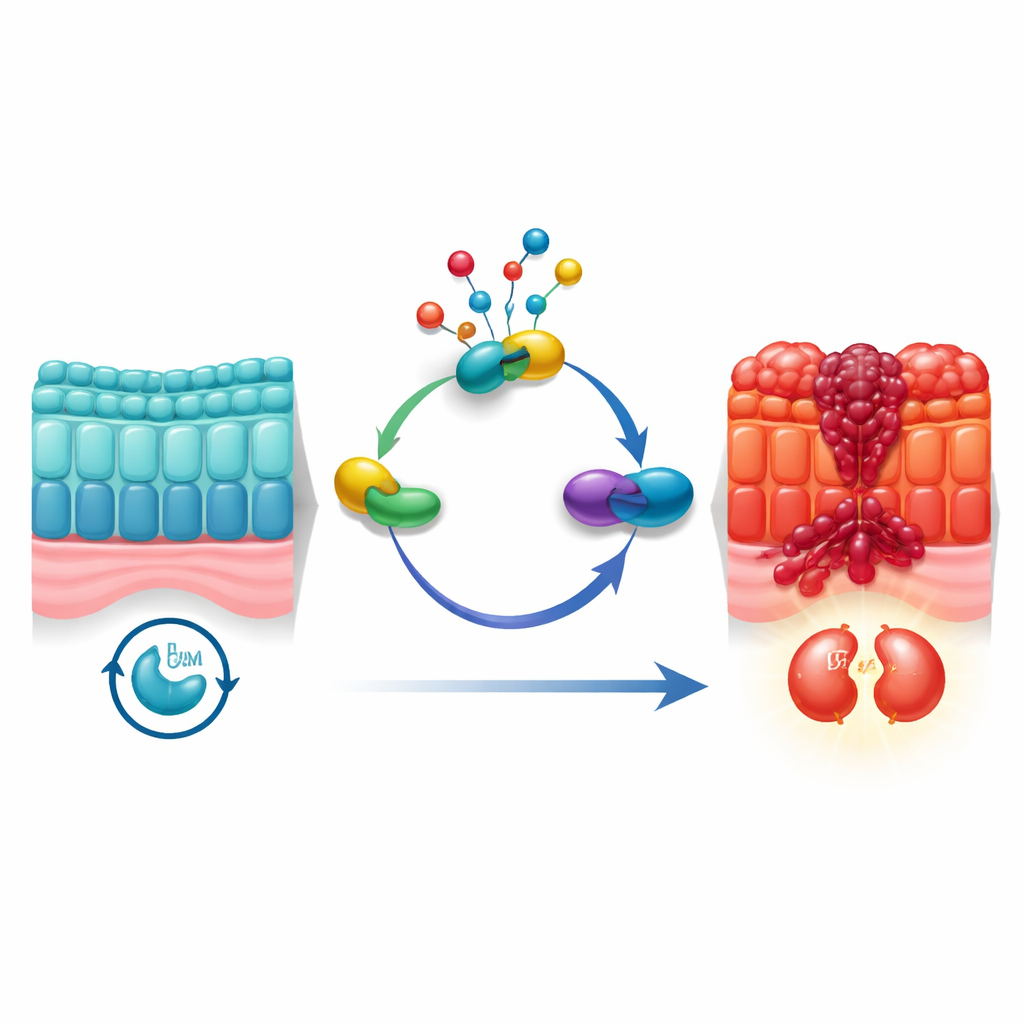
Uwypuklenie molekularnego „mostu”
Aby ustalić, które molekuły łączą neddylację z podziałem komórkowym, badacze zastosowali analizy sieciowe do przesiania tysięcy genów. Jedno białko wyróżniało się wyraźnie: UBE2M, enzym pomagający przyłączać małą grupę NEDD8 do innych białek. UBE2M nie tylko silnie korelował w danych ze szlakami neddylacji i cyklu komórkowego; występował też na znacznie wyższym poziomie w guzach jelita w porównaniu z przylegającą tkanką normalną. Pacjenci, których guzy miały więcej UBE2M, mieli zazwyczaj gorsze przeżycie, co wskazuje, że może on pełnić rolę czynnika napędowego, a nie tylko obserwatora. Redukcja UBE2M w liniach komórkowych raka i w modelach mysich spowalniała wzrost guza, zmniejszała liczbę podziałów i zwiększała odsetek komórek ulegających zaprogramowanej śmierci. Natomiast przymusowa nadekspresja UBE2M przyspieszała wzrost i postęp cyklu komórkowego.
Przekaźnik chroniący kluczowe białko promujące wzrost
Wnikliwsze badania wykazały, w jaki sposób UBE2M ułatwia podział komórek. Odkryto, że UBE2M nie działa samodzielnie, lecz uruchamia przekaźnik obejmujący dwa inne białka: USP39 i PABPC1. Zwykle PABPC1 jest oznaczane łańcuchem ubikwityny, co kieruje je do komórkowego systemu degradacji białek. Zespół pokazał, że UBE2M chemicznie modyfikuje USP39 poprzez przyłączenie NEDD8. Ta modyfikacja zwiększa zdolność USP39 do usuwania łańcuchów ubikwityny z PABPC1, chroniąc je przed zniszczeniem i stabilizując. Przy wyższych poziomach PABPC1 komórka staje się bardziej efektywna w translacji wybranych mRNA na białka, w tym mRNA dla CCNB1, cykliny działającej jak pedał gazu w punkcie kontrolnym G2/M. W istocie UBE2M pomaga stabilizować PABPC1, co z kolei zwiększa produkcję CCNB1, ułatwiając wejście komórek w podział.
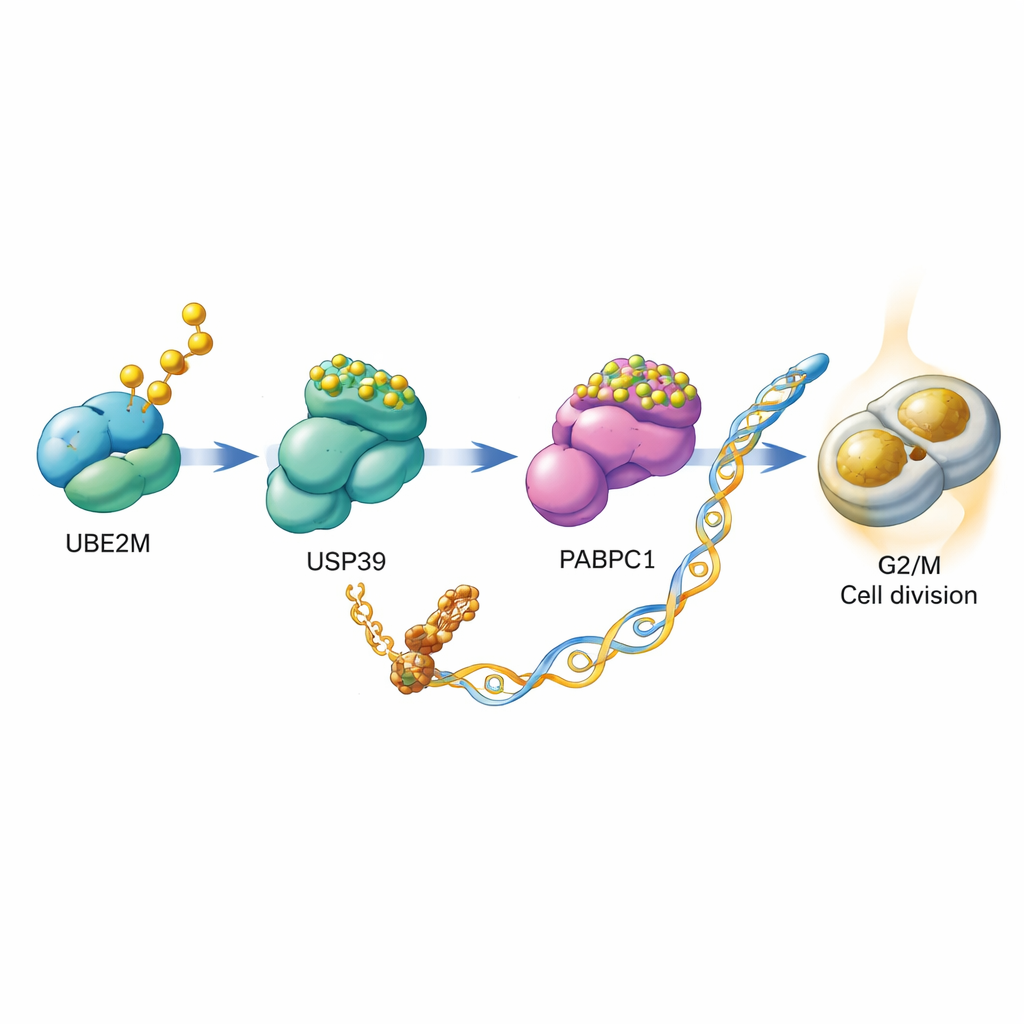
Od mechanizmu molekularnego do możliwości terapeutycznej
Odkrycie łańcucha UBE2M–USP39–PABPC1–CCNB1 ujawniło nową słabość komórek raka jelita. Autorzy zwrócili się ku mikafunginie, lekowi już stosowanemu w leczeniu zakażeń grzybiczych, który niedawno został zidentyfikowany jako inhibitor aktywności neddylacyjnej UBE2M. W hodowlach komórek raka jelita mikafungina osłabiła neddylację USP39, zwiększyła degradację PABPC1 i obniżyła poziomy białka CCNB1. W efekcie tempo podziałów spadło, więcej komórek utknęło w punkcie G2/M, a apoptoza wzrosła. U myszy wszczepionych komórkami raka jelita codzienne leczenie mikafunginą znacząco zmniejszyło guzy w porównaniu z grupą nieleczoną, bez konieczności usuwania samego UBE2M.
Co to może znaczyć dla pacjentów w dłuższej perspektywie
Praca ta klarownie ilustruje, jak pojedynczy enzym, UBE2M, może łączyć subtelny system znakowania białek z decyzją komórki raka jelita o podziale. Stabilizując czynnik translacyjny (PABPC1) za pośrednictwem USP39, UBE2M pośrednio podnosi poziomy silnego regulatora cyklu komórkowego, CCNB1, pozwalając guzom rosnąć szybciej. Chociaż potrzebne są dalsze badania i testy kliniczne, wyniki sugerują, że zablokowanie tego przekaźnika — potencjalnie przy użyciu leków do ponownego zastosowania, takich jak mikafungina — mogłoby stanowić nową, skierowaną strategię spowalniającą postęp raka jelita i poprawiającą rokowania pacjentów.
Cytowanie: Wang, Z., Wang, Y., Chen, Y. et al. UBE2M as a bridge spanning neddylation and cell cycle regulation in colorectal adenocarcinoma. Exp Mol Med 58, 501–518 (2026). https://doi.org/10.1038/s12276-026-01636-z
Słowa kluczowe: rak jelita grubego, cykl komórkowy, neddylacja, UBE2M, terapia celowana