Clear Sky Science · pl
Toksyczność jelitowa wywołana lekami i integralność bariery: upośledzenie związane z cytoszkieletem w klinicznie istotnym modelu ludzkiego nabłonka jelitowego
Dlaczego działania niepożądane w jelitach mają znaczenie
Wiele leków stosowanych w walce z rakiem, stanami zapalnymi czy innymi chorobami może niezamierzenie uszkadzać wyściółkę naszych jelit. Gdy ta wewnętrzna „skóra” jelita zostanie naruszona, pacjenci mogą doświadczać biegunki, bólu, nudności i zaburzeń wchłaniania składników odżywczych — czasem na tyle poważnych, że lekarze muszą przerwać lub zmniejszyć dawki ratujących życie terapii. Tymczasem dzisiejsze testy laboratoryjne często nie wykrywają tych problemów zanim leki trafią do pacjentów. Badanie przedstawia bardziej realistyczny model jelita człowieka w warunkach laboratoryjnych i pokazuje, jak może on wcześniej wychwytywać leki uszkadzające jelito oraz ujawniać, w jaki sposób osłabiają one naturalną barierę organizmu.
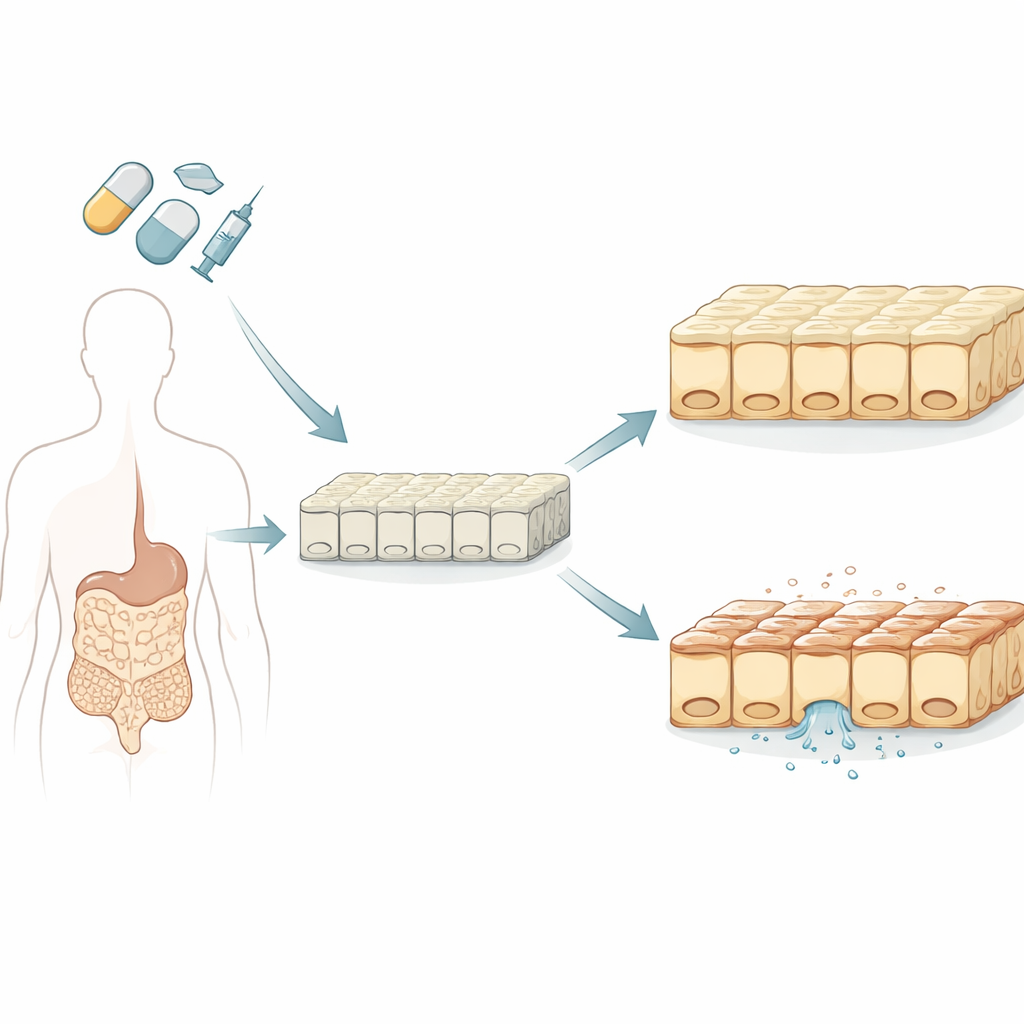
Budowanie lepszego mini-jelita
Naukowcy zaczęli od hodowli arkuszy ludzkich komórek jelitowych w laboratorium, wykorzystując komórki macierzyste, które mogą różnicować się w różne typy tkanek. W przeciwieństwie do tradycyjnych linii komórkowych pochodzących z nowotworów, długo używanych do testów leków, komórki pochodzące z komórek macierzystych utworzyły zróżnicowaną społeczność bardziej zbliżoną do prawdziwego jelita cienkiego, w tym komórki wydzielające śluz oraz produkujące hormony. Zespół potwierdził, że te laboratoryjnie wyhodowane wyściółki wykazują realistyczną szczelność, właściwą polaryzację góra‑dół oraz kluczowe cechy transportu i metabolizmu, które wpływają na to, jak leki przemieszczają się przez jelito i są tam przetwarzane.
Pomiary elektrycznej szczelności bariery
Aby ocenić bezpieczeństwo dla jelit, grupa skupiła się na transepithelial electrical resistance (TEER) — nieinwazyjnym wskaźniku tego, jak szczelnie przylegają do siebie sąsiednie komórki. Wysokie TEER oznacza zwartą, ochronną barierę; spadające TEER sygnalizuje, że przegroda między jelitem a krwią staje się nieszczelna. Naukowcy porównali TEER z klasycznym testem przeżywalności komórek mierzącym cząsteczki energetyczne, takie jak ATP. Zarówno nowy model jelitowy, jak i starsza linia komórek nowotworowych zostały poddane ekspozycji na 17 leków, o znanym zróżnicowanym ryzyku wywoływania działań niepożądanych w układzie pokarmowym, w tym powszechnie stosowane leki chemioterapeutyczne, celowane pigułki przeciwnowotworowe oraz leki przeciwbólowe, takie jak ibuprofen i inne niesteroidowe leki przeciwzapalne.
Wykrywanie ukrytych uszkodzeń zanim komórki umrą
W całym tym zestawie leków pomiary TEER na wyściółce pochodzącej z komórek macierzystych przewyższyły wyniki tradycyjnego testu ATP oraz bariery z komórek nowotworowych. Kilka leków chemioterapeutycznych nie wykazywało dużych zmian ATP, co sugerowało, że komórki nadal żyją, a mimo to powodowały znaczne spadki TEER oraz wyraźne uszkodzenia widoczne w barwieniach żywy‑martwy. Oznacza to, że bariera może zawodzić zanim komórki całkowicie obumrą — wczesny sygnał, który omijają klasyczne testy przeżywalności. Porównując wyniki laboratoryjne z danymi klinicznymi dotyczącymi częstości, z jaką każdy lek wywołuje objawy jelitowe, nowy test TEER prawidłowo wykrywał niemal wszystkie leki o wyższym ryzyku i prawidłowo uspokajał w przypadku leków niskiego ryzyka, osiągając bardzo wysoką dokładność.
Jak leki podkopują wewnętrzny szkielet
Aby odkryć, co zawodzi w komórkach, naukowcy przeanalizowali aktywność genów po leczeniu dwoma lekami chemioterapeutycznymi celującymi w mikrotubule — kluczowy element wewnętrznego szkieletu komórki. Stwierdzili szerokie obniżenie ekspresji genów związanych z cytoszkieletem, adhezją międzykomórkową oraz macierzą pozakomórkową — siecią, która pomaga komórkom kotwiczyć się w otoczeniu. Dalsze eksperymenty wykazały zależne od dawki wzrosty reaktywnych form tlenu, niestabilnych cząsteczek zawierających tlen, które mogą uszkadzać struktury komórkowe. Razem te zmiany wskazują na łańcuch zdarzeń, w którym niektóre leki zaburzają wewnętrzne rusztowanie i połączenia komórek jelitowych, rozluźniając barierę i umożliwiając przeciekanie substancji między komórkami.
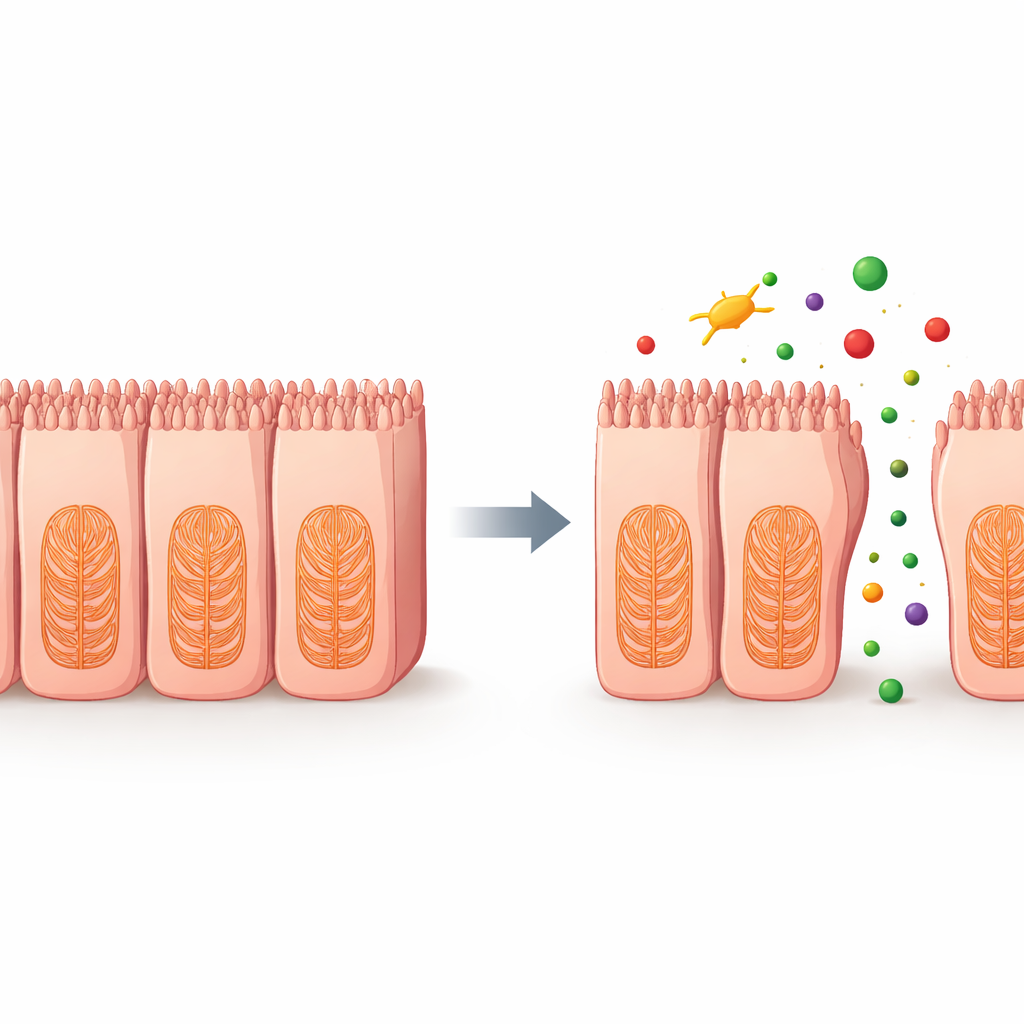
Co to oznacza dla pacjentów
Praca ta pokazuje, że ludzka wyściółka jelit oparta na komórkach macierzystych, połączona z prostymi pomiarami elektrycznymi szczelności bariery, może bardziej niezawodnie przewidzieć, które leki prawdopodobnie spowodują uszkodzenia jelit niż długo stosowane metody laboratoryjne. Dzięki wczesnemu wykrywaniu osłabienia bariery — i powiązaniu tego z uszkodzeniami podstawowego rusztowania komórkowego — platforma ta może pomóc deweloperom leków odrzucać lub przeprojektowywać ryzykowne związki zanim trafią do kliniki. W dłuższej perspektywie takie realistyczne testy „mini‑jelit” mogą zmniejszyć nieprzyjemne lub niebezpieczne działania niepożądane w układzie pokarmowym u pacjentów, jednocześnie pozwalając lekarzom bezpieczniej stosować silne terapie.
Cytowanie: Yu, W.D., Lee, S., Cho, HS. et al. Drug-induced gastrointestinal toxicity and barrier integrity: cytoskeleton-mediated impairment in a clinically relevant human intestinal epithelium model. Exp Mol Med 58, 487–500 (2026). https://doi.org/10.1038/s12276-025-01635-6
Słowa kluczowe: toksyczność jelitowa, bariera jelitowa, model komórek macierzystych, bezpieczeństwo leków, skutki uboczne chemioterapii