Clear Sky Science · pl
CDK13 napędza raka jasnokomórkowego nerki poprzez m6A-modyfikację mRNA ACLY zależną od METTL16
Dlaczego tłuszcz w guzach nerek ma znaczenie
Rak jasnokomórkowy nerki często wygląda pod mikroskopem na blady i oleisty, ponieważ jego komórki są wypełnione tłuszczem. Ten nietypowy wygląd to nie tylko cecha wyglądu — odzwierciedla głębszą zmianę w sposobie, w jaki komórki nowotworowe gospodarują paliwem. W badaniu postawiono proste, lecz istotne pytanie: jaki molekularny przełącznik nakazuje komórkom guza nerki gromadzić tłuszcz i czy można go wyłączyć, by spowolnić rozwój choroby?
Ukryty dyrygent wzrostu guza
Naukowcy skoncentrowali się na białku nazwanym CDK13, należącym do rodziny enzymów, które zwykle pomagają komórkom się dzielić. Analiza dużych zbiorów danych pacjentów i próbek guza wykazała, że poziomy CDK13 są konsekwentnie wyższe w raku jasnokomórkowym nerki niż w zdrowej tkance nerkowej. Pacjenci z guzami o wyższej ekspresji CDK13 mieli skłonność do większych, bardziej zaawansowanych nowotworów i gorszych wyników klinicznych. Gdy zredukowano CDK13 w liniach komórkowych raka nerki, komórki rosły wolniej i miały trudności z przechodzeniem przez cykl komórkowy, co sugeruje, że CDK13 działa jako ukryty dyrygent koordynujący zarówno wzrost, jak i przeżywalność.
Od cukru do tłuszczu: przebudowa fabryki paliwowej komórki
Ponieważ guzy jasnokomórkowe są pełne lipidów, zespół sprawdził, czy CDK13 kontroluje także wytwarzanie tłuszczu przez te komórki. Wykorzystując profilowanie ekspresji genów i barwienia tłuszczu w mikroskopie, wykazano, że zwiększenie poziomu CDK13 powoduje narastanie kropli lipidowych w komórkach nowotworowych, podczas gdy redukcja CDK13 wywołuje efekt odwrotny. CDK13 silnie wpływał na enzym ACLY, który przekształca powszechny metabolit w acetyl-CoA — substrat wyjściowy do syntezy kwasów tłuszczowych i cholesterolu. Wysoki poziom CDK13 współwystępował z wysokim ACLY w guzach pacjentów, a oba białka koncentrowały się w tych samych obszarach tkanki nowotworowej. Sztuczne zwiększenie ACLY naprawiało wiele zaburzeń wzrostu i magazynowania tłuszczu spowodowanych utratą CDK13, lokując ACLY jako kluczowy efektor tego szlaku. 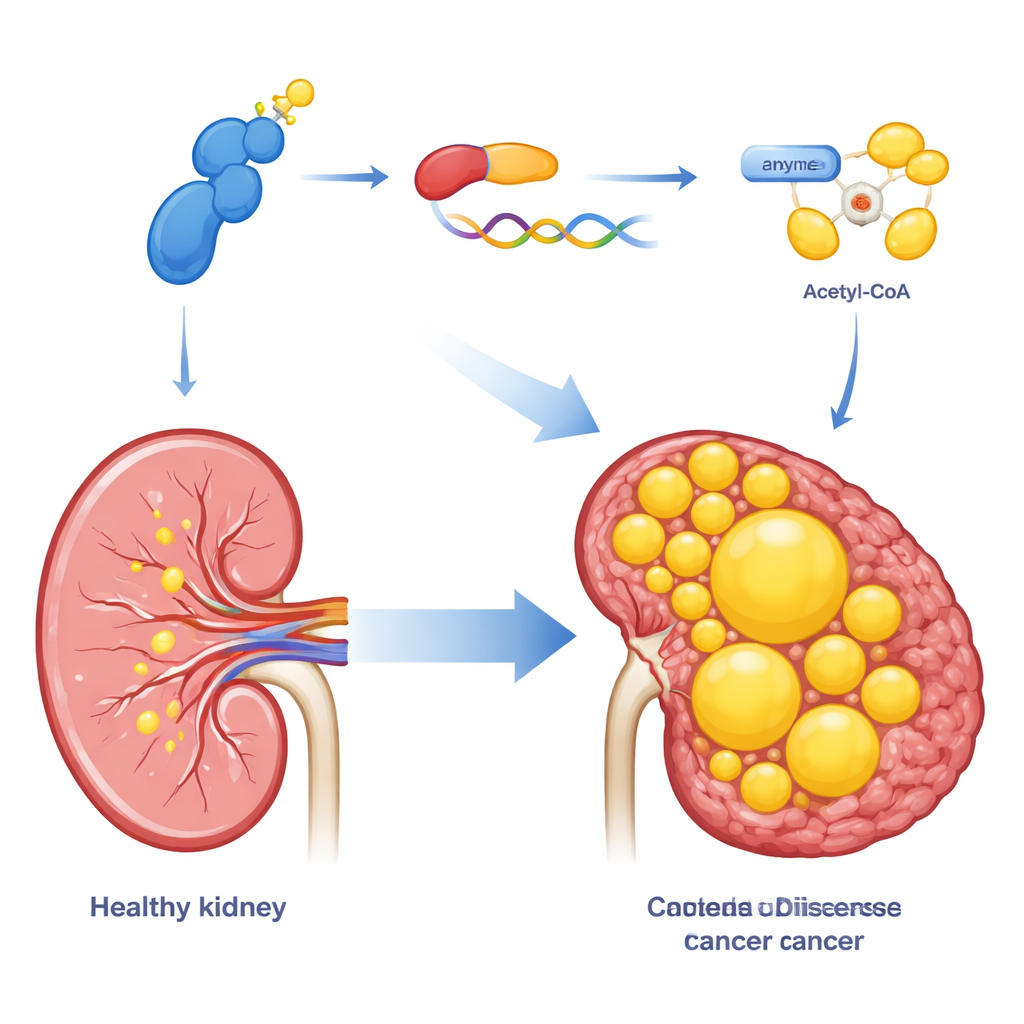
Wielowarstwowy system komunikacji w komórkach nowotworowych
Zamiast działać bezpośrednio na ACLY jak prosty włącznik, CDK13 wywiera wpływ przez wielowarstwowy system oparty na RNA — cząsteczce przenoszącej instrukcje genetyczne od DNA do maszynerii białkowej. Autorzy odkryli, że CDK13 fizycznie wiąże się z innym enzymem, METTL16, i chemicznie go modyfikuje; METTL16 nanosi drobne chemiczne znaczki (grupy metylowe) na wybrane wiadomości RNA. CDK13 przyłącza fosforową etykietę do METTL16 w precyzyjnym miejscu, czyniąc METTL16 bardziej aktywnym. METTL16 z kolei dodaje dodatkowe znaki metylowe na matrycowy RNA ACLY. Znaki te nie zmieniają kodu genetycznego, ale modyfikują sposób, w jaki komórka traktuje tę wiadomość. Trzecie białko, YTHDC2, rozpoznaje zmodyfikowany RNA ACLY i chroni go przed rozkładem, umożliwiając dłuższe powstawanie białka ACLY. Ta kaskada — CDK13 aktywujący METTL16, METTL16 znakujący RNA ACLY i YTHDC2 strzegący tej oznaczonej wiadomości — tworzy silny napęd do syntezy tłuszczów. 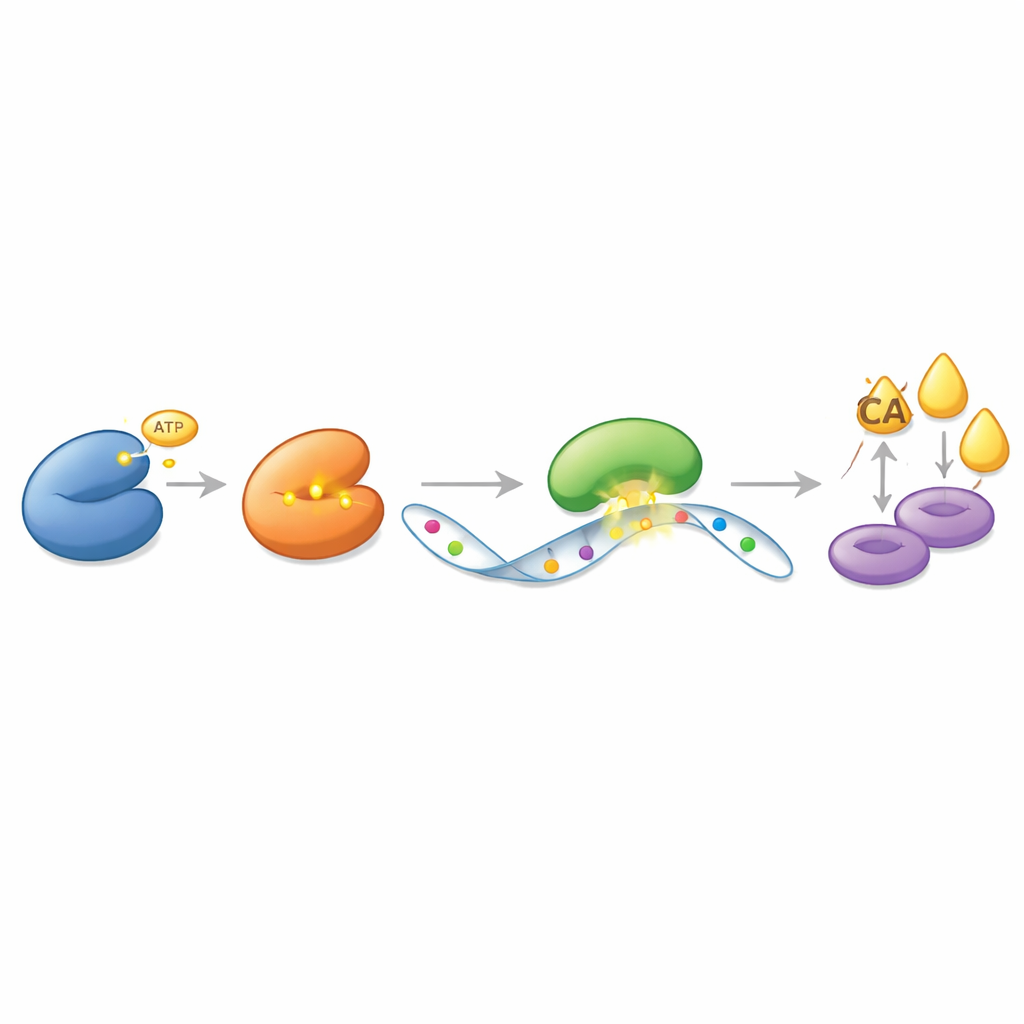
Testowanie łańcucha w komórkach, myszach i próbkach pacjentów
Siła pracy polega na tym, jak gruntownie autorzy sprawdzili ten ciąg zdarzeń. W hodowlach komórek raka nerki zakłócenie dowolnego ogniwa osi CDK13–METTL16–ACLY zmniejszało liczbę kropli lipidowych i spowalniało proliferację. U myszy wszczepionych ludzkimi komórkami raka nerki blokada CDK13 lub ACLY osobno zmniejszała guzy i redukowała zasoby tłuszczu w ich obrębie, podczas gdy jednoczesne zablokowanie obu miało jeszcze silniejszy efekt. Zespół użył także małocząsteczkowego związku, 1NM-PP1, który hamuje aktywność CDK13. Ten związek podobny do leku zmniejszył aktywującą etykietę na METTL16, obniżył poziomy ACLY i zahamował wzrost guza, szczególnie w połączeniu z deplecją METTL16. W analizach zbiorów danych pacjentów CDK13, METTL16 i ACLY miały tendencję do jednoczesnych wzrostów i spadków, co wzmacnia przekonanie, że oś ta jest aktywna w rzeczywistych nowotworach, nie tylko w modelach laboratoryjnych.
Co to może znaczyć dla przyszłych terapii
Dla czytelników niebędących specjalistami kluczowy wniosek jest taki: badanie ujawnia nowy element kontroli „fabryki tłuszczu” w guzach jasnokomórkowych nerki. Zamiast atakować jedynie enzymy wytwarzające lipidy, naukowcy opisują wyższy poziom dowodzenia, który stabilizuje instrukcje dla tych enzymów. Przerwanie osi CDK13–METTL16–ACLY może umożliwić pozbawienie guzów tłuszczów niezbędnych do wzrostu i przerzutów, przy jednoczesnym mniejszym wpływie na komórki normalne. Choć prace są nadal przedkliniczne, a 1NM-PP1 nie jest jeszcze lekiem na raka nerki, ustalenia te wskazują nowe strategie łączące inhibitory kinaz z lekami celującymi enzymy modyfikujące RNA, oferując bardziej precyzyjne podejście do leczenia tej metabolicznie napędzanej postaci raka nerki.
Cytowanie: Chen, J., Liu, H., Zhang, Y. et al. CDK13 drives clear cell renal carcinoma through METTL16-mediated m6A modification of ACLY mRNA. Exp Mol Med 58, 472–486 (2026). https://doi.org/10.1038/s12276-025-01634-7
Słowa kluczowe: rak jasnokomórkowy nerki, metabolizm lipidów, CDK13, modyfikacja RNA (metylacja), ACLY