Clear Sky Science · pl
Interferon regulatory factor 5 bierze udział w patogenezie rozedmy poprzez komórki wyrażające NLRP3 i Ly6C
Dlaczego to badanie nad płucami ma znaczenie
Przewlekła obturacyjna choroba płuc (POChP) i rozedma odbierają oddech milionom ludzi, często długo po zaprzestaniu palenia. Obecne leki mogą pomóc rozszerzyć drogi oddechowe, ale niewiele robią, by uciszyć tliwą się przewlekłą zapalność, która nadal niszczy płuca. To badanie identyfikuje molekularnego „organizatora” tego uszkodzenia, sugerując nowy sposób ochrony delikatnych pęcherzyków płucnych i spowalniania spadku funkcji płuc.
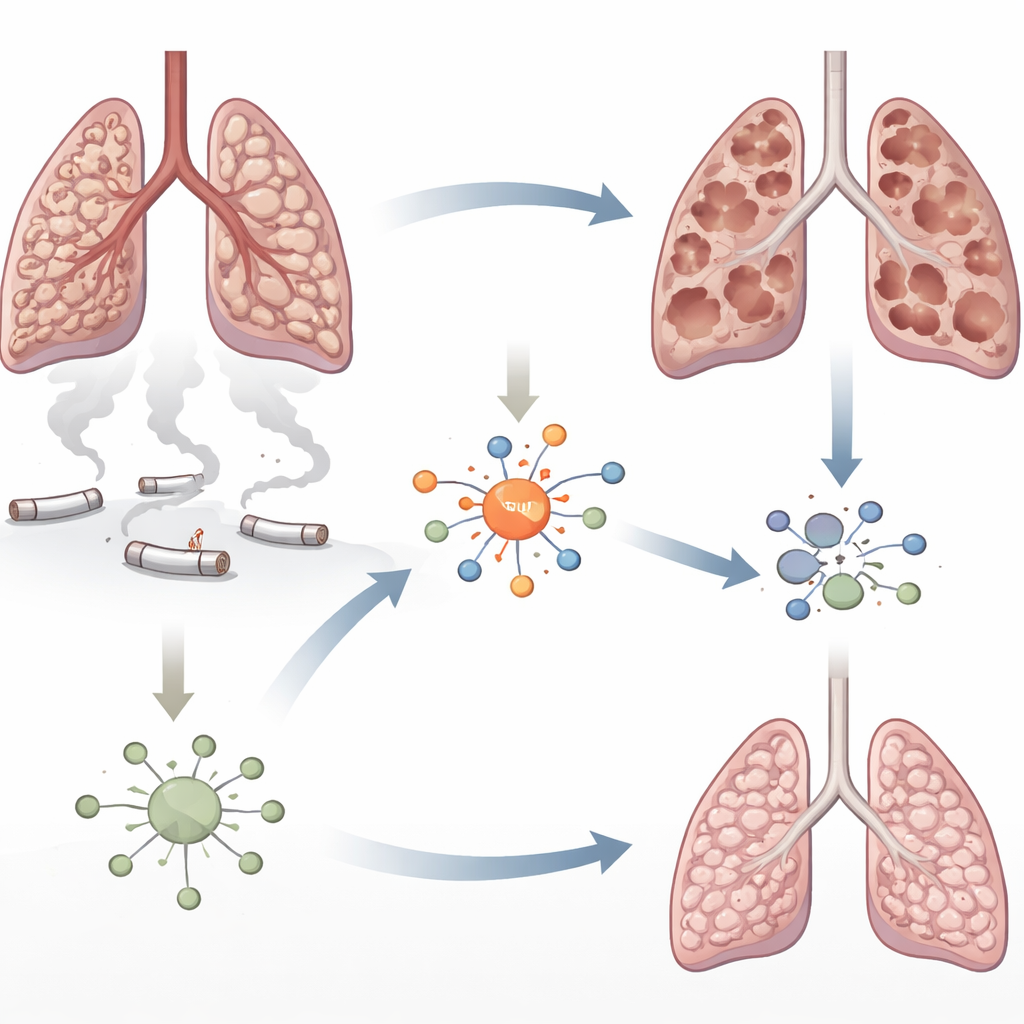
Bliższe spojrzenie na płuca uszkodzone dymem
Rozedma charakteryzuje się stopniowym rozpadem drobnych pęcherzyków, w których zachodzi wymiana tlenu i dwutlenku węgla. Dym papierosowy kąpie płuca w toksycznych cząstkach, które uszkadzają komórki i przyciągają fale komórek odpornościowych. Autorzy skupili się na białku zwanym interferon regulatory factor 5 (IRF5), znanym z wywoływania zapalenia w chorobach autoimmunologicznych, ale słabiej zbadanym w POChP. Wcześniejsze prace sugerowały, że poziomy IRF5 rosną w płucach wystawionych na działanie dymu. W tym badaniu naukowcy postanowili sprawdzić, czy IRF5 jedynie towarzyszy zapaleniu, czy rzeczywiście przyczynia się do niszczenia tkanki płucnej.
Wyłączenie kluczowego przełącznika u myszy
Aby zbadać rolę IRF5, zespół zmodyfikował myszy tak, by całkowicie pozbawić je genu kodującego to białko. Następnie eksponowali normalne i pozbawione IRF5 zwierzęta na dym papierosowy przez kilka tygodni i porównali stan ich płuc. U myszy kontrolnych dym wywołał wyraźne objawy rozedmy: ściany między sąsiednimi pęcherzykami ulegały zanikowi, pozostawiając duże, nadmiernie rozdęte przestrzenie. Natomiast myszy bez IRF5 były w dużej mierze chronione przed tym uszkodzeniem strukturalnym, mimo że dym nadal przyciągał komórki odpornościowe do przestrzeni powietrznych i zwiększał wiele cząsteczek zapalnych. Wskazywało to na IRF5 jako istotne ogniwo łączące ekspozycję na dym z faktycznym niszczeniem architektury płuc.
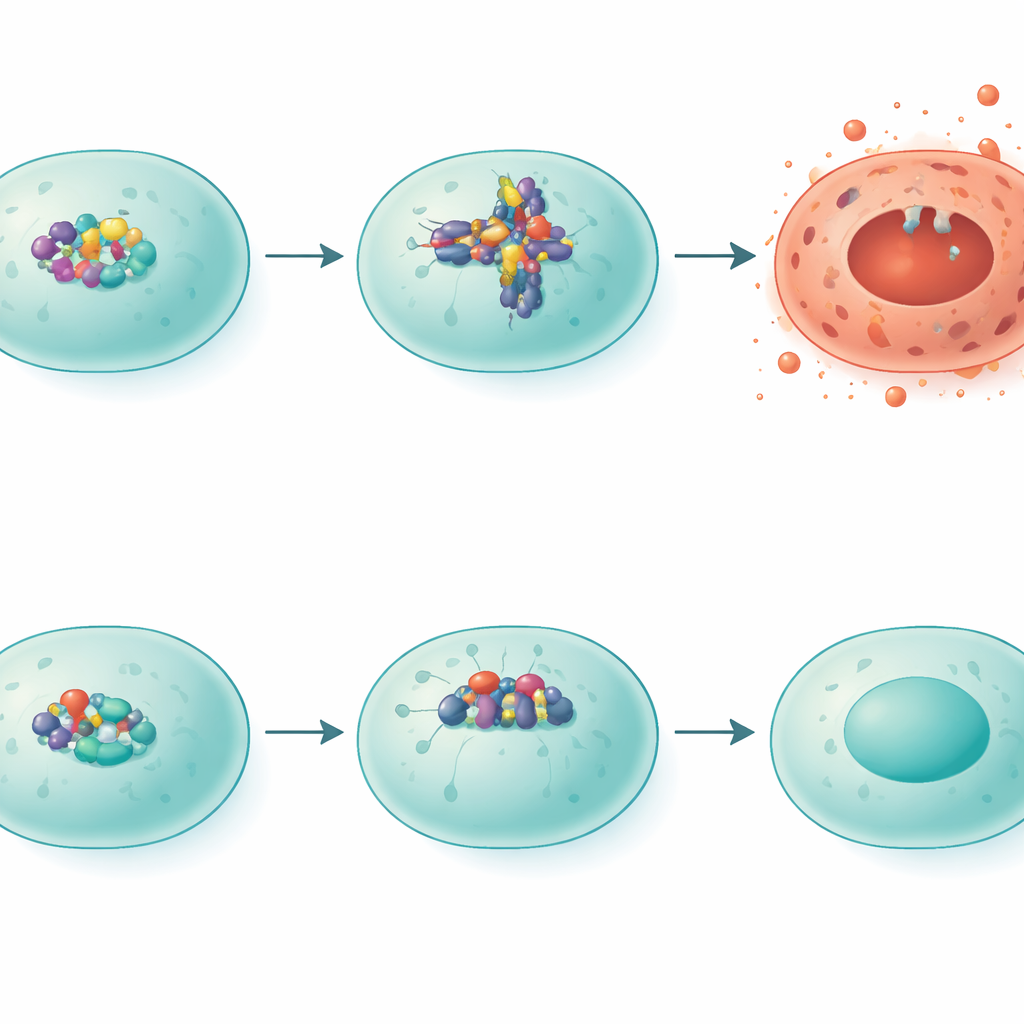
Jak IRF5 popycha komórki ku gwałtownej śmierci
Naukowcy przyjrzeli się następnie szczególnej formie gwałtownej śmierci komórkowej zwanej pyroptoza, która tworzy dziury w błonach komórkowych i uwalnia zapalne treści do otaczającej tkanki. W centrum tego procesu znajduje się kompleks białkowy znany jako NLRP3. U myszy wystawionych na dym poziomy NLRP3 wzrosły, a wzory innego białka, gasderminy D, odpowiadały stanowi podobnemu do pyroptozy. U myszy pozbawionych IRF5 poziomy NLRP3 były znacznie niższe, a gasdermina D była rozcinana na alternatywne formy związane z mniej destrukcyjnymi konsekwencjami. Kiedy zespół sztucznie zwiększył ekspresję IRF5 w komórkach związanych z płucami w warunkach laboratoryjnych, poziomy NLRP3 wzrosły, potwierdzając, że IRF5 działa jako przełącznik transkrypcyjny włączający tę szkodliwą ścieżkę.
Do obrazu wkraczają komórki odpornościowe o działaniu ochronnym
IRF5 zmieniał też skład komórek odpornościowych w płucu. U myszy pozbawionych IRF5 zaobserwowano wyraźny wzrost podzbioru krążących komórek wyraźnie oznaczonych powierzchniowym markerem Ly6C. Te komórki Ly6C‑high obejmowały zarówno monocyty, jak i limfocyty T i pojawiały się w większej liczbie po ekspozycji na dym. Gdy naukowcy oczyszczali komórki Ly6C‑high z myszy pozbawionych IRF5 i przetaczali je do zwykłych zwierząt wystawionych na dym, biorcy rozwijali mniejsze zniszczenie pęcherzyków i wykazywali niższe poziomy NLRP3 w płucach. Dodatkowe eksperymenty wykazały, że IRF5 bezpośrednio tłumi aktywność genu Ly6C, co sugeruje, że obecność IRF5 zmniejsza liczbę tych potencjalnie ochronnych komórek lub utrudnia ich utrzymanie.
Ludzkie płuca potwierdzają sygnał
Aby sprawdzić, czy te wyniki mogą mieć znaczenie dla ludzi, autorzy przebadali tkankę płucną od pacjentów poddawanych operacji z powodu raka płuca. Porównali próbki od osób o dobrej zdolności wymiany gazowej z próbkami od pacjentów z istotną rozedmą. Poziomy białka IRF5 były znacząco wyższe w płucach grupy z rozedmą. Choć badanie nie było na tyle duże, by precyzyjnie powiązać IRF5 z ciężkością objawów czy zaostrzeniami, wzorzec odpowiadał obserwacjom u myszy: więcej IRF5 w płucach chorych, mniej w zdrowszych.
Co to może oznaczać dla przyszłych terapii
Podsumowując, praca wskazuje IRF5 jako centralnego koordynatora uszkodzeń płuc wywoływanych dymem. Wzmacnia on silnik śmierci komórkowej skupiony wokół NLRP3 i odsuwa układ odpornościowy od populacji Ly6C‑high, które zdają się pomagać w zachowaniu struktury pęcherzyków. Dla pacjentów implikacja jest prosta: lek, który stłumi aktywność IRF5, mógłby w teorii ograniczyć najbardziej destrukcyjne formy zapalenia, nie wyłączając jednak całkowicie układu odpornościowego. Chociaż takie terapie jeszcze nie istnieją w leczeniu POChP, to badanie dostarcza wyraźnego celu molekularnego i biologicznie wiarygodnej ścieżki prowadzącej do terapii, które robią coś więcej niż tylko rozszerzają zwężone drogi oddechowe — mogłyby rzeczywiście chronić delikatną strukturę płuc.»
Cytowanie: Heo, SH., Park, S.Y., Kim, N.H. et al. Interferon regulatory factor 5 involves the pathogenesis of emphysema through NLRP3 and Ly6C expressing cells. Exp Mol Med 58, 425–435 (2026). https://doi.org/10.1038/s12276-025-01632-9
Słowa kluczowe: rozedma, POChP, zapalanie, odporność płuc, śmierć komórek