Clear Sky Science · nl
Ultrasensitieve biomarker‑detectie voor Alzheimer met nanobuis‑fotonicakristalbiosensoren
Waarom een eenvoudige bloedtest voor geheugenverlies ertoe doet
Naarmate nieuwe geneesmiddelen verschijnen die de ziekte van Alzheimer kunnen vertragen, hebben artsen dringend behoefte aan eenvoudige tests die aantonen wie risico loopt, lang voordat symptomen duidelijk worden. Vandaag de dag betekent bevestiging van Alzheimer meestal dure hersenscans of lumbaalpuncties die maar door weinigen in de routinezorg worden ondergaan. Deze studie beschrijft een klein, lichtgebaseerd sensorplatform dat sleutel‑moleculen gerelateerd aan Alzheimer kan opsporen in een druppel bloed op klinisch relevante concentraties, en daarmee mogelijk de weg vrijmaakt voor snelle, goedkope tests die in gewone klinieken of zelfs naast het bed gebruikt kunnen worden.
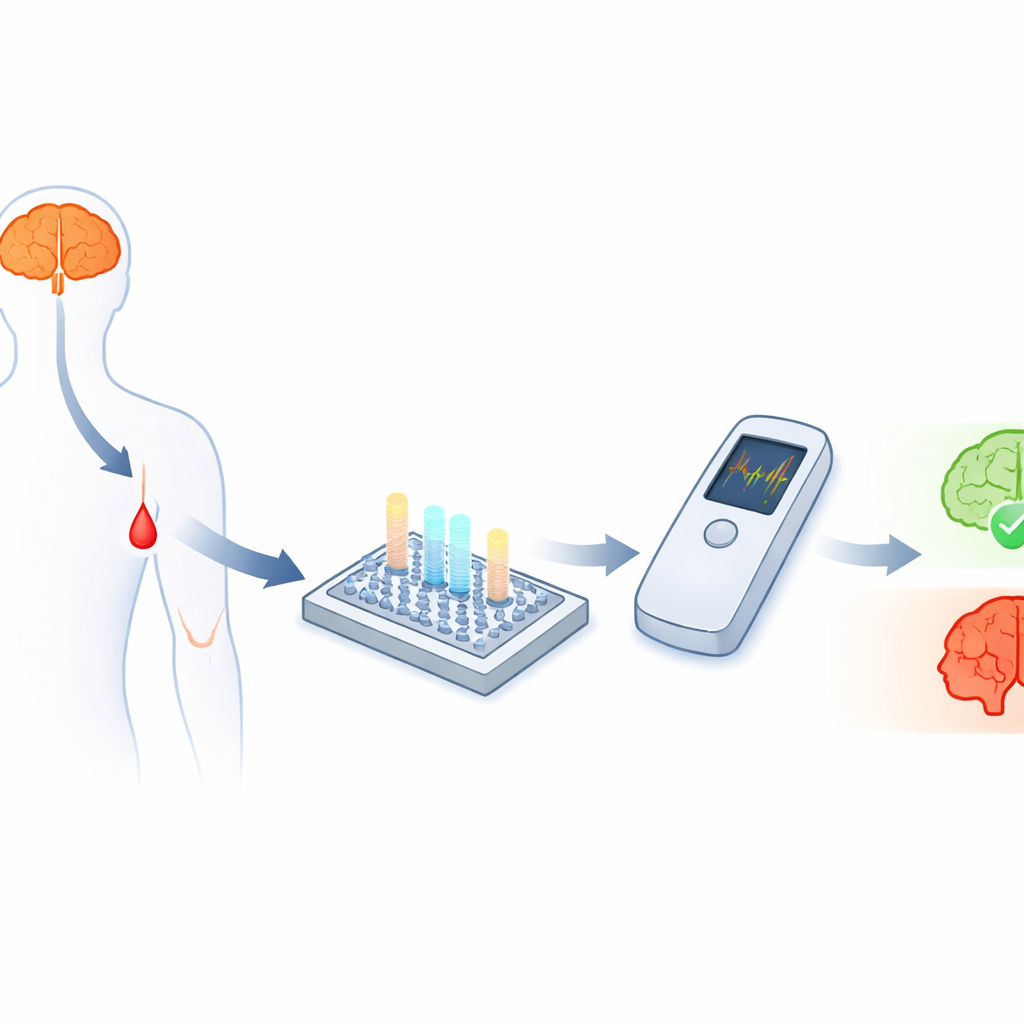
Op zoek naar aanwijzingen in het bloed
De ziekte van Alzheimer hangt nauw samen met kleine eiwitfragmenten die amyloïde‑bèta worden genoemd, met name twee vormen bekend als Aβ40 en Aβ42. Hun hoeveelheden, en vooral hun verhouding, bevatten belangrijke aanwijzingen over de aanwezigheid van de ziekte en de voortgang ervan. De uitdaging is dat deze fragmenten extreem klein zijn en in het bloed circuleren op zeer lage concentraties — biljoenensten van een gram per milliliter — wat ze buiten gespecialiseerde laboratoria moeilijk nauwkeurig meetbaar maakt. Hoewel elektrochemische sensoren in principe zulke lage concentraties kunnen detecteren, blijkt het moeilijk om ze om te zetten in robuuste, betaalbare point‑of‑care‑tests die meerdere biomarkers tegelijk kunnen volgen.
Licht geleiden door piepkleine zuiltjes
Het team pakte deze uitdaging aan met nanofotonica — structuren die licht beheersen op een schaal kleiner dan de golflengte van dat licht. Zij bouwden een chip bedekt met een regelmatig raster van gepaarde, haar‑dunne siliciumzuiltjes op glas. Wanneer licht op dit geordende oppervlak valt, raakt het gevangen in een speciale resonantiemode die bijzonder gevoelig is voor veranderingen nabij de bovenkanten van de zuiltjes, vergelijkbaar met hoe de toon van een stemvork verschuift als er materiaal aan wordt toegevoegd. Door zorgvuldig de afstand tussen de zuiltjes in elk paar af te stemmen, brachten de onderzoekers drie cruciale eigenschappen in balans: hoe scherp de optische resonantie is, hoe sterk deze verandert met de omgeving, en hoe groot het geproduceerde signaal is. Dit ‘sweet spot’‑ontwerp maakt de chip bijzonder geschikt om zeer kleine hoeveelheden materiaal te detecteren.
Onzichtbare moleculen zichtbaar maken
Zelfs met dit geoptimaliseerde ontwerp zouden de Alzheimer‑markers op zichzelf nauwelijks effect op het licht hebben. Om het effect te versterken, gebruikten de onderzoekers een sandwich‑strategie met gouden nanodeeltjes. Eerst bedekten ze het sensorsurface met lagen kleverige chemie die gespecialiseerde antilichamen correct oriënteert, zodat hun bindingsplaatsen de vloeistof in wijzen. Deze antilichamen vangen uit het monster óf Aβ40 óf Aβ42. Vervolgens worden gouden nanodeeltjes, elk bekleed met een tweede antilichaam dat een ander uiteinde van hetzelfde amyloïdefragment herkent, over de chip gevoerd. Wanneer een amyloïdefragment aanwezig is, vormt het een brug tussen het oppervlak en een gouddeeltje, waardoor het effectief wordt ‘gevlagd’. Omdat goud het lokale optische milieu sterk verstoort, veroorzaakt elk gevangen fragment een veel grotere verschuiving in de resonantie van de sensor dan het peptide alleen, wat de gevoeligheid met ongeveer één tot twee orde van grootte verhoogt terwijl het optische signaal schoon blijft.
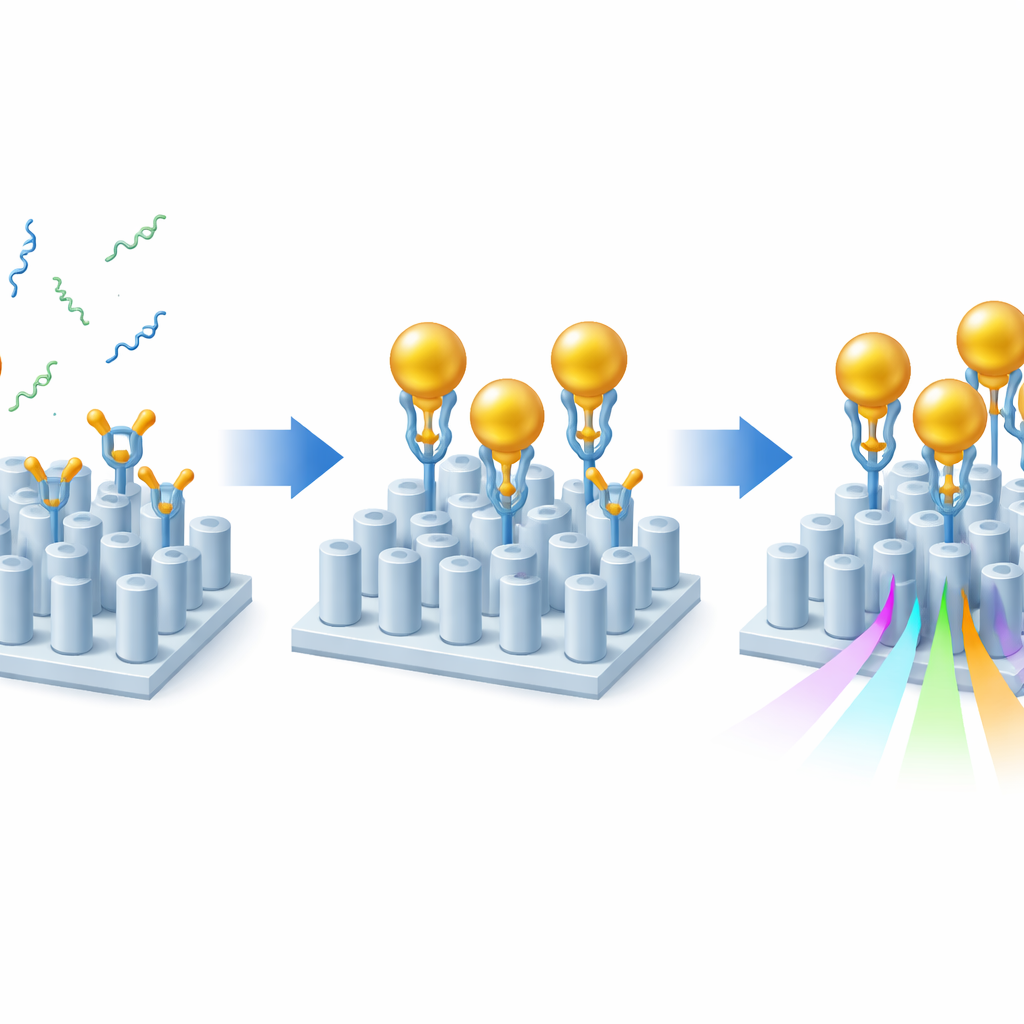
Realistische monsters testen
Om aan te tonen dat de methode werkt buiten eenvoudige laboratoriumbuffers, testte het team hun sensor met menselijk bloedserum. Ze verdunden serum zodat het compatibel was met microfluidische verwerking, maar behielden de amyloïde‑niveaus representatief voor die in patiënten. Belangrijk is dat ze zowel Aβ40 als Aβ42 konden detecteren op 0,2 picogram per milliliter in dit verdunde serum — wat overeenkomt met het klinisch relevante niveau van 20 picogram per milliliter in volledig bloed. Door verschillende capture‑antilichamen in aparte regio’s op dezelfde chip te plaatsen, maten ze beide vormen van amyloïde gelijktijdig binnen één enkele kleine kanaal, een belangrijke stap richting het bepalen van hun verhouding uit één klein monster. De signalen onderscheidden duidelijk monsters die extra amyloïde waren toegediend van monsters die alleen de natuurlijk voorkomende achtergrondniveaus bevatten die zelfs bij gezonde personen worden gevonden.
Wat dit kan betekenen voor toekomstige zorg
Samengevat tonen deze vorderingen aan dat een compact, lichtgebaseerd sensorplatform, versterkt door gouden nanodeeltjes, de sensitiviteiten kan bereiken die nodig zijn voor zinvolle Alzheimer‑bloedtesten, terwijl het meerdere biomarkers tegelijk kan verwerken. Hoewel aanvullend werk nodig is om dit om te zetten in een robuust commercieel apparaat en om andere markers zoals vormen van het tau‑eiwit toe te voegen, is de onderliggende technologie opgebouwd uit schaalbare materialen en kan ze worden gekoppeld aan eenvoudige, handzame optiek. Als het volledig wordt ontwikkeld, zou het clinici in staat kunnen stellen de hersengezondheid te monitoren met slechts een kleine bloedafname, waardoor het veel gemakkelijker wordt om Alzheimer vroeg te detecteren en te volgen hoe goed behandelingen in de loop van de tijd werken.
Bronvermelding: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Trefwoorden: Alzheimer‑bloedtest, nanofotonische biosensor, amyloïde bèta, gouden nanodeeltjes, vroegtijdige diagnose