Clear Sky Science · nl
Selectieve tumorafschaffing via femtosecondenlaser resonant met collageen
Licht omzetten in een gericht kankerinstrument
Pancreaskanker behoort tot de dodelijkste vormen van kanker, deels omdat het moeilijk is de tumor te verwijderen zonder het kwetsbare omliggende orgaan te beschadigen. Deze studie onderzoekt een nieuwe manier om ultrakorte pulsen van onzichtbaar infrarood licht te gebruiken om pancreastumoren preciezer weg te branden door zich te richten op een structureel bestanddeel dat in tumoren in overmaat aanwezig is. Het werk suggereert toekomstige behandelingen die meer gezond weefsel kunnen sparen terwijl ze toch hard toekomen aan de kanker.
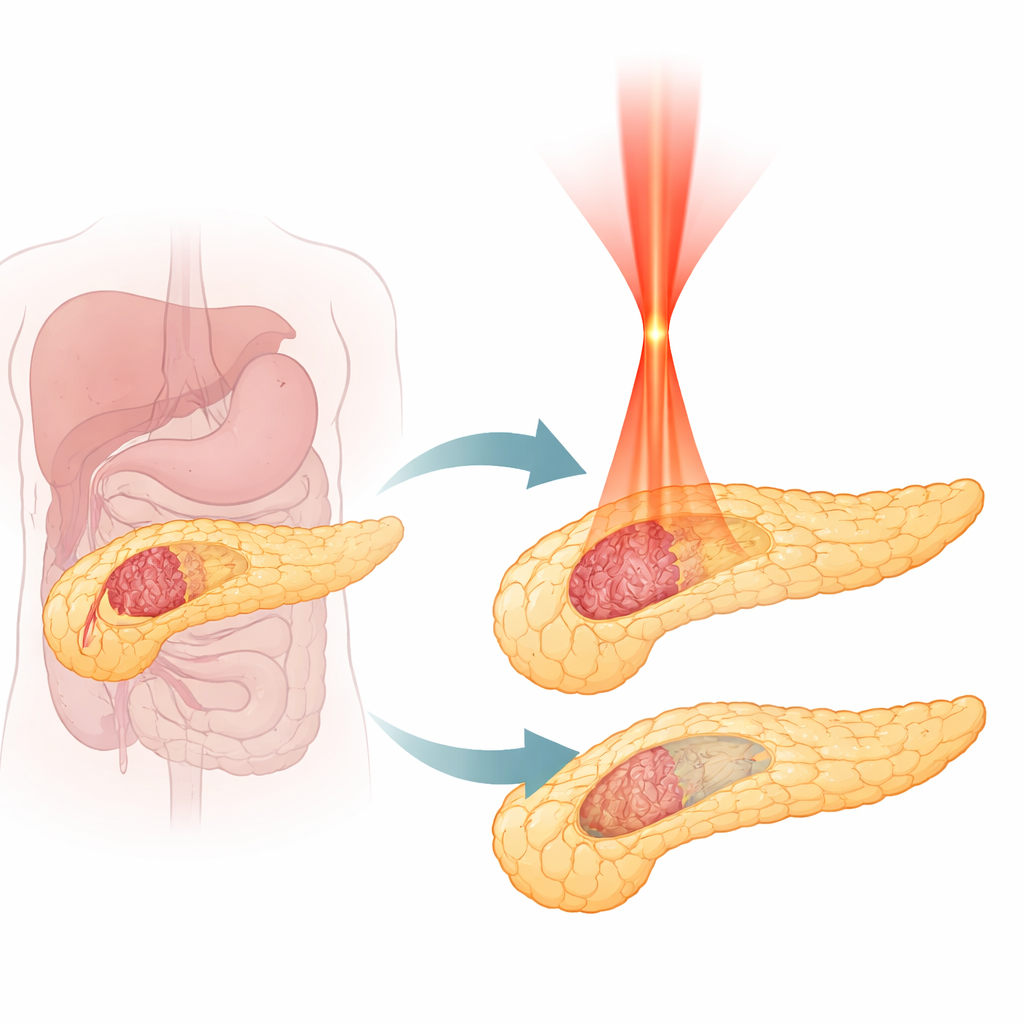
Waarom pancreastumoren zo moeilijk te behandelen zijn
Pancreatische ductale adenocarcinoom, de meest voorkomende vorm van pancreaskanker, groeit agressief en wordt vaak laat ontdekt. Slechts een klein deel van de patiënten komt in aanmerking voor chirurgie, en zelfs moderne chemo- en bestralingstherapieën bieden beperkte voordelen. Warmtegebaseerde behandelingen die weefsel vernietigen, zoals radiofrequentie-, microgolf- of standaard laserablaties, kunnen tumoren verkleinen, maar ze verbranden vaak alles op hun pad. Omdat de alvleesklier dicht bij vitale bloedvaten en kwetsbare spijsverteringsstructuren ligt, brengt het vergroten van het behandelingsgebied het risico op ernstige complicaties met zich mee. Artsen hebben daarom een methode nodig die tijdens het vernietigen onderscheid kan maken tussen tumor en normaal pancreas, in plaats van simpelweg een breed gebied te garen.
Een verborgen zwakke plek in tumorweefsel vinden
De auteurs concentreerden zich op een belangrijk fysisch verschil tussen pancreastumoren en gezond pancreas: tumoren zitten vol stijf, vezelig materiaal dat rijk is aan collageen, terwijl gezond weefsel zachter en losser is. Met standaard weefselkleuringen en elektronenmicroscopie van operatief verkregen monsters toonden ze aan dat kankergezwellen dichte bundels collageenvezels bevatten, terwijl het nabijgelegen gezonde pancreas veel minder bevat. Vervolgens gebruikten ze infraroodspectroscopie om te meten hoe sterk deze weefsels verschillende golflengten van midden-infrarood licht absorberen. Beide weefsels absorberen bij vergelijkbare golflengten, maar tumoren vertonen een veel sterkere piek nabij een golflengte van 6,1 micrometer, wat overeenkomt met trillingen van collageen. Dat suggereerde dat een laser precies op die golflengte afgestemd tumorweefsel efficiënter zou kunnen verwarmen en afbreken dan normaal pancreas.
Een laser bouwen die naar collageen luistert
Om dit idee te testen bouwde het team een krachtige midden-infraroodlaser die ultrakorte pulsen uitzendt — van slechts enkele honderden biljardsten van een seconde — gecentreerd op 6,1 micrometer. Deze “femtoseconde”-pulsen beperken ongewenste warmteverspreiding, vergelijkbaar met een reeks kleine, gecontroleerde blikseminslagen. Het systeem zet licht van een hoogvermogen industriele laser om naar de gewenste golflengte met behulp van speciale kristallen en kan meer dan één watt gemiddelde vermogen leveren; dat is voldoende voor praktische weefselablaties. De onderzoekers ontwikkelden ook een holle vezel van glas die dit licht langs een flexibele baan kan geleiden, een belangrijke stap richting het doorvoeren van de laser door een dunne naald in het lichaam voor minimaal invasieve procedures.
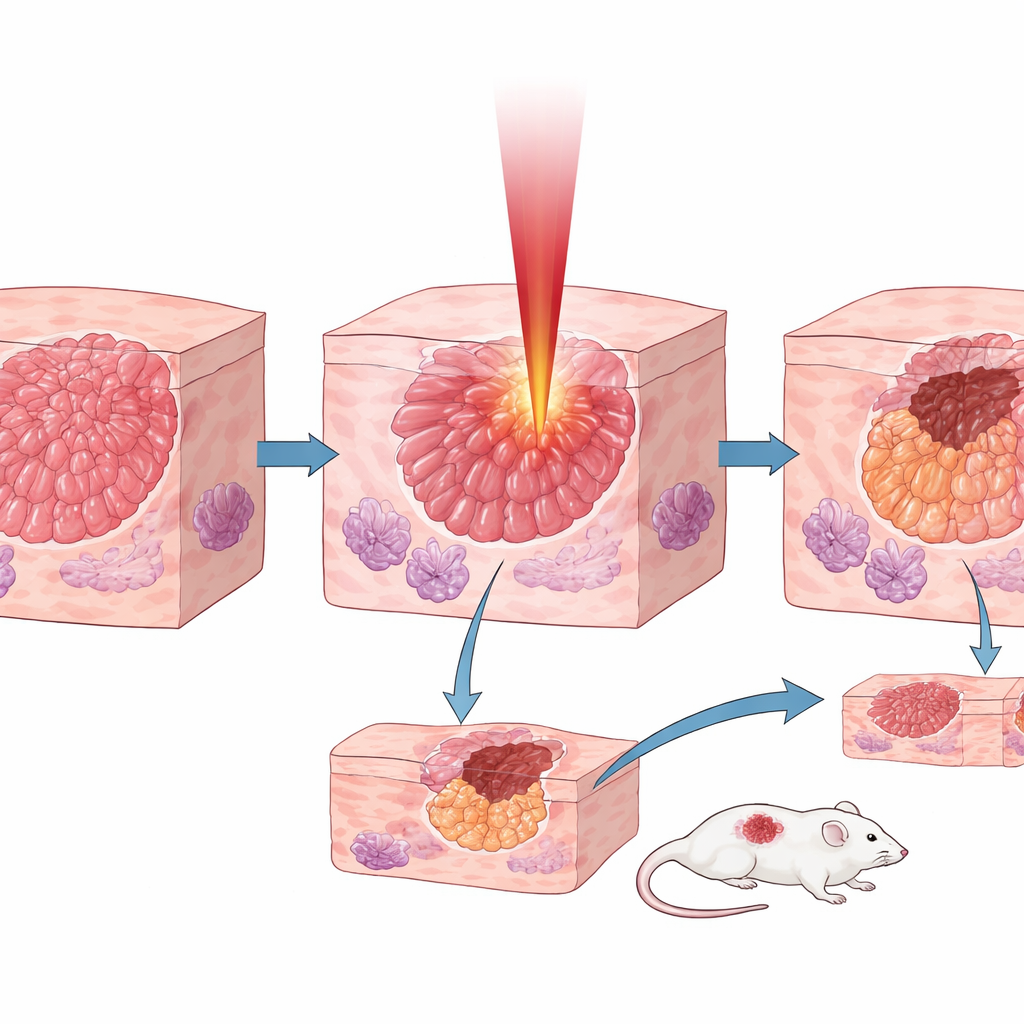
Selectiviteit testen in cellen, muizen en menselijk weefsel
In kweekceltests met twee pancreaskankerlijnen was de 6,1-micrometerlaser veel dodelijker dan lasers bij 1 of 3 micrometer, en verminderde sterk de overleving van cellen binnen seconden tot minuten na blootstelling. In muismodellen met onderhuids geplaatste pancreastumoren werden drie verschillende golflengten vergeleken. Hoewel de 1-micrometerstraal veel meer vermogen droeg, verwijderde deze slechts ondiepe lagen tumor. De op collageen afgestemde 6,1-micrometerlaser bereikte ablatie-dieptes vijf tot tien keer groter en vertraagde de tumorgroei zo sterk dat behandelde tumoren uiteindelijk ongeveer een achtste van de grootte hadden van die in onbehandelde dieren. Het belangrijkste: toen het team de 6,1-micrometerlaser op menselijke tumormonsters en aangrenzend normaal pancreas toepaste, waren de insnijdingen in tumor twee- tot driemaal dieper dan in gezond weefsel onder dezelfde omstandigheden, wat echte selectiviteit aantoonde. Ter vergelijking: bij een andere levertumor die geen extra collageen ophoopt, verdween het voordeel grotendeels, wat de centrale rol van collageen versterkt. Tot slot toonden ze aan dat de holle vezel hetzelfde selectieve effect kan leveren, wat needle-based behandelingen in de toekomst ondersteunt.
Wat dit kan betekenen voor toekomstige kankerzorg
De studie laat zien dat zorgvuldig afgestemde bursts van midden-infrarood licht een materiaalkenmerk tussen tumoren en gezond weefsel kunnen benutten om meer selectieve vernietiging te bereiken. Door collageenrijke gebieden te targeten, snijdt de 6,1-micrometer femtosecondenlaser dieper in pancreaskanker terwijl meer van het omliggende orgaan gespaard blijft. Hoewel het werk nog experimenteel is en meer tests in realistische modellen en klinische settings nodig zijn, wijst het op een nieuwe klasse van beeldgestuurde, vezelgeleverde procedures die mogelijk niet alleen pancreastumoren maar ook andere collageenrijke kankers met grotere precisie en minder bijwerkingen kunnen behandelen.
Bronvermelding: Dunxiang Zhang, Xing Huang, Xuemei Yang, Ning Xia, Kan Tian, Jinmiao Guo, Maoxing Xiang, Linzhen He, Zhizhuo Fu, Ang Deng, Han Wu, Yuxi Wang, Wonkeun Chang, Bole Tian, Junjie Xiong, Qi Jie Wang, Anderson S. L. Gomes, and Houkun Liang, "Selective tumor ablation via femtosecond laser resonant with collagen," Optica 12, 1578-1586 (2025). https://doi.org/10.1364/OPTICA.561337
Trefwoorden: pancreaskanker, laserablaties, collageen, midden-infrarood, minimaal invasieve chirurgie