Clear Sky Science · nl
De oorsprong in de quaternaire structuur van de fibrillatie van sikkelhemoglobine: een moleculaire-dynamicaonderzoek
Waarom dit bloedverhaal ertoe doet
Sikkelcelziekte begint met een kleine wijziging in één bloedproteïne, maar kan toch rode bloedcellen vervormen, vaten blokkeren en levenslange pijn veroorzaken. Deze studie bekijkt, vanuit een natuurkundig perspectief, hoe die ene wijziging ertoe leidt dat het eiwit hemoglobine zich opstapelt tot stijve vezels in de cel. Met geavanceerde computersimulaties koppelen de auteurs atomaire details aan problemen op celniveau en bieden ze nieuwe aanwijzingen voor hoe toekomstige geneesmiddelen kunnen verhinderen dat hemoglobine onze bloedbaan verstopt.
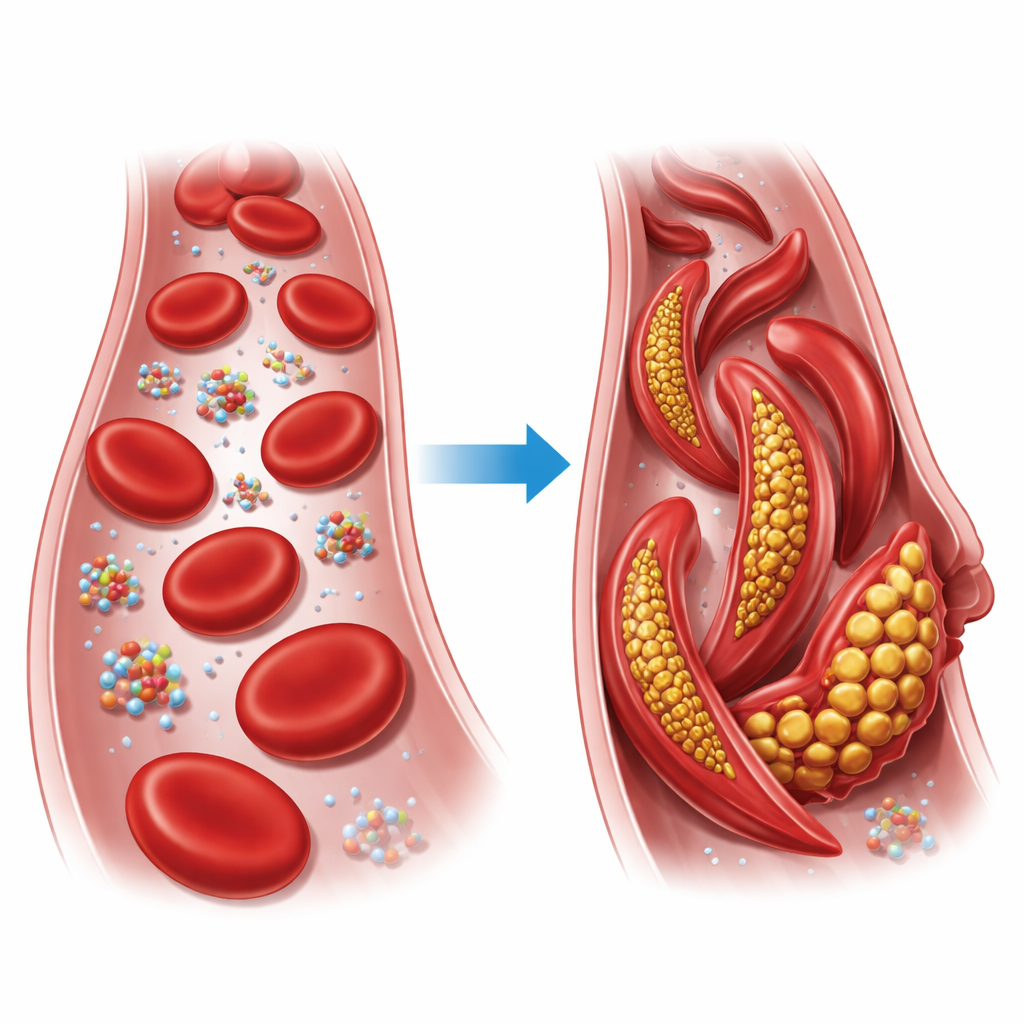
Een kleine verwisseling met grote gevolgen
Hemoglobine is het zuurstofdragende eiwit in onze rode bloedcellen. Elk hemoglobine-eenheid bestaat uit vier ketens die zich in twee hoofdvormen kunnen rangschikken, bekend als de ontspannen (R) toestand en de gespannen (T) toestand. Bij sikkelcelziekte wordt in één van die ketens slechts één bouwsteen verwisseld: een geladen glutamaat wordt op positie zes van de bèta-keten vervangen door een vettere valine. Onder lage-zuurstofomstandigheden koppelt deze veranderde vorm, sikkelhemoglobine genoemd, zich aan andere eenheden tot lange vezels die normaal ronde rode bloedcellen vervormen tot stijve, sikkelachtige vormen, waardoor kleine vaten kunnen stoppen en weefsels van zuurstof worden verstoken.
Het volgen van de veranderende vorm van hemoglobine
De auteurs richten zich op hoe hele hemoglobine-eenheden roteren en zich in een vezel inpaken. Ze volgen deze grootschalige vormverandering met één enkele hoek die meet hoe twee helften van het eiwit ten opzichte van elkaar draaien. Met moleculaire-dynamicasimulaties — virtuele experimenten die berekenen hoe atomen zich in de tijd bewegen in water en zout — duwen ze deze hoek langzaam over een breed bereik en berekenen ze hoeveel energie elke vorm kost. Ze vinden dat zowel normaal als sikkelhemoglobine bij lichaamstemperatuur veel van zulke vormen kunnen verkennen. Sikkelhemoglobine toont een licht voorkeurshoek, maar deze vormvoorkeuren alleen verklaren niet waarom alleen de sikkelvorm stabiele vezels vormt.
Waarom sikkelvezels blijven plakken en normale uiteenvallen
Om het hart van de vezelvorming te doorgronden, meet de studie hoe sterk aangrenzende hemoglobine-eenheden elkaar aantrekken langs en dwars op de vezel. Het team berekent de cohesieve energie — de netto aantrekkingskracht die de eenheden bij elkaar houdt — voor vele verschillende algehele vormen. Bij sikkelhemoglobine blijft deze cohesieve energie over het volledige bereik dat ze onderzochten negatief (dus aantrekkelijk), zodat vezels stabiel blijven en niet snel uiteen vallen. Bij normaal hemoglobine daarentegen hebben sommige hoeken juist een positieve cohesieve energie, waardoor vezels bij die hoeken onstabiel zijn en spontaan kunnen breken. Een cruciaal verschil is hoe de gemuteerde valine-zijgroepen in aangrenzende eiwitten passen: bij sikkelhemoglobine vormen deze vette plekjes robuuste contacten zowel zijwaarts als langs de vezelas, en bevorderen ze direct de groei van de vezel.
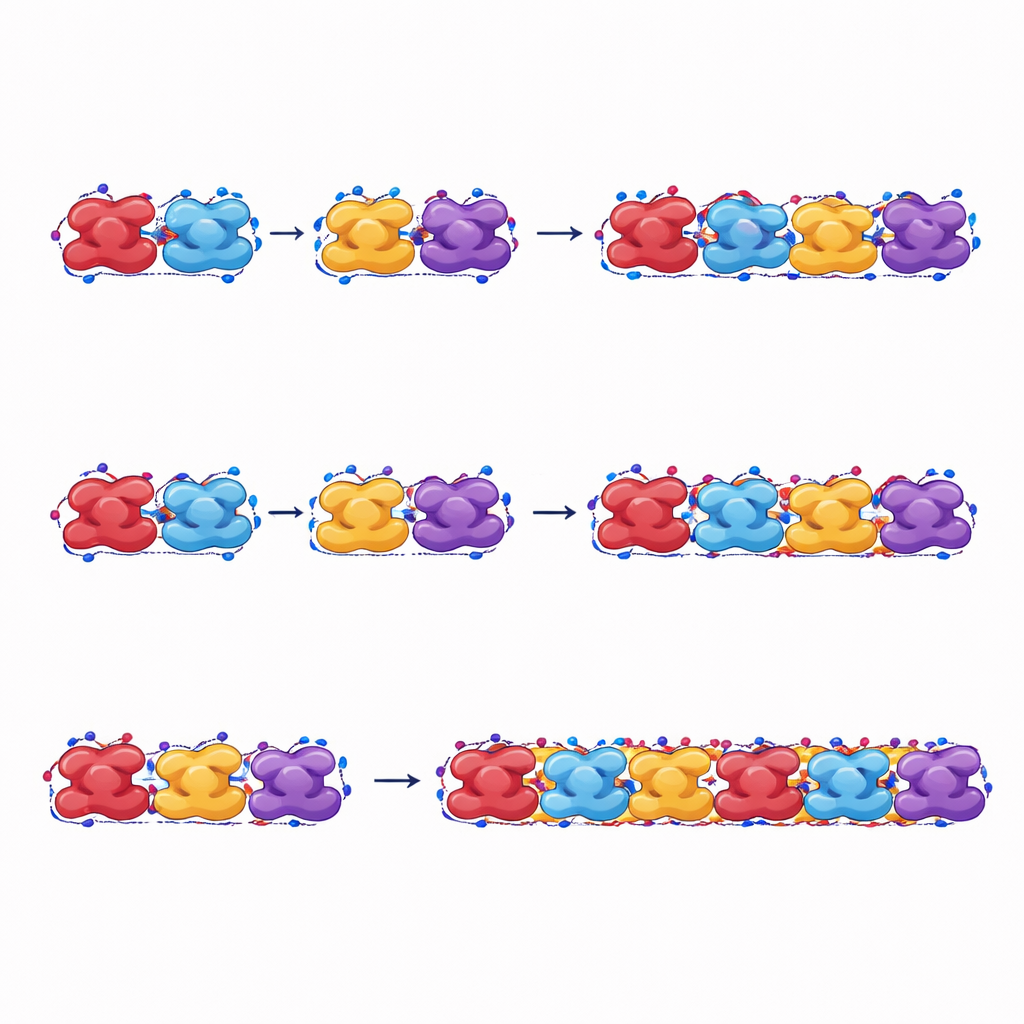
Hoe deze vezels belasting dragen en breken
De auteurs rekken hun gesimuleerde vezels ook uit om mechanische spanningen na te bootsen. Wanneer ze in de lengte worden uitgetrokken, verdragen vezels van sikkelhemoglobine hogere krachten en vervormingen en dissiperen ze meer energie voordat ze breken dan vezels van normaal hemoglobine. Zelfs de ontspannen vorm van sikkelvezels, die niet de vorm is waarin vezels eerst ontstaan, kan de ketting door plastische vormveranderingen alsnog behouden, waardoor de vezel intact blijft zodra deze eenmaal gevormd is. Vezels van normaal hemoglobine scheiden zich daarentegen gemakkelijker tussen aangrenzende eenheden en absorberen minder energie vóór falen, wat bevestigt dat ze minder stabiel zijn onder mechanische belasting.
Aanwijzingen voor toekomstige behandelingen en nieuwe materialen
Gezamenlijk tonen de simulaties dat één aminozuurwijziging de manier verandert waarop hemoglobine-eenheden elkaar ontmoeten, waardoor de algehele assemblage draait naar hoeken die sterke aantrekking bevoordelen, vooral in de gespannen toestand. Deze combinatie van geometrie en kleverigheid stelt sikkelhemoglobine in staat lange, stijve vezels te vormen die zowel thermische beweging als mechanische belasting weerstaan, en die uiteindelijk rode bloedcellen vervormen en de bloedstroom blokkeren. Door te wijzen op specifieke kenmerken van de eiwitassemblage die de vezelstabiliteit bepalen, suggereert het werk dat effectieve antisikkelmiddelen kunnen werken door hemoglobine te sturen naar vormen waarin vezels energetisch ongunstig en mechanisch kwetsbaar worden — waardoor een dodelijke moleculaire blokkade weer verandert in een vrij stromende bloedbaan.
Bronvermelding: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Trefwoorden: sikkelcelziekte, hemoglobinevezels, eiwitaggregatie, moleculaire dynamica, bloedziekten