Clear Sky Science · nl
APP E590D-mutatie verhoogt de productie van Aβ- en Aη-peptiden en verergert tauopathie
Waarom deze zeldzame mutatie ertoe doet
De ziekte van Alzheimer wordt meestal gezien als de geleidelijke ophoping van twee schadelijke eiwitten, amyloïde en tau, in de hersenen. De meeste mensen ontwikkelen Alzheimer zonder één duidelijke oorzaak, maar enkele families dragen zeldzame genetische veranderingen die het evenwicht sterk kunnen verschuiven. Dit artikel onderzoekt zo’n ongewone verandering in het gen voor het amyloïde precursor-eiwit (APP) en laat zien hoe die de productie van toxische eiwitfragmenten kan versterken en het in de hersenen verstrengelde proces dat bekendstaat als tauopathie kan verergeren. Het begrijpen van dit zeldzame geval biedt aanwijzingen die veel algemener toepasbaar kunnen zijn op hoe Alzheimer begint en vervolgens versnelt.
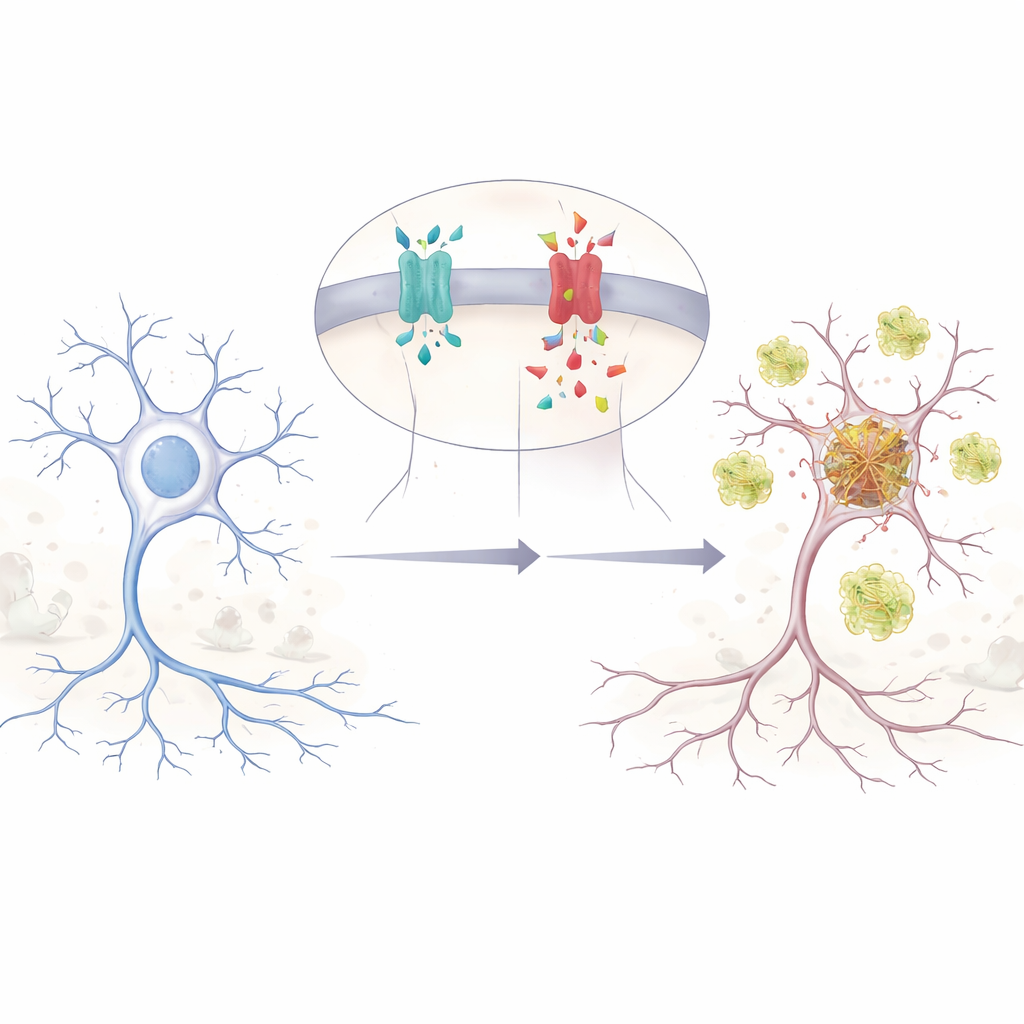
Een kleine genetische wijziging met grote gevolgen
De auteurs richten zich op een enkelletterwijziging in het APP-gen, aangeduid als E590D in de belangrijkste hersenvorm van APP. Deze mutatie is slechts bij twee mensen gerapporteerd, beide met bevestigde Alzheimer op relatief jonge leeftijd en met ongebruikelijke, zeer vroege geheugen- en gedragsproblemen. Omdat zij zo zeldzaam is, wisten wetenschappers niet zeker of ze werkelijk ziekte veroorzaakt of slechts een onschuldige bijverschijnsel is. Om dat uit te zoeken reconstrueerde het team de mutatie in menselijke cellen en in muisneuronencellen, en volgde vervolgens hoe APP in zijn vele fragmenten werd geknipt. Ze ontdekten dat het gemuteerde APP veel meer amyloïde bèta (Aβ) produceert — het kleverige peptide dat lang met Alzheimer is geassocieerd — dan normaal APP wanneer de niveaus eerlijk worden vergeleken.
Twee toxische peptiden in plaats van één
APP kan op verschillende manieren worden geknipt, zoals een stuk hout op verschillende punten wordt gezaagd. De klassieke Alzheimer-route genereert Aβ, maar een andere knip produceert een minder bekend fragment genaamd Aη. Eerder werk toonde aan dat Aη de verbindingen tussen zenuwcellen kan beschadigen en het vermogen van de hersenen om herinneringen te versterken kan verzwakken. In hun experimenten vonden de onderzoekers dat de E590D-mutatie niet alleen Aβ verhoogt; ze verhoogt ook sterk Aη en een upstream-fragment dat in beide routes voorziet. Dit betekent dat de mutatie de APP-verwerking verschuift naar een dubbele aanslag van schadelijke peptiden, wat mogelijk hersencircuits verstoort nog voordat klassieke amyloïdeplaquevorming verwacht zou worden.
Hoe de mutatie het cellulaire verkeer versnelt
Om te begrijpen waarom er meer toxische fragmenten worden gemaakt, bestudeerde het team waar APP zich bevindt en hoe het over het celoppervlak beweegt. Veel van de knippen die Aβ creëren vinden alleen plaats nadat APP via een proces dat endocytose heet in de cel is opgenomen. Met behulp van beeldvorming en biochemische trucs die eiwitten aan het oppervlak labelen en vervolgens hun internalisatie volgen, toonden de wetenschappers aan dat gemuteerd APP minder aanwezig is aan de buitenkant van cellen en sneller wordt opgenomen in interne compartimenten dan normaal APP. Eenmaal in deze vroege endosomen komt APP de enzymen tegen die Aβ genereren, en de gewijzigde trafficking lijkt die enzymen meer gelegenheid te geven om te werken. Tegelijkertijd neemt ook het knippen op de η-plaats aan het oppervlak toe, wat de toename van Aη verklaart.
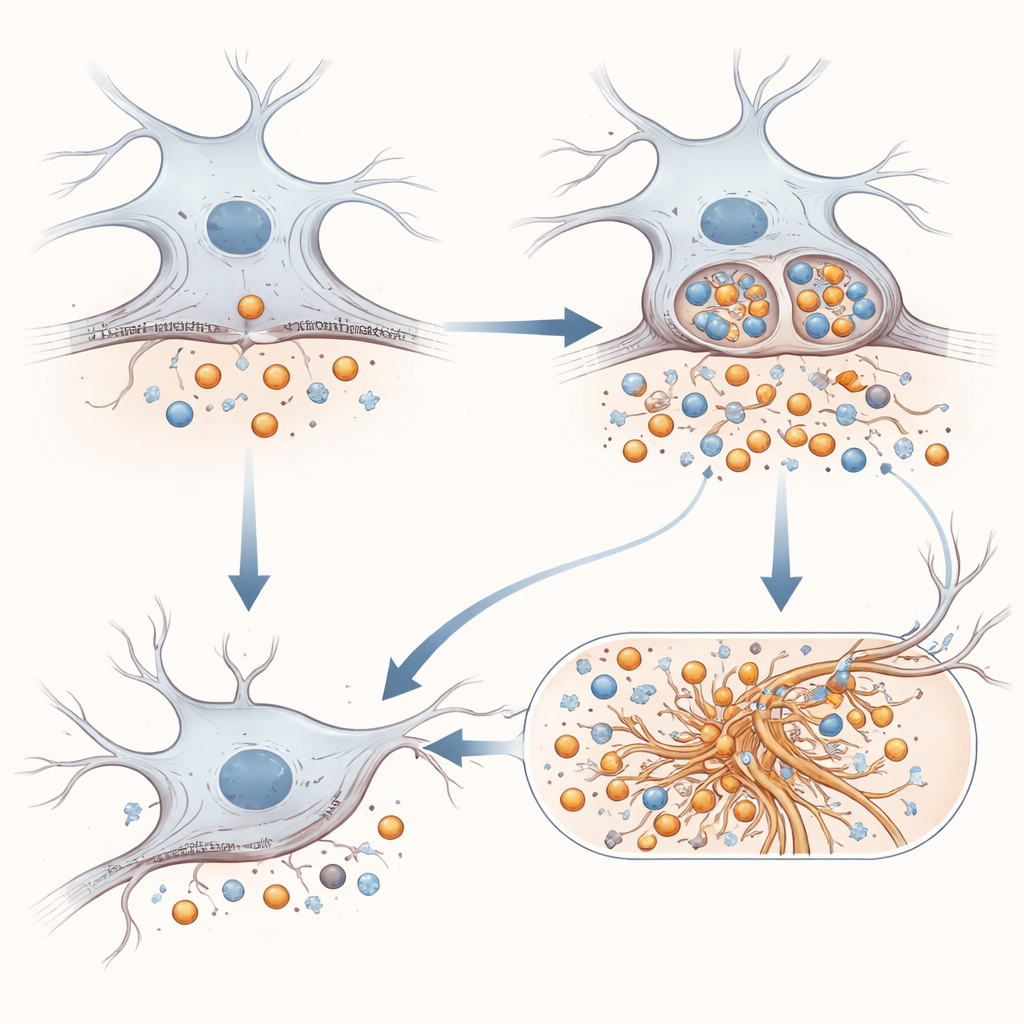
Van eiwitfragmenten naar verstrengelde tau en hersenontsteking
Het verhaal stopt niet bij amyloïde-gerelateerde fragmenten. De onderzoekers testten of gemuteerd APP invloed zou hebben op tau, het structurele eiwit dat in vele dementieën gedraaide vezels vormt. In celmodellen die oplichten wanneer tau-seeds nieuwe tau-kluwens doen ontstaan, leidde de aanwezigheid van E590D-APP tot sterkere aggregatie dan zowel normaal APP als geen APP. In een muismodel dat al gevoelig is voor tau-problemen maakte het injecteren van een virus dat het gemuteerde APP in de hippocampus produceert de tau-kluwens erger en activeerde het sterker astrocyten en microglia, de ondersteunende en immuuncellen van de hersenen. Interessant genoeg waren standaard oplosbare amyloïdefragmenten moeilijk te detecteren in deze muizenhersenen, maar verscheen er slechts wanneer de mutatie aanwezig was een onderscheidend APP-afgeleid fragment, wat wijst op gewijzigde verwerking in levende weefsels.
Wat dit betekent voor het begrijpen van Alzheimer
Alles bij elkaar laten de bevindingen zien dat deze zeldzame APP-mutatie niet onschuldig is. Ze duwt APP richting de productie van meer dan één toxisch peptide, versnelt de internalisatiestappen die schadelijke knippen bevorderen, en versterkt tau-verstrengeling en ontsteking in de hersenen. Voor niet-specialisten is de kernboodschap dat de biologie van Alzheimer niet door één probleemmaker wordt aangedreven, maar door een netwerk van onderling reagerende eiwitfragmenten en cellulaire reacties. Het bestuderen van zulke krachtige maar ongewone genetische varianten geeft een vergrootglas op dat netwerk. In dit geval suggereert het dat therapieën zowel amyloïde als alternatieve APP-afgeleide peptiden zoals Aη — en hun gecombineerde impact op tau — moeten overwegen, in plaats van één route geïsoleerd aan te pakken.
Bronvermelding: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Trefwoorden: Ziekte van Alzheimer, amyloïde precursor-eiwit, tau-kluwens, neuro-inflammatie, genetische mutatie