Clear Sky Science · nl
Een hoogdoorvoerende, kwantitatieve platformbenadering met 2D-gedissocieerde menselijke cerebrale organoïden om neuroinflammatie bij de ziekte van Alzheimer te modelleren
Waarom infecties van belang kunnen zijn voor geheugenverlies
De ziekte van Alzheimer wordt meestal omschreven als een langzame ophoping van kleverige eiwitten in de hersenen, maar steeds meer bewijs suggereert dat infecties dit proces kunnen helpen starten. Deze studie onderzoekt dat idee met behulp van kleine in het laboratorium gekweekte modellen van de menselijke hersenen en stelt een eenvoudige vraag: kan een veelvoorkomend koortslipvirus Alzheimerachtige veranderingen in menselijke hersencellen veroorzaken, en kan een antiviraal middel die veranderingen terugdraaien?
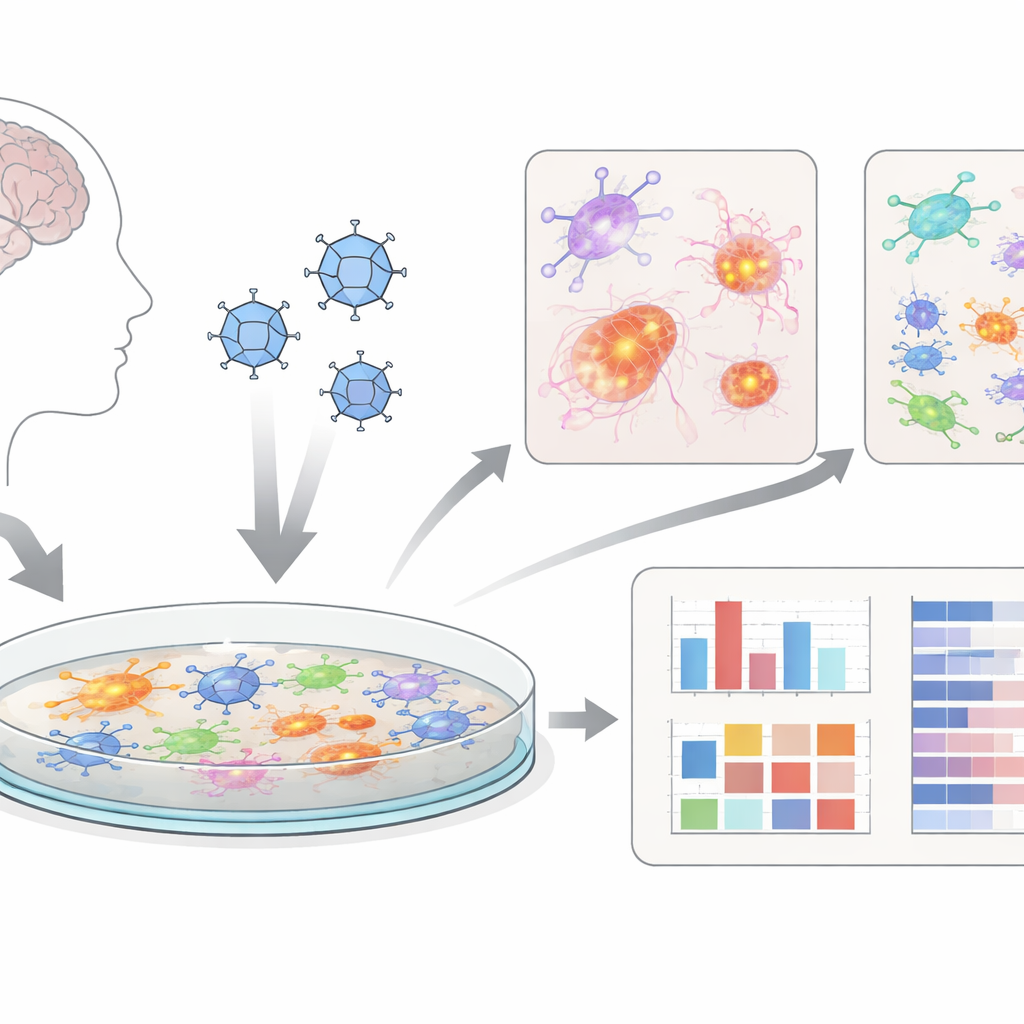
Mini-hersenen op een petrischaal
In plaats van alleen met dieren te werken, gebruikten de onderzoekers “cerebrale organoïden” – clusters van hersenachtige cellen gekweekt uit humane stamcellen. Ze maakten deze driedimensionale organoïden voorzichtig kapot tot platte lagen met gemengde hersencellen, waaronder neuronen, ondersteunende astrocyten en immuunachtige microglia. Deze tweedimensionale kweekjes, die zij dcOrgs noemen, zijn gemakkelijker gelijkmatig te infecteren en geschikt voor grootschalige, parallelle testen, waarbij veel platen en geneesmiddelcondities tegelijk kunnen worden onderzocht. Dat maakt het systeem aantrekkelijk als screeningsinstrument voor nieuwe behandelingen.
Een koortslipvirus als vonk
Het team infecteerde dcOrgs met herpes simplexvirus 1 (HSV-1), het virus dat verantwoordelijk is voor de meeste koortsblaasjes en dat al langer wordt verdacht een rol te spelen bij dementie bij sommige mensen. Ze vergeleken geïnfecteerde kweekjes met nepbehandelde controles, met kweekjes die een antiviraal middel (acyclovir) kregen, met kweekjes blootgesteld aan een ander virus (influenza A) en met virus dat met ultraviolet licht was geïnactiveerd. Met geautomatiseerde celanalyse en enkelcelsequencing bevestigden ze dat HSV-1 veel celtypen op het schaaltje effectief infecteerde, terwijl het geïnactiveerde virus en influenza duidelijk andere, mildere veranderingspatronen veroorzaakten.
Alzheimerachtige veranderingen binnenin en tussen cellen
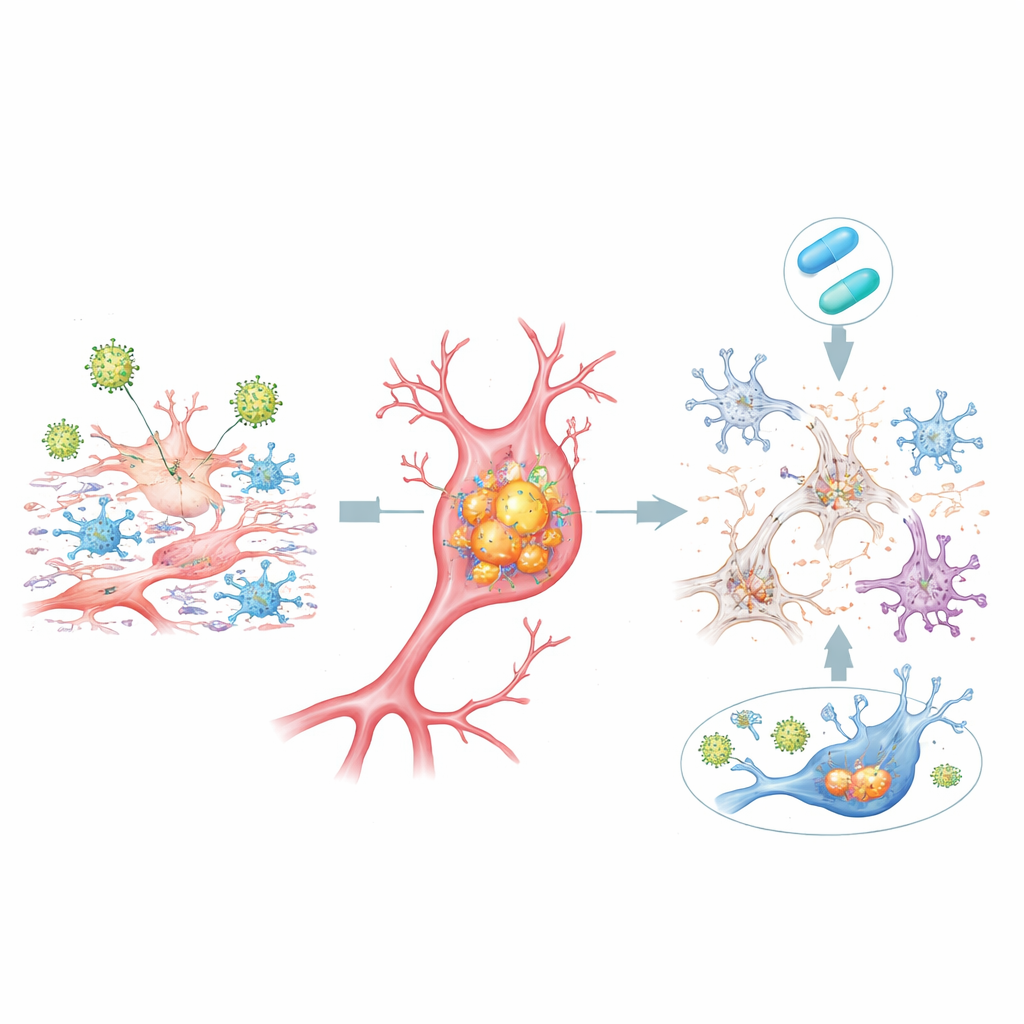
In HSV-1–geïnfecteerde dcOrgs stapelden veel cellen hoge niveaus op van dezelfde eiwitvormen die in Alzheimerhersenen worden gezien: klonterende bèta-amyloïde binnen cellen en meerdere “gefosforyleerde” varianten van tau, een ander centraal ziekte-eiwit. Deze ophopingen waren het sterkst gekoppeld aan cellen die virale eiwitten bevatten en waren bijzonder uitgesproken in stervende cellen. Tegelijkertijd werd relatief minder van het langere bèta-amyloïdefragment (Aβ42) vrijgegeven in de omliggende vloeistof vergeleken met kortere vormen, een verschuiving die overeenkomt met patronen gemeten in het ruggenmergvocht van patiënten met de ziekte van Alzheimer. Ook veranderden celpopulaties: het aantal neuronen daalde, terwijl astrocyten en microglia toenamen, wat de neuronale verlies en reactieve ontsteking weerspiegelt die in weefsel van patiënten worden gezien.
Genactiviteit verbindt het model met menselijke Alzheimer
Toen de onderzoekers de genactiviteit over het hele genoom bekeken, vonden ze dat HSV-1-infectie in dcOrgs veel genen aan- en uitzette die eerder in grote menselijke genetische studies met Alzheimer-risico waren geassocieerd. Deze veranderingen werden niet gezien in eenvoudigere stamcelculturen of in influenza-geïnfecteerde dcOrgs, wat wijst op een specifieke wisselwerking tussen HSV-1 en de gemengde hersenachtige omgeving. Enkelcelsequencing liet zien dat sommige van de Alzheimer-geassocieerde genverschuivingen afkomstig waren van cellen die aan het virus waren blootgesteld maar zelf weinig of geen viraal genetisch materiaal bevatten, wat suggereert dat signalen van geïnfecteerde buren schadelijke ontstekingsprogramma’s kunnen verspreiden.
Wat antivirale behandeling wel en niet kan herstellen
Toediening van het antivirale middel acyclovir kort na blootstelling aan HSV-1 verminderde de virale genexpressie, dempte veel ontstekingsreacties, verlaagde de ophoping van toxische bèta-amyloïde en tau binnen cellen en herstelde gedeeltelijk de balans tussen verschillende celtypen. Voor een substantieel deel van de Alzheimer-geassocieerde genen bewogen hun activiteitsniveaus weer naar normaal. Niet alle veranderingen waren echter omkeerbaar: een aanzienlijke groep humane genen bleef onveranderd of raakte zelfs verder verstoord door de behandeling, vooral wanneer het middel minder effectief was in het blokkeren van latere virale genen. Dit benadrukt dat het stoppen van virale replicatie kan helpen, maar mogelijk niet de hele biologische cascade kan terugdraaien zodra die op gang is gekomen.
Wat dit betekent voor het begrip van Alzheimer
Voor niet-specialisten is de hoofdconclusie dat een menselijk koortslipvirus, werkend binnen een realistische mix van menselijke hersencellen, snel veel kenmerken van de ziekte van Alzheimer kan produceren – van eiwitklonters en stervende neuronen tot genetische patronen die al bij patiënten zijn waargenomen. Het hier ontwikkelde platte, organoïde gebaseerde systeem is snel, kwantitatief en schaalbaar, en vormt daarmee een krachtig testveld voor antivirale middelen en andere therapieën gericht op het kalmeren van hersenontsteking. Hoewel dit niet bewijst dat herpesinfecties bij iedere patiënt Alzheimer veroorzaken, versterkt het de aanwijzing dat bij een subset van mensen chronische of gereactiveerde virusinfecties een belangrijk onderdeel van de puzzel kunnen vormen — en een potentieel doel voor preventie.
Bronvermelding: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Trefwoorden: Ziekte van Alzheimer, herpes simplex-virus, hersenorganoïden, neuroinflammatie, antivirale therapie