Clear Sky Science · nl
Functionele randen in grafen coderen om ruimtelijk variërende relaties in het tumormilieu te modelleren
Waarom het in kaart brengen van de omgeving van kanker ertoe doet
Kanker groeit niet geïsoleerd. Tumorcellen leven in een drukke omgeving van immuuncellen, ondersteunende cellen, bloedvaten en chemische signalen, allemaal dicht opeengepakt in de ruimte. Hoe deze buren gerangschikt zijn en hoe sterk ze elkaar beïnvloeden, kan bepalen of een kanker uitzaait, op behandeling reageert of onder controle blijft. Dit artikel introduceert SPIFEE, een nieuw kunstmatig-intelligentiekader dat microscopische beelden en moleculaire kaarten van tumoren omzet in netwerken, waardoor onderzoekers kunnen aanwijzen welke cel- en padinteracties het sterkst samenhangen met ziektetype en uitkomst voor de patiënt.
Weefsel omzetten in een netwerkkaart
Moderne kankeronderzoeken meten veel meer dan alleen hoe een tumor onder de microscoop eruitziet. Sommige methoden markeren tientallen eiwitten op individuele cellen, andere leveren gedetailleerde gekleurde weergaven van weefselstructuur, en nieuwere technieken leggen vast welke genen actief zijn op duizenden locaties over een tumordwarsdoorsnede. SPIFEE behandelt al deze bronnen als verschillende gezichtspunten op dezelfde omgeving. Het stelt elk monster voor als een graaf: knooppunten staan voor sleutelentiteiten in het tumormilieu—zoals celtypen, visuele weefselpatronen of moleculaire paden—terwijl randen vastleggen hoe deze entiteiten ruimtelijk met elkaar interageren. Cruciaal is dat SPIFEE een interactie niet reduceert tot één enkel getal zoals “afstand.” In plaats daarvan slaat elke rand een klein kromme op die beschrijft hoe sterk twee entiteiten mengen of elkaar afstoten over een reeks afstanden, waardoor veel rijkere ruimtelijke details bewaard blijven.
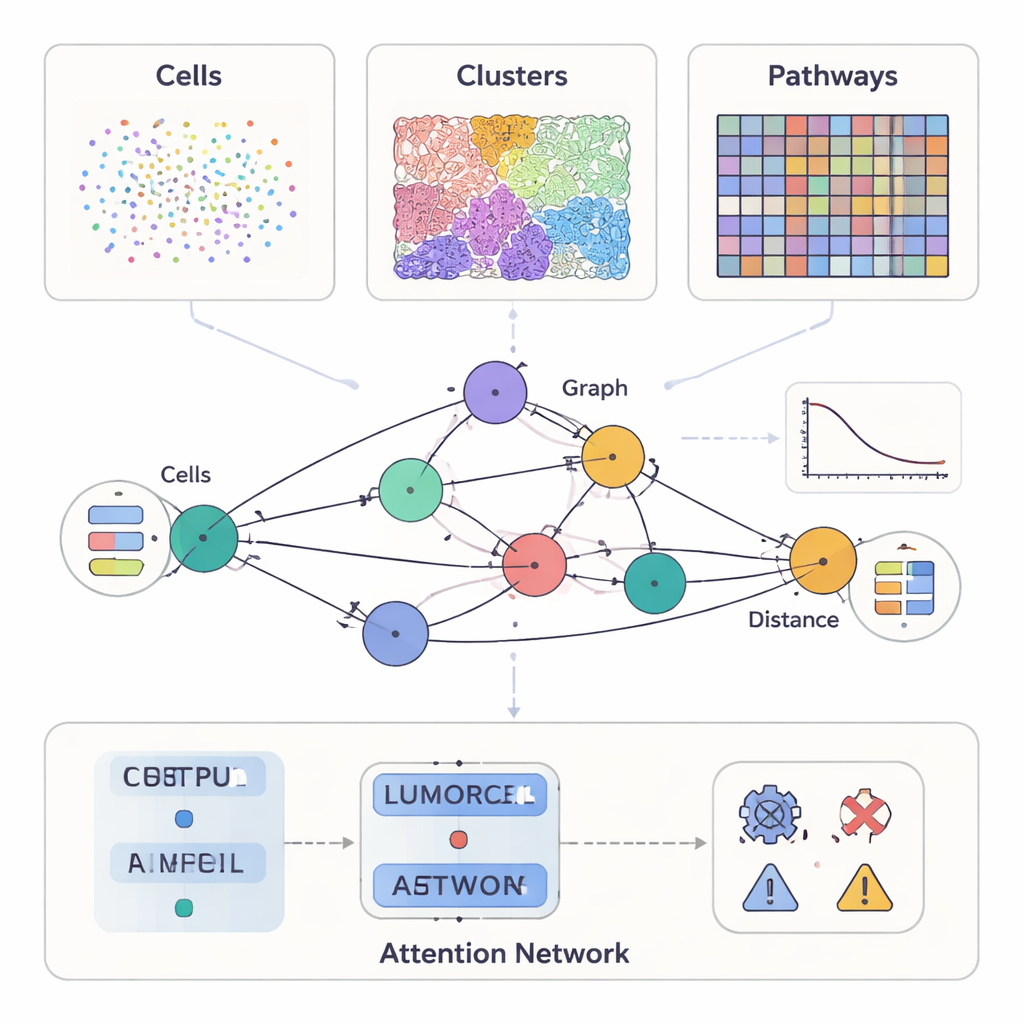
Een flexibele lens voor veel soorten kankergegevens
De auteurs testten SPIFEE op meerdere grote, onafhankelijke kankerdatasets die verschillende technologieën en schalen bestrijken. In pancreasaandoeningen die met multiplex immunofluorescentie waren gemarkeerd, vertegenwoordigde elk knooppunt in de graaf een celtype, en kwamen knooppunteigenschappen uit single-cell RNA-sequencing die samenvatten hoe die cellen geneigd zijn te communiceren. In longkankersneden geverfd met de gebruikelijke hematoxylineen-eosine-methode, vertegenwoordigden knooppunten terugkerende visuele weefselpatronen die automatisch werden ontdekt door een zelf-gestuurde leermethode. In een derde toepassing werden standaard longkankersneden door een deep-learningtool omgezet in virtuele ruimtelijke transcriptomica, en vertegenwoordigden SPIFEE-knooppunten moleculaire paden zoals hypoxie, oestrogeen- of JAK–STAT-signalering, met kenmerken afgeleid van genactiviteit. In al deze scenario’s kon hetzelfde kader verschillende typen knooppunten verwerken en toch vergelijkbare ruimtelijke grafen bouwen.
De interacties vinden die uitkomsten scheiden
Zodra SPIFEE een graaf heeft opgebouwd, verwerkt het die met een graph attention network, een soort neuraal netwerk dat niet alleen leert een uitkomst te voorspellen—zoals kankersubtype, overlevingsrisico of ziekte versus niet-kankergeïnduceerde ontsteking—but ook benadrukt welke randen het meest belangrijk waren voor die voorspelling. In pancreatisch weefsel onderscheidde SPIFEE chronische pancreatitis van pancreas ductaal adenocarcinoom met hogere nauwkeurigheid dan eerdere graafgebaseerde methoden. Het model concentreerde zich consequent op interacties waarbij epitheliale (tumorachtige) cellen en regulerende T-cellen, antigeen-presenterende cellen en helper-T-cellen betrokken waren, wat wijst op een immuunsuppressieve omgeving die prominenter is bij kanker dan bij ontsteking. In longadenocarcinoom-sneden identificeerde SPIFEE specifieke stroma‑tumorpatronen waarvan de interacties correleerden met betere of slechtere overleving, wat suggereert dat de “grenszones” tussen tumor en ondersteunend weefsel belangrijke prognostische aanwijzingen bevatten die standaardanalyses mogelijk missen.
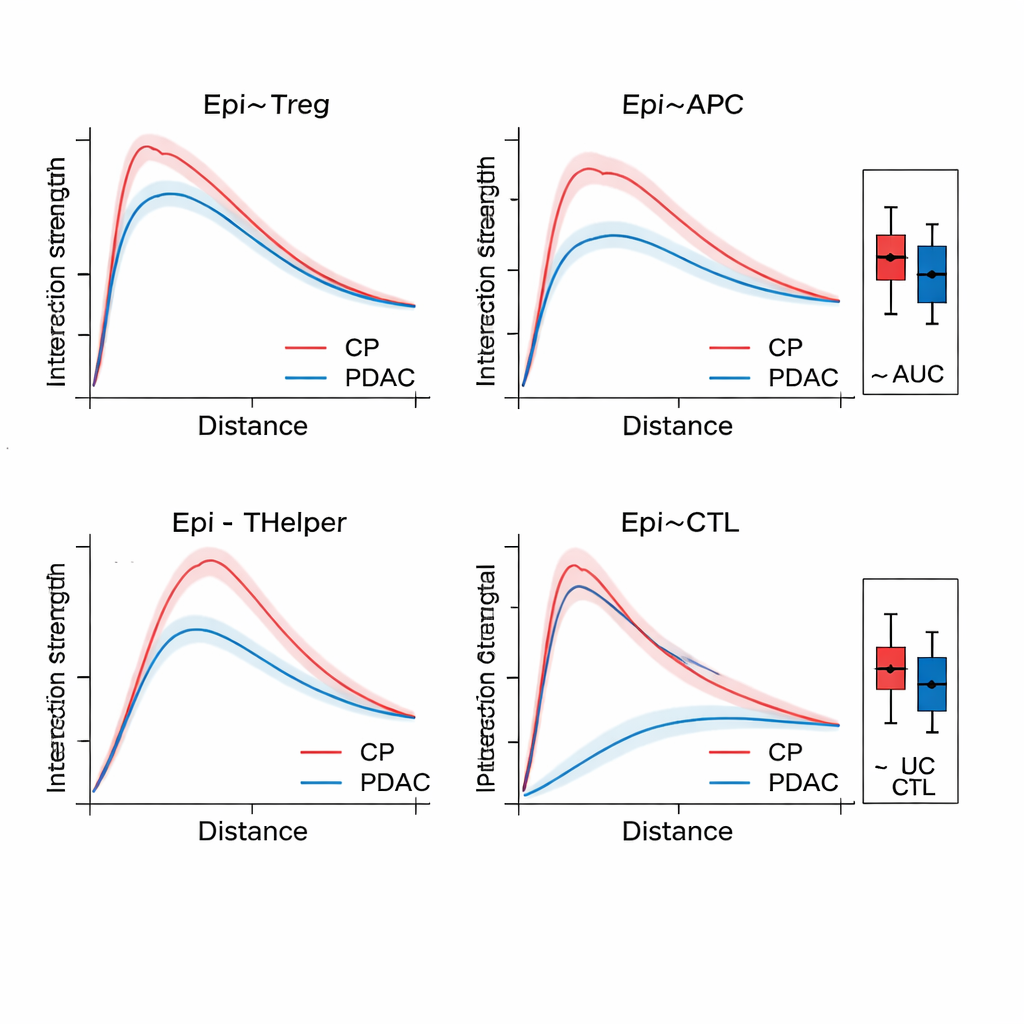
Moleculaire crosstalk lezen uit routinematig genomen sneden
Misschien nog opvallender: SPIFEE kon zinvolle padinteracties afleiden uit gewone pathologiefoto’s zodra die waren vertaald naar voorspelde gen-activiteitskaarten. Door paden als knooppunten te behandelen en hun ruimtelijke co-voorkomen als functionele randen, belichtte de methode paren zoals hypoxie met EGFR of JAK–STAT met PI3K—combinaties die al bekendstaan als drijvers van immuunontwijking en medicijnresistentie bij longkanker. Het plaatste ook oestrogeen-gerelateerde paden hoger in longadenocarcinoom en bepaalde immuun- en stresspaden in plaveiselcelcarcinomen, bevindingen die overeenkomen met patronen gezien in bulk-RNA‑sequencing en in een onafhankelijke echte ruimtelijke transcriptomica-dataset. Dit suggereert dat, zelfs wanneer moleculaire metingen benaderd zijn, ruimtelijke patronen in routinematige sneden nog steeds terugvindbare signalen bevatten over hoe sleutelpaden in levende tumoren met elkaar interageren.
Wat dit betekent voor toekomstige kankerzorg
Voor niet-specialisten is de kernboodschap dat SPIFEE een nieuwe manier biedt om het “sociale leven” van kankercellen direct uit beelden en moleculaire kaarten af te lezen. Door te coderen hoe relaties veranderen met afstand in plaats van ze te plakken op enkelvoudige scores, en door attention-gebaseerde neurale netwerken te gebruiken om te rangschikken welke interacties het belangrijkst zijn, kan het kader combinaties van cellen, weefselpatronen en paden blootleggen die kankertypen onderscheiden en overleving voorspellen. Hoewel deze bevindingen nog biologische en klinische validatie vereisen, wijzen benaderingen zoals SPIFEE op een toekomst waarin routinematige tumormonsters niet alleen statische momentopnames leveren, maar dynamische kaarten van interactie-hotspots die kunnen helpen bij diagnose, risicostratificatie en uiteindelijk gepersonaliseerde behandelkeuzes.
Bronvermelding: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Trefwoorden: tumormilieu, ruimtelijke transcriptomica, graph neural networks, kankerpathologie, cel-cel interacties