Clear Sky Science · nl
Door AI aangedreven 3D subcellulaire RPE-kaart ontdekt celtoestandoverdrachten bij het vestigen van apicaal-basale polariteit
Waarom de ondersteunende cellen van het oog ertoe doen
Het scherpe zicht dat we dagelijks ervaren berust op een dunne laag ondersteunende cellen achter in het oog, het retinale pigmentepitheel (RPE). Wanneer deze cellen hun ordelijke interne structuur verliezen, kunnen zichtberovende aandoeningen zoals leeftijdsgebonden maculadegeneratie ontstaan. Deze studie combineert stamcelbiologie, geavanceerde microscopie, kunstmatige intelligentie en wiskundige modellering om een gedetailleerde driedimensionale “digitale tweeling” van een RPE-cel te bouwen, waarmee wordt onthuld hoe de interne onderdelen zich herschikken naarmate de cel rijpt en wat er misgaat wanneer dat proces verstoord raakt.
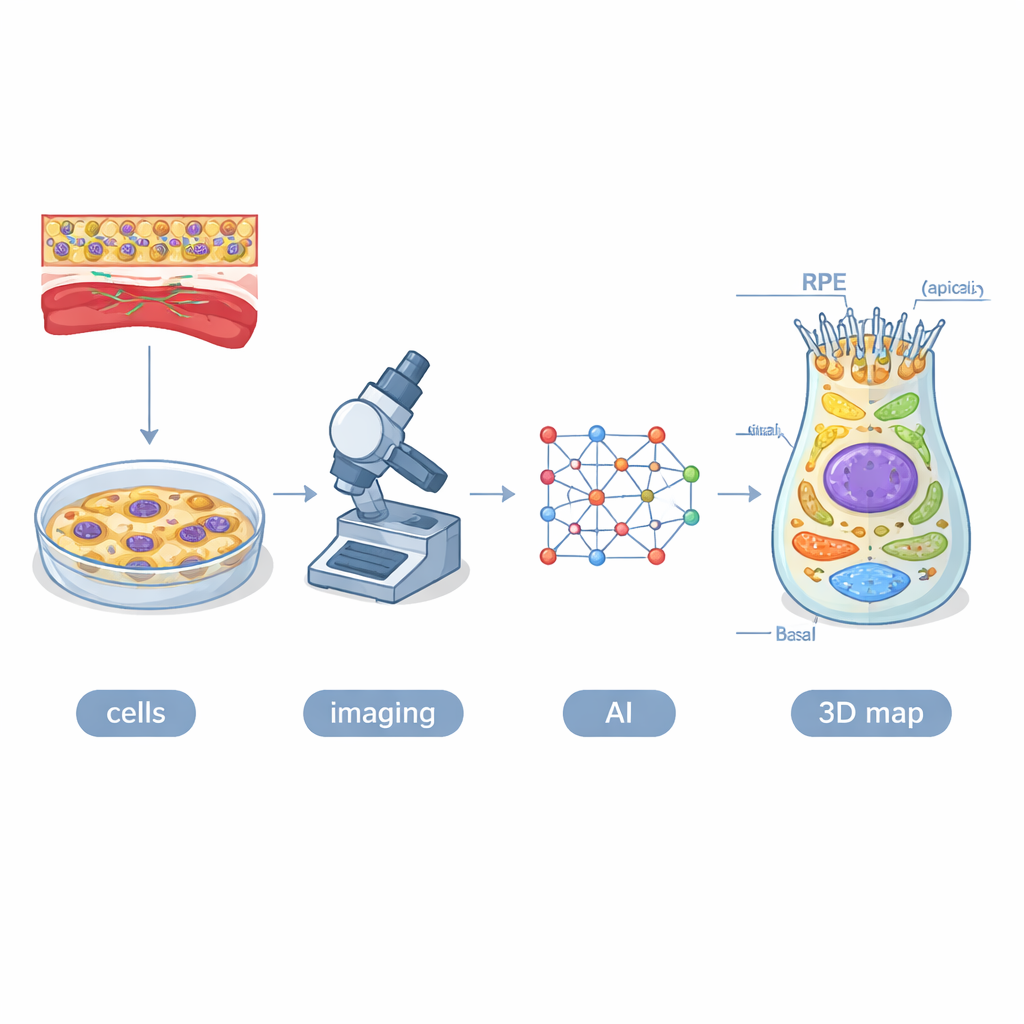
Het bouwen van een digitale tweeling van oogcellen
De onderzoekers begonnen met humane geïnduceerde pluripotente stamcellen — cellen die zijn geherprogrammeerd om zich als embryonale cellen te gedragen — en stroomden deze om naar RPE. Ze gebruikten 16 geconstrueerde cellijnen waarbij verschillende cellulaire structuren, zoals mitochondriën, lysosomen en het buitenste cytoskelet van de cel, groen oplichtten onder de microscoop. Gedurende vier weken maakten ze driedimensionale opnames van ongeveer 1,3 miljoen cellen met high-content confocale microscopie. Om deze enorme dataset te interpreteren, ontwikkelden ze een AI-systeem genaamd POLARIS, gebaseerd op een type neuraal netwerk dat automatisch elke cel, de kern en de gemarkeerde organellen in elke beeldlaag kan omlijnen. Menselijke experts controleerden en verfijnden het werk van de machine, waarna het team de resultaten combineerde tot een gemiddelde driedimensionale model — een digitale tweeling — van een typische RPE-cel in elke fase.
Twee paden: gezonde rijping versus geblokkeerde polariteit
RPE-cellen moeten “gepolariseerd” raken, met duidelijke bovenste (apicale) en onderste (basale) zijden, om voedingsstoffen te transporteren, afval te verwijderen en te communiceren met zowel het netvlies als de bloedvoorziening. Om dit te stimuleren, behandelde het team sommige kweekjes met een molecuul genaamd PGE2, dat de vorming van een klein zintuiglijk structuur, de primaire cilium, bevordert en polariteit versterkt. Andere kweekjes kregen HPI4, dat de cilia verstoort en verhindert dat polariteit zich goed ontwikkelt. Met behulp van metingen afgeleid uit POLARIS toonden de onderzoekers aan dat in het gezonde pad cellen langer en smaller werden en hun kernen compacter en ronder werden. Onder HPI4 bleven cellen platter en wijder, met meer onregelmatige vormen. Statistische modellen lieten zien dat bij succesvol polariserende cellen deze vormveranderingen een voorspelbare, niet-willekeurige volgorde volgden, terwijl geblokkeerde cellen afgleden naar meer variabele, chaotische toestanden.
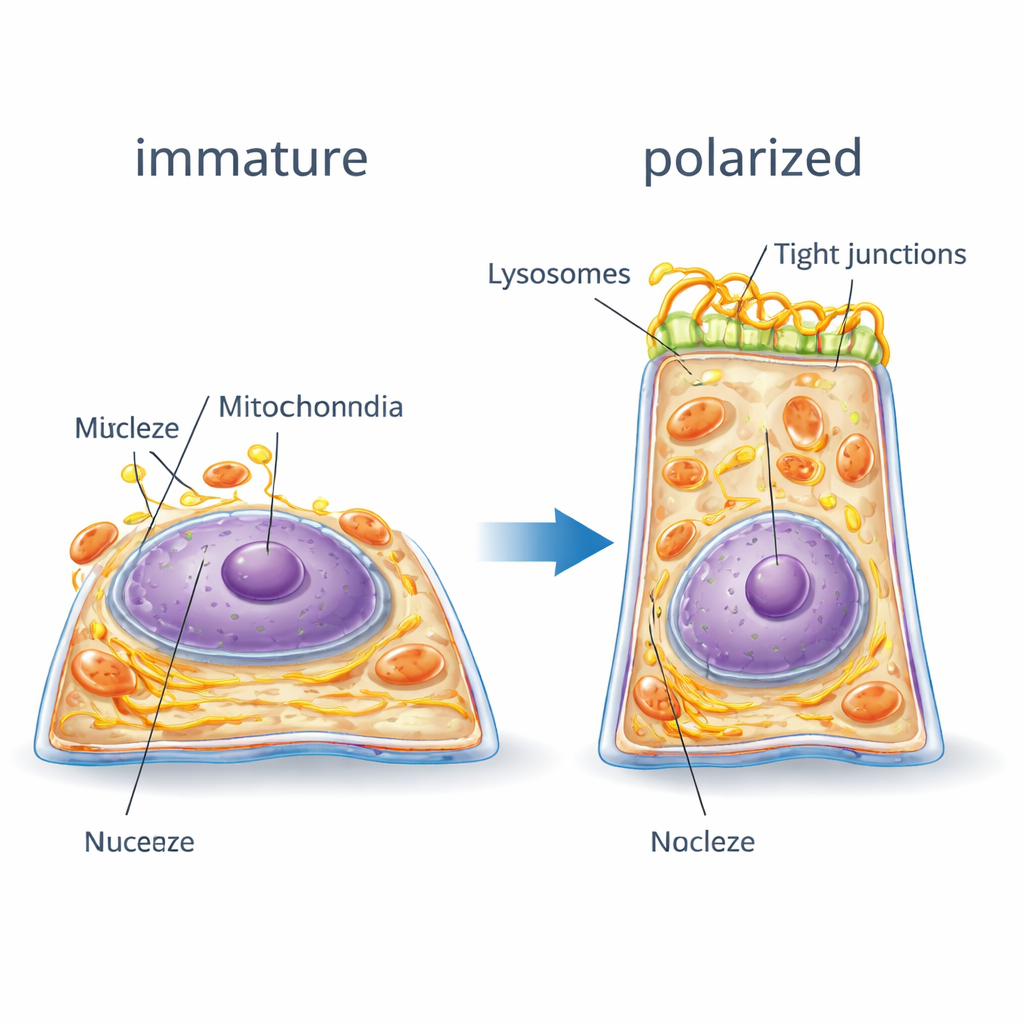
Hoe het interieur van de cel zich herschikt
De digitale tweeling maakte het mogelijk om te volgen hoe de interne architectuur van de cel zich reorganiseert. Naarmate RPE-cellen polariseerden, verschoof hun interne geraamte van actine- en myosinevezels van veel kleine fragmenten naar minder, dikkere strengen die de celranden omsloten — als het strakker trekken van een riem — om de nieuwe hoge vorm te ondersteunen. De kernomhulling ontwikkelde diepe plooien en cellen kregen doorgaans minder nucleoli, wat wijst op een rijper en stabieler genexpressieprogramma. Junction-eiwitten die naburige cellen aan elkaar verbinden verschoofen van verspreide locaties binnen de cel naar goed gedefinieerde banden langs de zijwanden, waardoor de barrière werd versterkt. Ondertussen vergrootten en migreerden energieproducerende mitochondriën en het endoplasmatisch reticulum, dat helpt bij de verwerking van eiwitten en lipiden, richting de kern en vormden coherente netwerken. Lysosomen, de recyclingcentra van de cel, verschoofen naar het centrale, bovenste gedeelte van de cel. Wanneer polariteit werd geblokkeerd waren veel van deze verplaatsingen onvolledig of afwezig, en bleven organellen meer willekeurig verspreid.
Gesprekken tussen organellen
Het team onderzocht ook welke organellen de neiging hebben dezelfde buurt binnen de cel te bezetten, een aanwijzing dat ze mogelijk functioneel met elkaar interageren. Door organelkaarten over de gemiddelde cel heen te leggen en te berekenen hoe sterk hun posities correleerden, vonden ze dat in goed-gepolariseerde cellen structuren zich groepeerden in gecoördineerde clusters. Bijvoorbeeld vormden peroxisomen, mitochondriën, endoplasmatisch reticulum, bepaalde junctions en delen van het cytoskelet een strak verbonden netwerk dat gerelateerd is aan energiegebruik en membraanhermodellering. Lysosomen vestigden zich bij de centrale organiserende hub van de cel, de centriole, wat wijst op een rol bij het beheersen van cilia en oppervlaktevernieuwing. Daarentegen verzwakten deze ruimtelijke relaties wanneer polariteit werd geblokkeerd, en leek het algemene “gesprek” tussen organellen gefragmenteerd. Machine-learning classificatoren getraind op deze kenmerken gaven aan dat de laterale verdeling van mitochondriën en de verticale plaatsing van tight junctions bijzonder krachtige merkers waren of een cel correct gepolariseerd was.
Waarom dit belangrijk is voor zicht en ziekte
Door AI, grootschalige beeldvorming en wiskundige analyse te combineren levert dit werk een rijk gedetailleerde 3D referentie van hoe gezonde menselijke RPE-cellen zich in ruimte en tijd organiseren, en hoe die organisatie instort wanneer polariteit faalt. Voor niet-specialisten is de kernboodschap dat de gezondheid van het netvlies niet alleen afhangt van welke moleculen aanwezig zijn, maar van waar en wanneer cellulaire componenten binnen elke ondersteunende cel worden gerangschikt. De hier geproduceerde digitale tweeling biedt een kwantitatieve maatstaf om subtiele defecten in patiënt-afgeleide RPE te detecteren, en opent nieuwe wegen voor het diagnosticeren van vroege cellulaire problemen bij retinale ziekten en voor het testen van therapieën die erop gericht zijn de juiste celstructuur te herstellen voordat het zicht onherstelbaar verloren gaat.
Bronvermelding: Ortolan, D., Sathe, P., Volkov, A. et al. AI driven 3D subcellular RPE map discovers cell state transitions in establishment of apical-basal polarity. npj Artif. Intell. 2, 20 (2026). https://doi.org/10.1038/s44387-026-00074-6
Trefwoorden: retinale pigmentepitheel, celpolariteit, kunstmatige intelligentie, 3D celmapping, leeftijdsgebonden maculadegeneratie