Clear Sky Science · nl
Een metabolisme-geïnformeerd neuraal netwerk identificeert routes die de werkzaamheid en toxiciteit van antimicrobiële combinaties beïnvloeden
Waarom dit belangrijk is voor de dagelijkse gezondheid
Naarmate meer infecties niet meer reageren op onze standaardantibiotica, grijpen artsen steeds vaker naar combinaties van geneesmiddelen. Maar het mengen van medicijnen kan tweeërlei uitpakken: de juiste combinatie kan hardnekkige bacteriën uitroeien, terwijl een onjuiste mix organen zoals de nieren en de lever kan schaden. Deze studie introduceert een nieuwe computergebaseerde benadering, CALMA genaamd, die onderzoekers en clinici moet helpen geneesmiddelcombinaties te vinden die zowel krachtig tegen microben als minder belastend voor patiënten zijn.
Germs bestrijden zonder giswerk
Traditioneel betekende het vinden van goede antibioticacombinaties het in het lab en bij patiënten testen van enorme aantallen paren of trio’s geneesmiddelen. Het aantal mogelijke mengsels groeit explosief met elk toegevoegd middel, waardoor volledige experimentele toetsing onrealistisch wordt. Daarbovenop richten de meeste bestaande hulpmiddelen zich alleen op hoe sterk combinaties bacteriën doden en negeren ze hoe die combinaties mogelijk menselijk weefsel kunnen beschadigen. De auteurs betogen dat we, om betere therapieën te ontwerpen, beide zijden van de vergelijking moeten meenemen: werkzaamheid tegen ziekteverwekkers en veiligheid voor mensen.
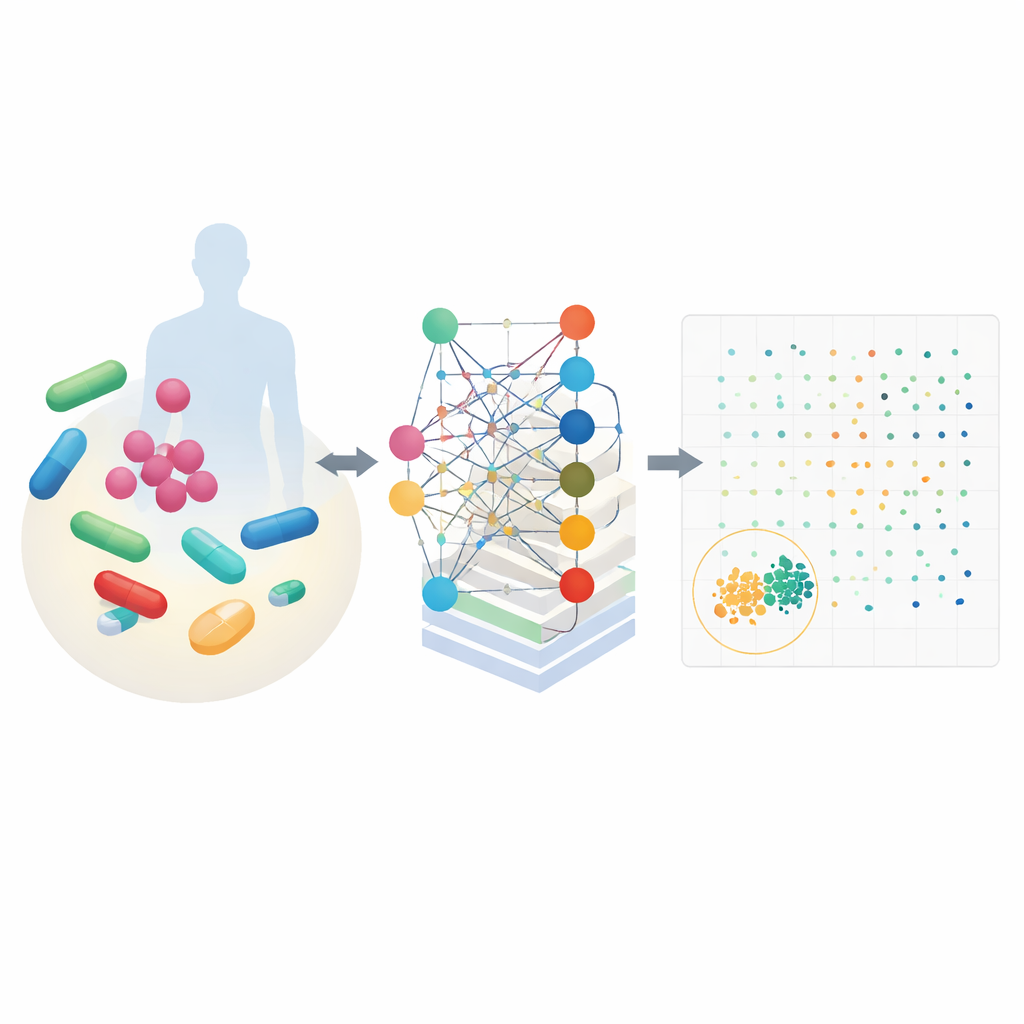
Een slim model dat celchemie begrijpt
CALMA combineert twee krachtige ideeën. Ten eerste gebruikt het gedetailleerde kaarten van cellulaire metabolisme die beschrijven hoe organismen voedingsstoffen omzetten in energie en bouwstenen. Deze kaarten, opgesteld voor bacteriën zoals Escherichia coli en de tuberculosekiem, simuleren hoe duizenden chemische reacties veranderen wanneer een geneesmiddel aanwezig is. Ten tweede voert CALMA deze simulaties in een kunstmatig neuraal netwerk waarvan de structuur de metabole routes weerspiegelt. Door informatie te groeperen volgens bekende biologische paden—zoals energieproductie of nucleotide-recycling—leert het model patronen herkennen die specifieke routes koppelen aan óf effectieve bacteriedoding óf schadelijke bijwerkingen in menselijke cellen.
Het landschap van geneesmiddelmengsels verkennen
Met gebruik van gegevens uit eerdere experimenten en grote veiligheidsdatabanken trainden de onderzoekers CALMA om elke geneesmiddelcombinatie twee scores toe te kennen: één voor hoe sterk het de bacteriën aanvalt en één voor hoe waarschijnlijk het toxiciteit bij mensen veroorzaakt. Het uitzetten van deze scores creëert een landschap waarin de beste kandidaten in de linkerbenedenhoek zitten—krachtig tegen microben en zacht voor menselijke cellen. Toen zij CALMA toepasten op 35 klinisch relevante middelen, reduceerde het hulpmiddel bijna 600 mogelijke paren tot een kleine set veelbelovende opties, en verkleinde daarmee de experimentele zoekruimte met ongeveer 97 procent. Onder de topaanbevelingen waren combinaties met veelgebruikte antibiotica zoals azithromycine, vancomycine, isoniazide en trimethoprim.
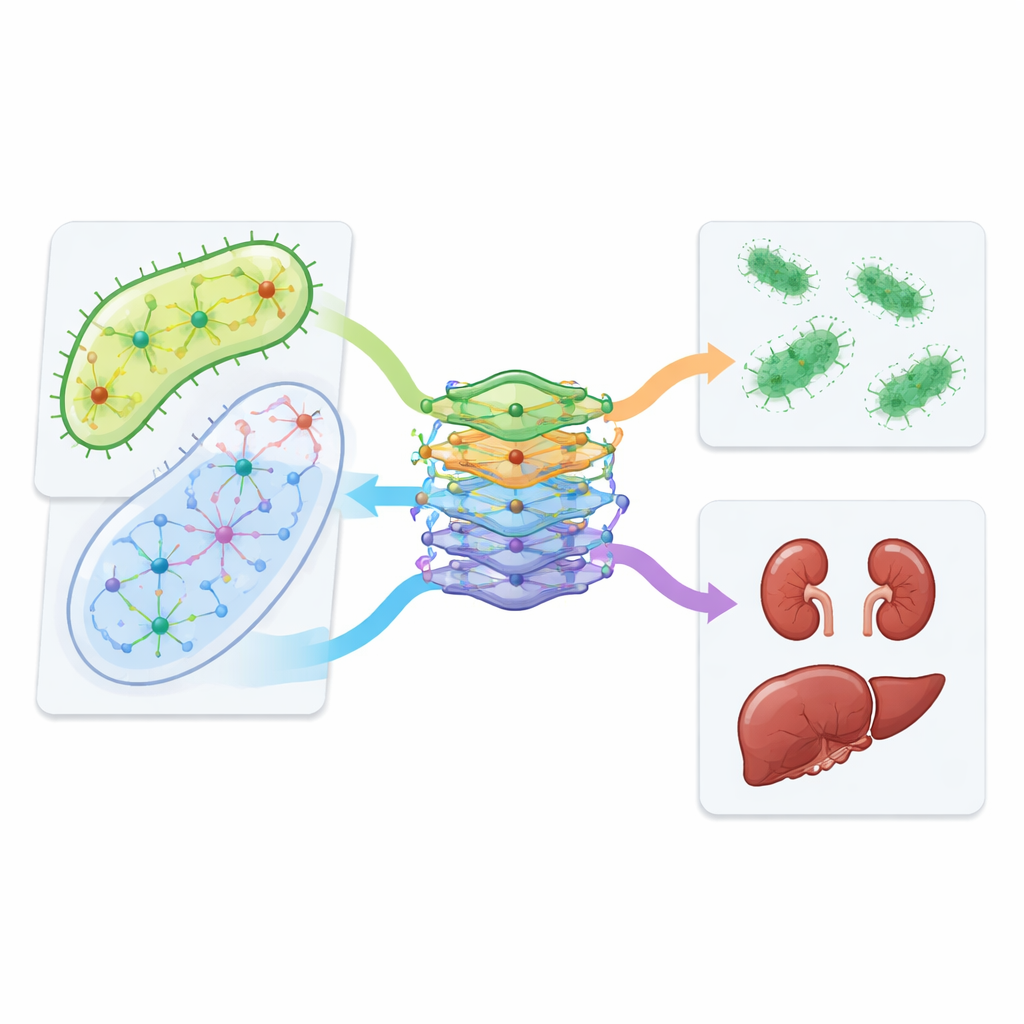
Van computervoorspellingen naar labtests en echte patiënten
Het team ging voorbij simulaties en testte meerdere voorspelde combinaties in nier- en levercellijnen. Ze ontdekten dat bepaalde paren, waaronder azithromycine met vancomycine en isoniazide met trimethoprim, minder toxisch waren voor menselijke cellen dan de afzonderlijke middelen, terwijl ze toch actief bleven tegen E. coli. Het ontwerp van CALMA stelde de onderzoekers ook in staat te onderzoeken welke metabole routes de toxiciteit aansturen. Een pad dat DNA-bouwstenen recyclet, bekend als nucleotide-salvage, bleek een belangrijke rol te spelen: het aanpassen daarvan in celexperimenten veranderde hoe schadelijk sommige combinaties waren. Ten slotte onderzochten de auteurs medische dossiers van honderden duizenden patiënten en zagen dat mensen die azithromycine samen met vancomycine kregen minder gedocumenteerde nierproblemen hadden dan vergelijkbare patiënten die alleen vancomycine kregen, wat de laboratoriumbevindingen weerspiegelt.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten kan CALMA worden gezien als een intelligente filter die genoeg biologie begrijpt om te suggereren welke geneesmiddelmengsels het eerst het testen waard zijn. In plaats van antibiotica blindelings te combineren en op het beste te hopen, kunnen onderzoekers zich richten op combinaties waarvan modellen voorspellen dat ze bacteriële zwakke plekken raken terwijl kwetsbare menselijke paden gespaard blijven. Hoewel de methode afhankelijk is van beschikbare gegevens en niet perfect is, biedt ze een rationelere route naar het ontwerpen van combinatietherapieën. In de loop van de tijd zouden tools als CALMA artsen kunnen helpen resistente infecties veiliger te behandelen, het giswerk in geneesmiddelenontwikkeling te verminderen en zelfs aangepast kunnen worden voor andere aandoeningen waarbij combinatietherapieën en bijwerkingen belangrijke zorgpunten zijn.
Bronvermelding: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Trefwoorden: antibiotica-combinaties, geneesmiddelentoxiciteit, kunstmatige neurale netwerken, metabolisme, antimicrobiële resistentie