Clear Sky Science · nl
Interaction-beperkte 3D-molecuulgeneratie met een diffusie-model maakt structuurgebaseerde farmacofore modellering voor medicijnontwerp mogelijk
Waarom het ontwerpen van betere medicijnen zo moeilijk is
Modern geneesmiddelenonderzoek draait vaak om het overtuigen van een klein molecuul om in een eiwit te passen als een sleutel in een slot. Maar de sleutel moet meer doen dan alleen passen: hij moet de juiste reeks kleine aantrekkingen vormen — zoals zwakke elektrische trekken en waterafstotende plekjes — zodat het geneesmiddel sterk en specifiek gebonden blijft. Het chemische universum is astronomisch groot, ver buiten wat de huidige databases bevatten, dus onderzoekers zoeken naar slimmere manieren om nieuwe sleutels helemaal zelf uit te vinden terwijl ze deze cruciale contactpatronen behouden.
Een computer leren wat echt telt
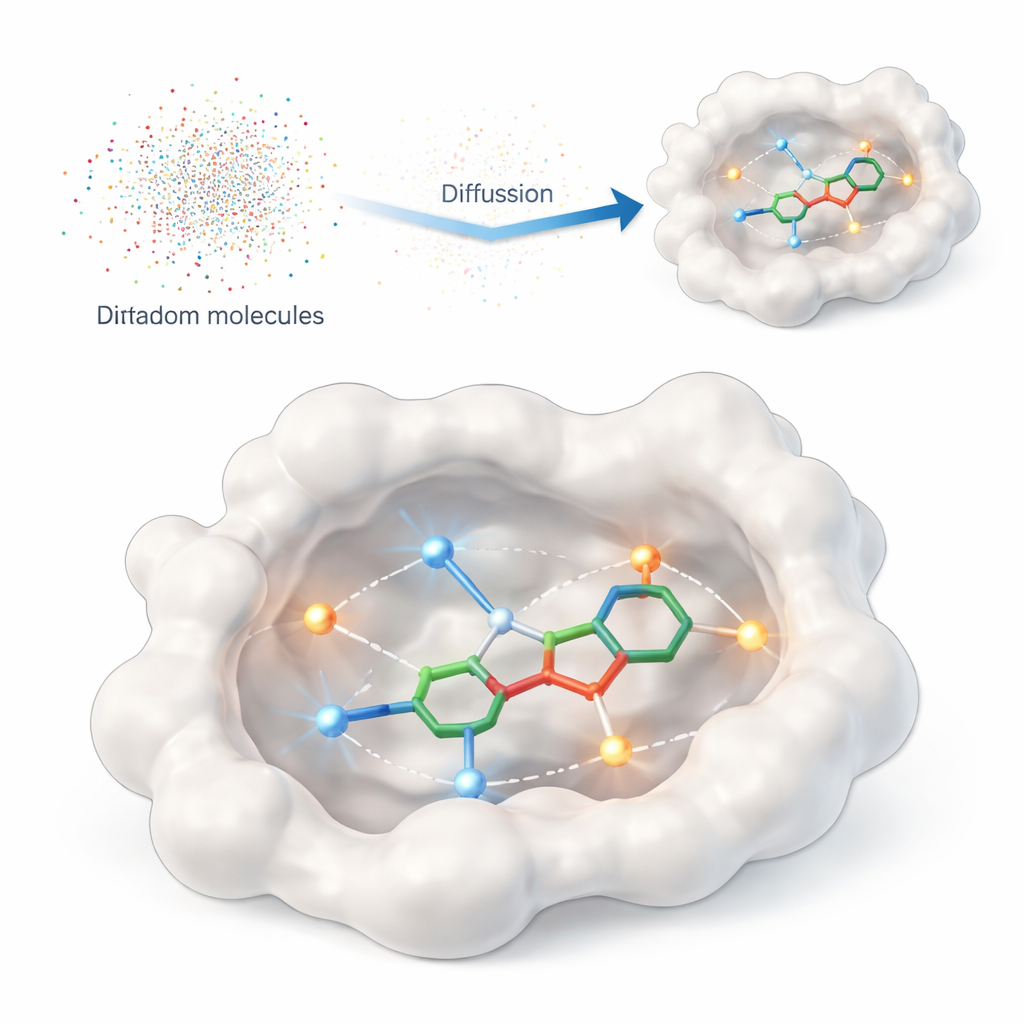
Deze studie introduceert DiffPharma, een computationeel kader dat driedimensionale, geneesmiddelachtige moleculen direct in de bindingsplaats van een eiwit genereert. In plaats van het algoritme bestaande enorme catalogi van verbindingen te laten doorzoeken, creëert DiffPharma nieuwe moleculen atoom voor atoom, gestuurd door hoe ze verondersteld worden met het eiwit te interageren. De methode is gebouwd op een moderne klasse van generatieve modellen genaamd diffusie-modellen, die beginnen met willekeurige ruis en die geleidelijk 'denoisen' tot een gestructureerd object — in dit geval een 3D-molecuul genesteld in de eiwitpocket.
De handdruk van het eiwit coderen
Om het model te vertellen wat belangrijk is op het eiwitoppervlak, representeren de auteurs sleutelcontacten als kleine "interactie-deeltjes" verspreid langs de paden tussen het eiwit en een referentiemolecuul. Twee veelvoorkomende interactietypen worden benadrukt: waterstofbruggen, die zich gedragen als directionele magneten tussen specifieke atomen, en hydrofobe contacten, waar olieachtige regio's samenklonteren weg van water. Aparte neurale netwerken leren de geometrie en chemie van elk interactietype, evenals de algemene vorm van de bindingspocket, en vervolgens combineert een speciale fusie-architectuur deze gezichtspunten tot één samenhangend beeld dat de molecuulgeneratie stuurt.
Hoe goed bootst het echte bindingspatronen na?
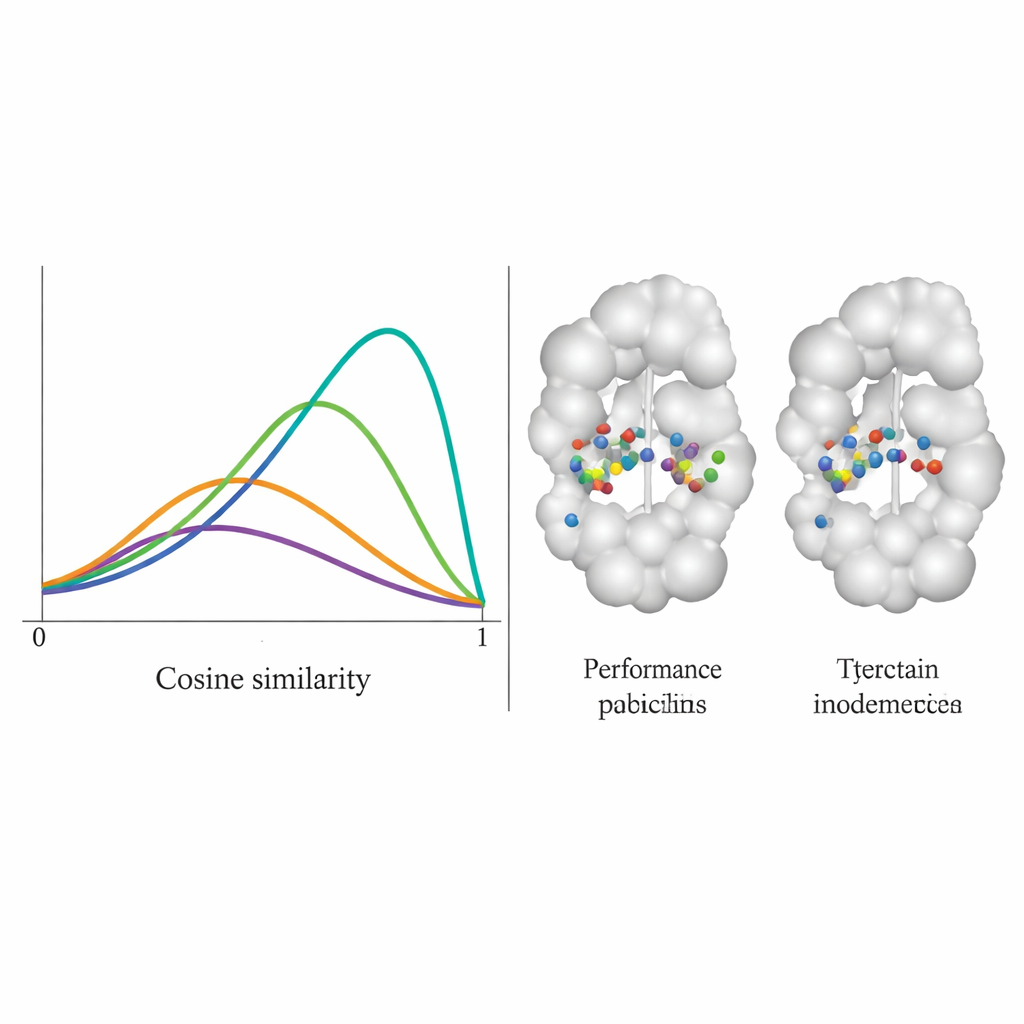
Het team testte DiffPharma op 100 verschillende eiwit–molecuulparen en vroeg hoe trouw nieuwe moleculen de oorspronkelijke contactpatronen nabootsten, residu voor residu. Ze maten dit met een cosinus-similariteitsscore tussen 0 en 1, waarbij 1 perfecte overeenstemming betekent. De distributie van DiffPharma piekte rond 0,9, wat betekent dat gemiddeld dezelfde eiwitresiduen dezelfde typen sleutelinteracties vormden als in de referentiestructuren — aanzienlijk beter dan zes concurrerende methoden. Belangrijk is dat het model dit deed terwijl het nog steeds een verscheidenheid aan moleculaire vormen produceerde, en de gegenereerde verbindingen behielden realistische bindingslengtes, hoeken en algemene 3D-geometrie die kenmerkend zijn voor echte, stabiele moleculen.
Van theorie naar praktische medicijnkandidaten
Buiten benchmarks vroegen de auteurs of DiffPharma plausibele medicijnkandidaten voor echte doelwitten kon ontwerpen. Voor twee goed bestudeerde enzymen — AKT-kinase en een β-lactamase die gekoppeld is aan antibioticaresistentie — genereerde de methode moleculen die de essentiële interactiepatronen van bekende liganden behielden en vaak verschillende chemische scaffolds gebruikten, een gewenste vorm van "scaffold hopping" in de medicinale chemie. In een zwaardere casestudy op de hoofprotease van SARS‑CoV‑2 werd DiffPharma aangestuurd met specifieke interactiekeuzes en vervolgens onderzocht met moleculaire-dynamica-simulaties en schattingen van bindingsenergieën. Moleculen die onder strengere interactiebeperkingen werden gegenereerd vormden stabielere complexen en toonden soms gunstiger voorspelde bindingsenergieën dan een bekende referentie-inhibitor. Opmerkelijk is dat het systeem zelfs die referentieverbinding herontdekte — ondanks dat deze nooit in de training voorkwam — louter op basis van de eiwitstructuur en interactie-instructies.
Wat dit betekent voor toekomstige medicijnen
Voor een niet‑specialist kan DiffPharma worden gezien als een slimme, 3D-bewuste ontwerptool voor geneesmiddelmoleculen: gegeven de vorm van een eiwitpocket en een gewenst patroon van "handdrukken", stelt het chemisch redelijke sleutels voor die passen en op de juiste manier interageren. Hoewel het nog niet elke eigenschap optimaliseert die een medicijn nodig heeft, zoals oplosbaarheid of metabolisme, behoudt de methode betrouwbaar de cruciale contactkaart op het eiwitoppervlak en verkent het nieuwe delen van chemische ruimte buiten de huidige catalogi. Deze door interacties geleide aanpak kan onderzoekers helpen sneller van structurele gegevens over ziektegerelateerde eiwitten naar diverse, realistische uitgangspunten voor experimentele medicijnontwikkeling te gaan.
Bronvermelding: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
Trefwoorden: structuurgebaseerd medicijnontwerp, moleculaire generatieve modellen, farmacofore modellering, eiwit–ligand interacties, SARS-CoV-2 hoofprotease