Clear Sky Science · nl
AI-gestuurde competitieve docking voor virtuele screening en voorspelling van samenstellingseffectiviteit
Slimmere zoektochten naar nieuwe geneesmiddelen
Het vinden van nieuwe medicijnen is een beetje alsof je een speld zoekt in een hooiberg van miljoenen moleculen. Deze studie laat zien hoe recente vooruitgang in kunstmatige intelligentie die zoektocht sneller en goedkoper kan maken door wetenschappers te helpen voorspellen welke moleculen het meest waarschijnlijk aan een ziektegerelateerd eiwit blijven plakken en daadwerkelijk als geneesmiddel werken. In plaats van één chemische stof tegelijk in het lab te testen, gebruiken de auteurs AI-modellen om virtuele wedstrijden tussen moleculen te laten lopen en de winnaars naar boven te laten komen.
Hoe AI leert moleculaire slot-en-sleutelpassingen te zien
Veel moderne medicijnen werken door in kleine zakjes op eiwitten te passen, vergelijkbaar met hoe een sleutel in een slot past. Traditioneel probeerden computerprogramma’s deze passing te voorspellen met behulp van fysische vergelijkingen die krachten tussen atomen inschatten. In de afgelopen jaren hebben nieuwe AI-systemen, zogenaamde diffusie-gebaseerde co-foldingmodellen—zoals AlphaFold3 en Boltz—echter geleerd van enorme aantallen bekende eiwit–molecuulstructuren. Deze systemen kunnen nu ‘voorstellen’ hoe een eiwit en een potentiëel geneesmiddel zich driedimensionaal samen vouwen, zelfs als er geen experimentele structuur beschikbaar is. De centrale vraag die de auteurs behandelen is of deze AI-hulpmiddelen meer kunnen dan plausibele plaatjes tekenen—kunnen ze ook goede geneesmiddelen onderscheiden van slechte?
Echte binders versus pretendenten
Het team testte eerst 16 goed bestudeerde eiwitten plus een complexer bacterieel enzym genaamd DNA-gyrase. Voor elk eiwit vroegen ze de AI-modellen zowel bekende actieve remmers als een reeks niet-gerelateerde “off-target”-moleculen in dezelfde bindingsplaats te plaatsen. In plaats van op één voorspelling te vertrouwen, keken ze hoe consistent de AI elk molecuul bij vele runs plaatste. Werkelijke remmers keerden vaak keer op keer terug naar dezelfde plek en oriëntatie, waarbij ze binnen een paar biljoensten van een meter van elkaar clusterden. Inactieve moleculen zwierven wijder rond en zaten vaak verder van het zakje. Dit eenvoudige idee—poseconvergentie—bleek een sterk signaal te zijn dat een verbinding echt op zijn eiwitdoel past.
Docking veranderen in één-tegen-één competitie
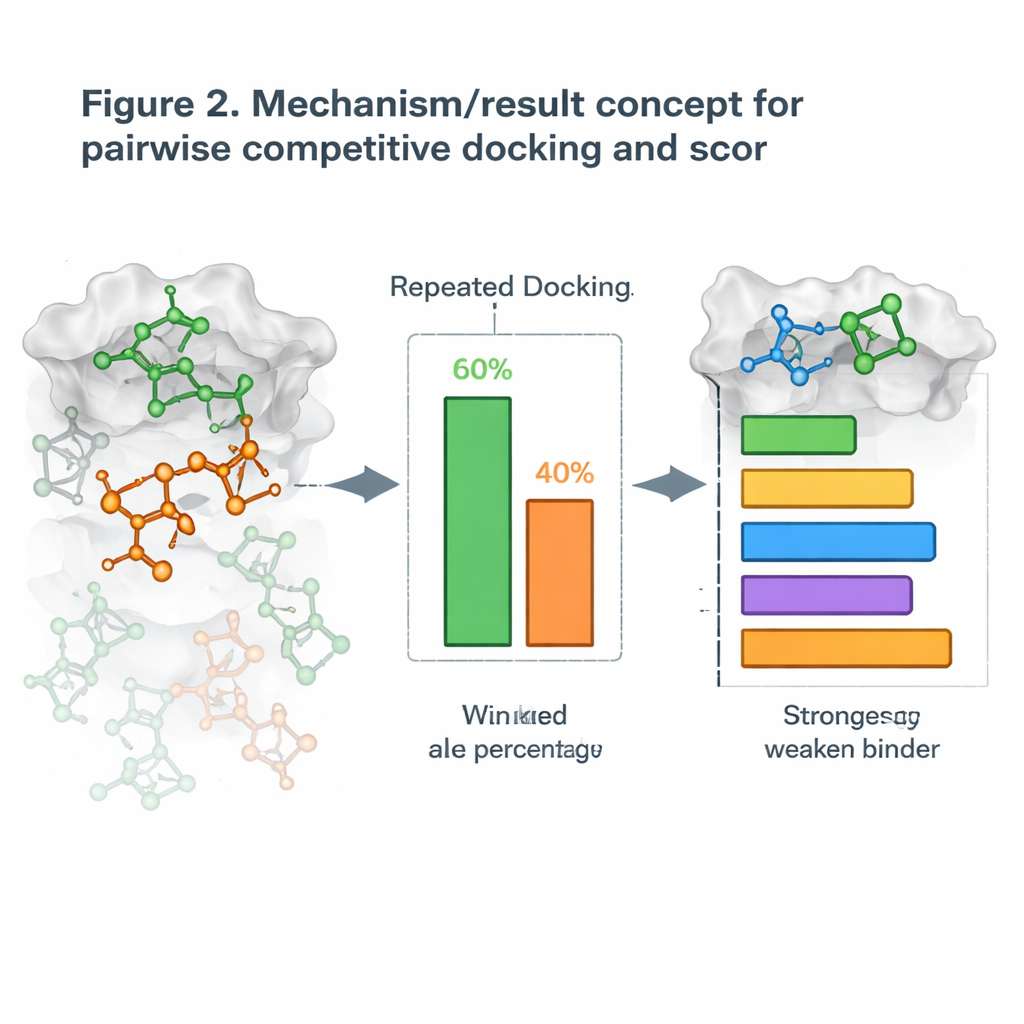
Daarop voortbouwend introduceerden de auteurs een nieuwe strategie die zij pairwise competitive docking noemen. In plaats van één molecuul tegelijk te docken, docken ze twee kandidaten samen met het eiwit en laten ze ze “strijden” om hetzelfde zakje. Na vele herhaalde runs wordt het molecuul dat het domein vaker inneemt uitgeroepen tot winnaar van die confrontatie. Door alle mogelijke paringen uit te voeren, bouwen ze een winst–verlies tabel en berekenen ze een Competitive Docking Score voor elk molecuul, vergelijkbaar met het rangschikken van spelers in een round-robin toernooi. Wanneer deze scores werden vergeleken met metingen uit de echte wereld van hoe sterk de moleculen hun doelen blokkeren, kwamen de ranglijsten vaak goed overeen, waarbij sommige eiwitsystemen bijna perfecte overeenstemming lieten zien.
Van virtuele screenings naar het ontwerpen van betere antibiotica
DNA-gyrase, een essentieel enzym voor bacteriën, diende als een gedetailleerd testcase. Dit eiwit heeft verschillende medicinale zakjes die door verschillende klassen antibiotica worden gericht, waaronder veelgebruikte fluoroquinolonen. De AI-modellen konden doorgaans elke medicijnklasse in het juiste zakje plaatsen, en de competitieve docking-scores volgden ruwweg hun gemeten potenties. De auteurs schaalden vervolgens op naar een virtuele screening van meer dan 3.000 goedgekeurde medicijnen en vroegen welke moleculen het beste concurreerden voor de fluoroquinolonplaats. Hun tweestapsstrategie—eerst met “alles-tegelijk” competitie waarschijnlijke winnaars selecteren en daarna filteren op hoe strak ze in het zakje clusterden—verrijkte de echte fluoroquinolonen sterk en verwierp zwakkere kandidaten. Ten slotte gebruikten ze een AI-gedreven molecuulgenerator om nieuwe fluoroquinolonachtige structuren voor te stellen en pasten competitieve docking toe om een handvol te vinden met zelfs betere voorspelde binding en acceptabele geneesmiddelachtige eigenschappen.
Belofte, grenzen en wat het voor patiënten betekent
De studie laat zien dat moderne AI-modellen meer kunnen dan plausibele eiwit–medicijnstructuren tekenen: wanneer ze in een competitief kader worden uitgevoerd, kunnen ze helpen verbindingen te rangschikken op een manier die vaak experimentele gegevens weerspiegelt. Dit vervangt het labwerk niet—de prestaties hangen nog steeds sterk af van het specifieke eiwit, sommige zakjes worden verkeerd voorspeld en AI-modellen kunnen falen bij zeer grote of ongewone moleculen. Maar naarmate deze modellen en hun trainingsgegevens verbeteren, zouden benaderingen als pairwise competitive docking de vroege fase van geneesmiddelenontdekking veel efficiënter kunnen maken. Voor patiënten zou dat uiteindelijk kunnen leiden tot snellere ontwikkeling van gerichte medicijnen, inclusief nieuwe antibiotica die gelijke tred houden met resistentiële bacteriën.
Bronvermelding: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
Trefwoorden: AI geneesmiddelenontdekking, virtuele screening, moleculaire docking, eiwit-ligand binding, antibioticumontwerp