Clear Sky Science · nl
Ontwikkeling van een protocol om spontane in vitro-activatie van intestinale fibroblasten tegen te gaan met design of experiments
Waarom het belangrijk is om herstelcellen van de darm rustig te houden
Bij chronische darmaandoeningen zoals de ziekte van Crohn kan littekenweefsel de darm langzaam vernauwen totdat voedsel nauwelijks nog passeert, wat vaak tot een operatie leidt. Deze littekenvorming, fibrose genoemd, wordt aangedreven door steuncellen die fibroblasten heten en overactief raken en te veel bindweefsel aanleggen. Om dit proces te begrijpen en op den duur te voorkomen, vertrouwen wetenschappers op in het laboratorium gekweekte fibroblasten. Er is echter een probleem: de eenvoudige kunststofkuipjes die in de meeste laboratoria worden gebruikt, zetten deze cellen al op zichzelf in een onnatuurlijk geactiveerde staat, waardoor het moeilijk is de eerste stappen te bestuderen die leiden van een gezonde naar een fibrotische darm.
Wanneer de kweekschotel het verkeerde signaal afgeeft
De auteurs lieten eerst zien hoe snel intestinale fibroblasten op standaard tissue-culture plastic geprikkeld raken. Binnen slechts 24 uur schakelden zowel een gevestigde cellijn als primaire cellen van mannelijke en vrouwelijke donoren van een rustige naar een geactiveerde, spierachtige vorm. Ze produceerden hoge niveaus van eiwitten die geassocieerd zijn met contractie en littekenvorming, zoals α-smooth muscle actin en fibroblast activation protein, zelfs zonder extra inflammatoire triggers. Dit betekent dat veel bestaande labmodellen mogelijk beginnen vanuit een toestand die al lijkt op een laatstadium van de ziekte in plaats van op vroege, omkeerbare veranderingen.
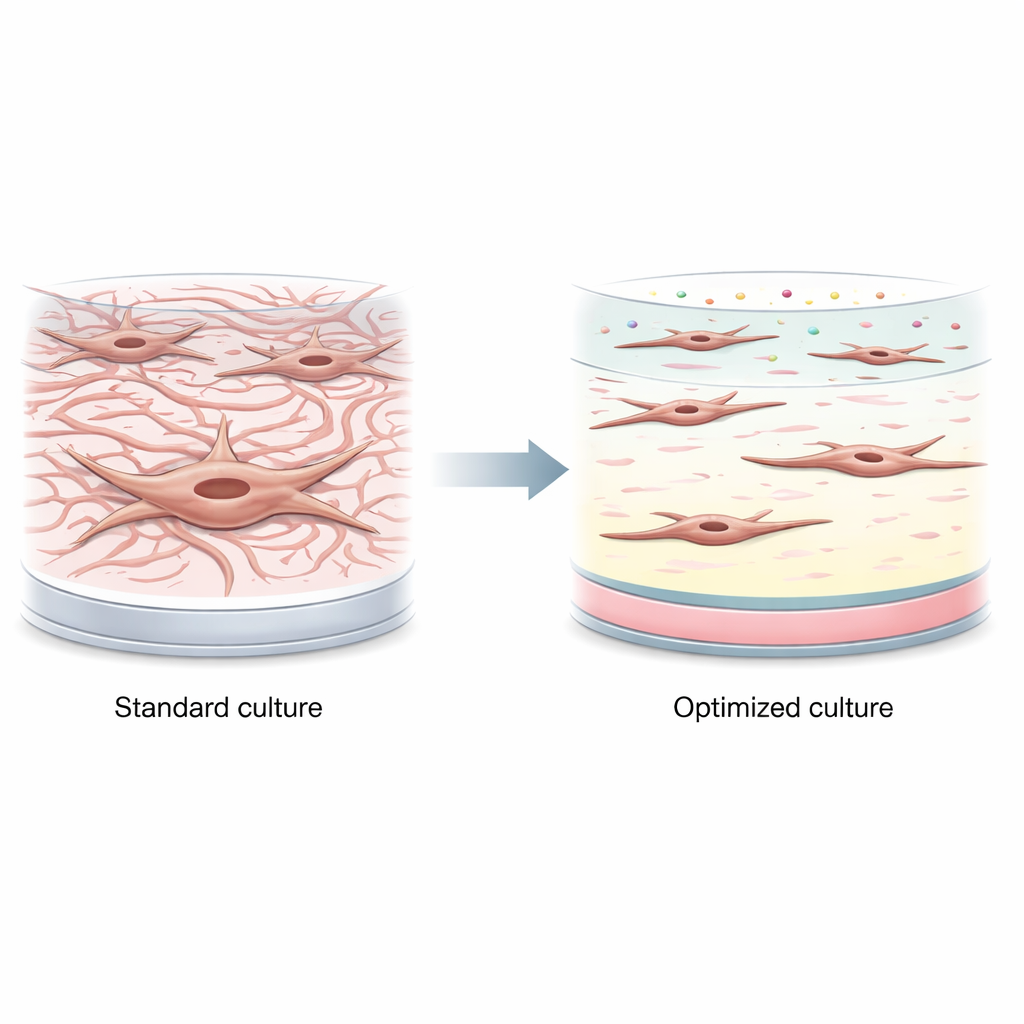
Het testen van losse ingrediënten is niet genoeg
Om de cellen weer tot rust te brengen, onderzocht het team componenten van de natuurlijke omgeving van fibroblasten in de darm, waaronder belangrijke matrixeiwitten (collageen type I en III, en laminine) en oplosbare factoren (vitamine D en basaal fibroblast groeifactor, of FGF). Ze probeerden deze één voor één, als oppervlaktecoatings of als toevoegingen aan het kweekmedium. Sommige condities drukten activatiemarkers omlaag: bijvoorbeeld, matige doseringen vitamine D verlaagden een belangrijke littekenmarker meerdere malen, en bepaalde coatingdichtheden hadden milde effecten. Maar deze voordelen werden tenietgedaan door problemen zoals verminderde celdoorleving bij hogere vitamine D-niveaus, en in het algemeen hielden de enkele aanpassingen de fibroblasten niet betrouwbaar in een laag-activiteitsstadium.
De statistiek die de mogelijkheden afzoekt
In plaats van één draaiknop tegelijk te verdraaien, gebruikte het team een formele ‘‘design of experiments’’-benadering om veel combinaties efficiënt te doorzoeken. Ze varieerden vijf inputs—de drie matrixeiwitten plus vitamine D en FGF—over een breed dosisbereik en genereerden 42 zorgvuldig gekozen kweekcondities. Voor elk daarvan maten ze vier uitkomsten die met littekenvorming samenhangen: een belangrijke activatiemarker, secretie van een hoofdmatrixeiwit (fibronectine), celgroei en celdoorleving. Statistische modellen onthulden vervolgens welke factoren, en welke paringen tussen hen, de grootste invloed hadden. Vitamine D bleek een krachtige maar dosisgevoelige speler te zijn die alle uitkomsten beïnvloedde, terwijl FGF geneigd was de activatie te verlagen en celgroei en overleving te ondersteunen. Collageen I, collageen III en laminine bepaalden hoe deze oplosbare signalen werden geïnterpreteerd, waarbij bepaalde combinaties activatie veel sterker dempten dan enig afzonderlijk bestanddeel kon.
Een recept bouwen voor rustige maar gezonde fibroblasten
Met behulp van deze modellen vroeg het team de software condities te identificeren die tegelijkertijd activatiemarkers en matrixproductie zouden verlagen terwijl de cellen leefden, zonder te eisen dat proliferatie laag bleef. Het beste recept combineerde een hoge dichtheid collageen I, lage collageen III en hoge laminine op het kweekoppervlak, samen met middelmatige vitamine D en hoge FGF in het medium. Onder dit protocol bleven fibroblasten slank en spilvormig in plaats van uitgespreid en sterachtig, brachten ze veel lagere niveaus tot expressie van genen en eiwitten die met contractie en fibrose geassocieerd zijn, en scheidden ze veel minder collageen en fibronectine uit. Tegelijkertijd bleef hun levensvatbaarheid net zo hoog als, of beter dan, die van cellen op gewoon plastic. Belangrijk is dat deze effecten niet alleen voor de modelcellijn golden, maar ook voor primaire fibroblasten van zowel mannelijke als vrouwelijke menselijke donoren, wat aantoont dat het protocol robuust is.
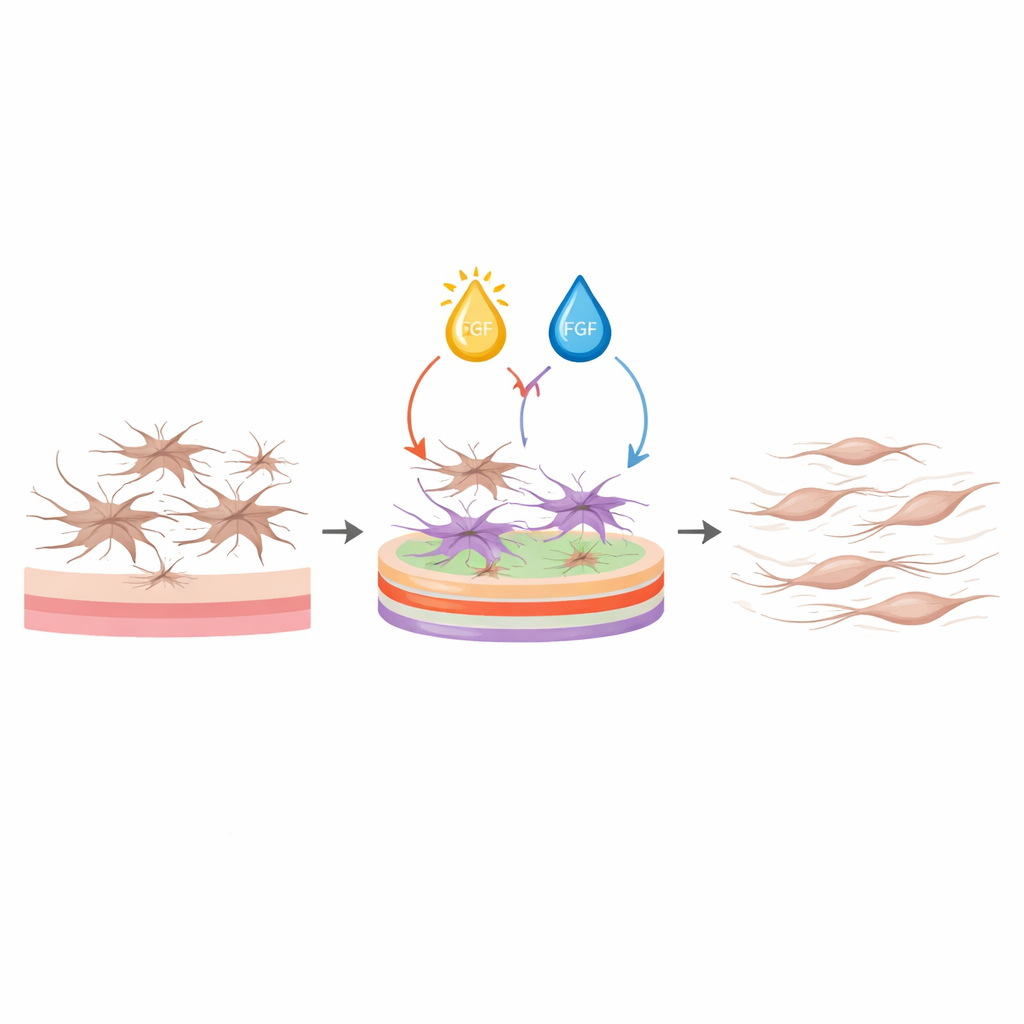
Wat dit betekent voor toekomstig onderzoek naar darmfibrose
Door zorgvuldig de ‘‘buurt’’ rond intestinale fibroblasten af te stemmen—zowel het oppervlak waaraan ze hechten als de factoren die hen omgeven—levert deze studie een rechttoe-rechtaan protocol dat deze cellen in een niet-geactiveerde maar gezonde toestand houdt met standaard laboratoriummaterialen. Voor onderzoekers biedt dit een schone uitgangspositie om specifieke inflammatoire of mechanische signalen toe te voegen en te observeren hoe fibrose begint, in plaats van te werken met cellen die al littekenachtig zijn. Breder gezien toont het werk aan hoe statistisch ontwerp subtiele, niet-intuïtieve combinaties van ingrediënten kan blootleggen die complex celgedrag temmen, en daarmee de weg vrijmaakt voor betere modellen van littekenvorming en uiteindelijk meer gerichte strategieën om darmfibrose te voorkomen of om te keren.
Bronvermelding: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Trefwoorden: darmfibrose, activatie van fibroblasten, celkweekprotocol, vitamine D en FGF, design of experiments