Clear Sky Science · nl
Afleiden van afwijkingen in signaleringsroutes uit histopathologische beelden via een door logica begrensde heterogene gen-pad kennisgrafiek
Verborgen celsignalen zien in kankensneden
Wanneer artsen kanker onder de microscoop bekijken, zien ze voornamelijk vormen en kleuren, niet de complexe moleculaire gesprekken die binnen de cellen plaatsvinden. Toch bepalen die onzichtbare signalerings"gesprekken" tussen genen en paden vaak hoe een tumor groeit en hoe hij op behandelingen kan reageren. Deze studie introduceert een nieuw kunstmatig-intelligentiesysteem dat routinematige pathologiebeelden leest en afleidt welke cellulaire communicatieroutes, ofwel paden, verstoord zijn—waardoor het mogelijk wordt moleculair gedrag te zien zonder extra laboratoriumtests.
Van aanwijzingen per enkel gen naar het grotere geheel
Traditionele benaderingen proberen de status van individuele genen uit weefselbeelden te voorspellen: is een bepaald gen gemuteerd of niet? Dat is nuttig, maar kanker berust zelden op één defect gen. In plaats daarvan werken groepen genen samen om volledige signaleringspaden te ontregelen die groei, overleving en immuniteit reguleren. De auteurs betogen dat concentratie op afzonderlijke genen dit collaboratieve gedrag mist en kan falen in het verklaren waarom tumoren er microscopisch gezien zo uitzien en zich zo gedragen.
Het bouwen van een kaart tussen beelden, genen en paden
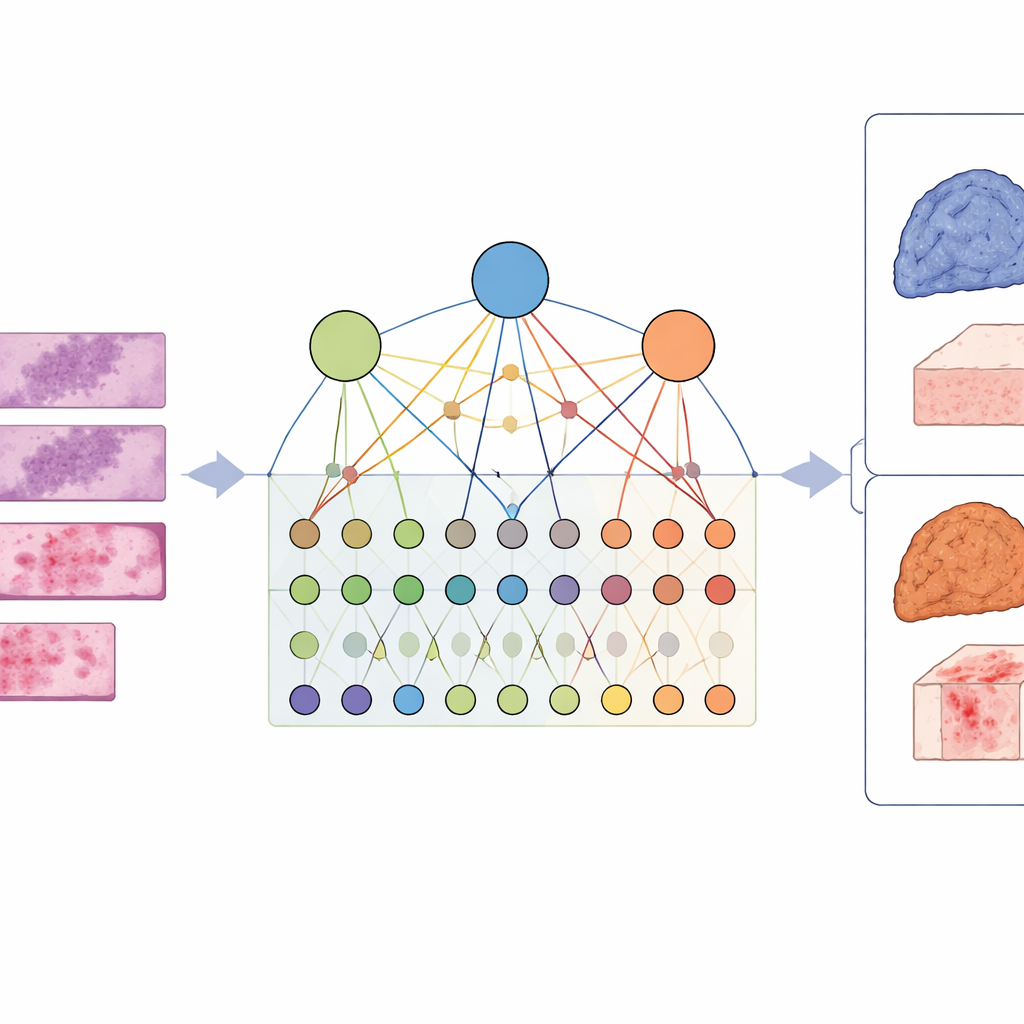
Om deze complexiteit vast te leggen, ontwierpen de onderzoekers een raamwerk genaamd LCG-HGNN dat drie informatielagen koppelt. Ten eerste splitsen ze elke whole-slide-afbeelding van longadenocarcinoom in vele kleine patches en representeren die patches als een graaf, waarbij nabijgelegen of gelijkende regio’s met elkaar verbonden zijn. Ten tweede koppelen ze genmarkers aan signaleringspaden met behulp van gevestigde biologische databanken, en bouwen zo een tweede graaf die encodeert welke genen tot welke paden behoren. Ten slotte laten ze een AI-model informatie door deze gecombineerde graaf laten stromen, zodat beeldpatronen, genen en paden elkaar beïnvloeden in plaats van geïsoleerd te worden behandeld.
Het systeem leren met bekende biologie
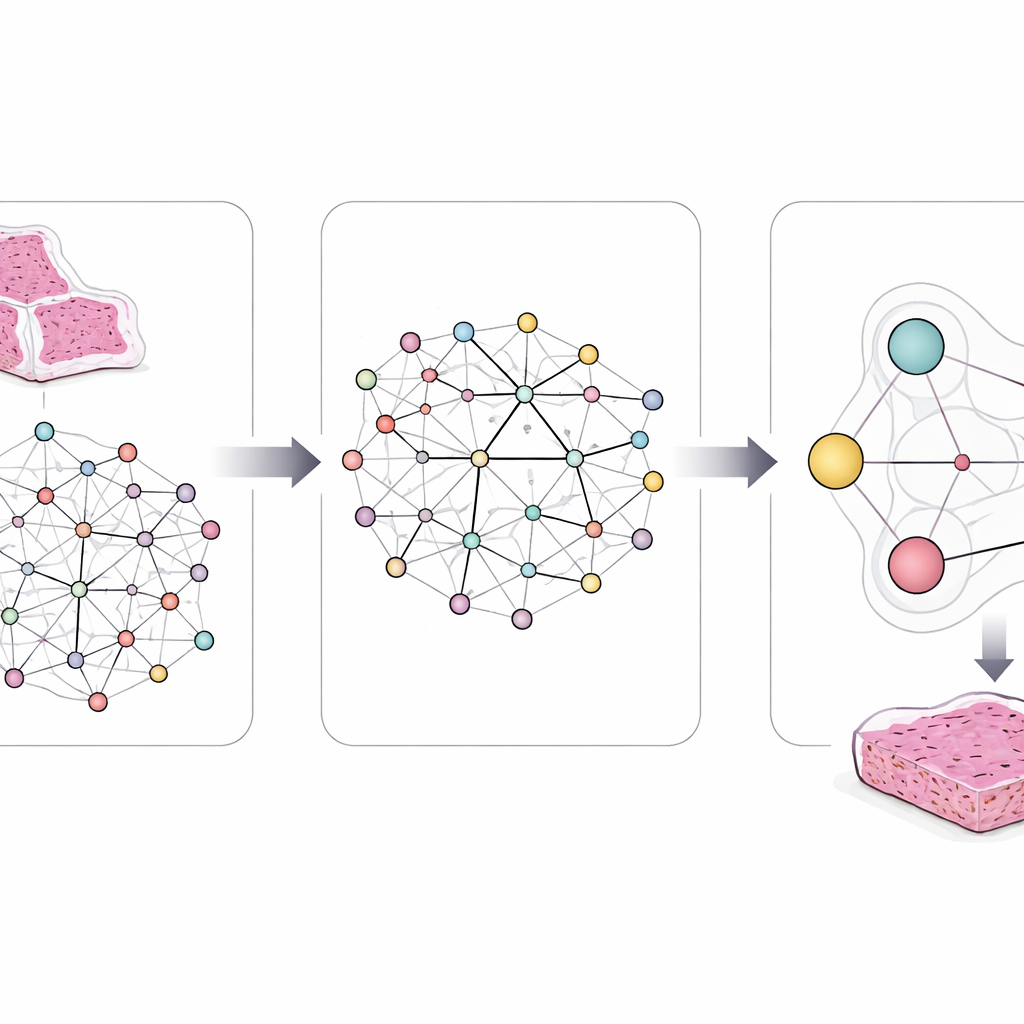
Een belangrijke innovatie is dat het model niet vrij mag leren zonder sturing. De auteurs verwerken duidelijke, regelachtige uitspraken afgeleid van decennia aan kankeronderzoek. Zo komen bepaalde mutaties vrijwel nooit samen in dezelfde tumor voor, en zitten sommige paden stroomop- of stroomafwaarts van anderen. Ze coderen zulke regels als logische beperkingen die de interne verbindingen en voorspellingen van de AI subtiel sturen. Als het model een combinatie van gen- en padveranderingen voorstelt die in strijd is met bekende biologische kennis of met overeenkomsten tussen patiëntenbeelden, duwen deze regels het naar meer realistische alternatieven.
De nauwkeurigheid testen tegenover bestaande methoden
Het team evalueerde hun systeem op meer dan 1.600 longkankersneden gekoppeld aan genetische data. Ze vergeleken het met standaard deep-learningmodellen die zich op individuele genen richten en met meer geavanceerde methoden die veel genen tegelijk verwerken maar de padstructuur negeren. Over meerdere belangrijke paden, waaronder die betrokken bij celgroeisignalen en het ondersteunende weefselraamwerk, voorspelde het nieuwe model veranderingen in genengroepen en padafwijkingen nauwkeuriger. Het produceerde ook image patches waarvan het uiterlijk goed overeenkwam met klinische voorbeelden die met bepaalde mutaties geassocieerd zijn, wat suggereert dat het zich op betekenisvolle microscopische patronen richtte in plaats van op willekeurige beeldartefacten.
Waarom dit belangrijk is voor patiënten
Voor de niet-specialist is de belangrijkste uitkomst dat deze aanpak van een routinematige pathologievrije een rijke bron van moleculair inzicht maakt. In plaats van afzonderlijke, vaak kostbare genetische tests voor elk mogelijk doel te bestellen, zouden artsen uiteindelijk dergelijke modellen kunnen gebruiken om verstoorde paden rechtstreeks uit de beelden die ze al verzamelen te screenen. Hoewel de methode nog grootschaligere, real-world validatie nodig heeft en het genomische onderzoek nog niet vervangt, wijst het op een toekomst waarin de microscoopweergave dubbel dient als een venster op de innerlijke bedrading van de tumor—en zo helpt bij het sturen van preciezere en biologisch onderbouwde kankerzorg.
Bronvermelding: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Trefwoorden: kankerpaden, histopathologie AI, graaf neurale netwerken, longadenocarcinoom, digitale pathologie