Clear Sky Science · nl
Gebruik van in vitro co-cultuurmodellen om bacteriële engineering voor de behandeling van solide tumoren te informeren
Waarom bacteriën bij kanker voor jou van belang kunnen zijn
Behandelingen voor kanker zoals chirurgie, chemotherapie en radiotherapie redden levens maar gaan vaak gepaard met zware bijwerkingen en, te vaak, behandelfalen. Een intrigerend nieuw idee is om levende bacteriën in te zetten als precisie-instrumenten die solide tumoren van binnenuit kunnen opsporen en aanvallen. Dit artikel legt uit hoe wetenschappers laboratoriumtestsystemen opbouwen—waar menselijke cellen en bacteriën samen groeien—om veiligere, slimmere bacteriële therapieën te ontwerpen voordat ze patiënten bereiken.
Kleine helpers die tumoren opzoeken
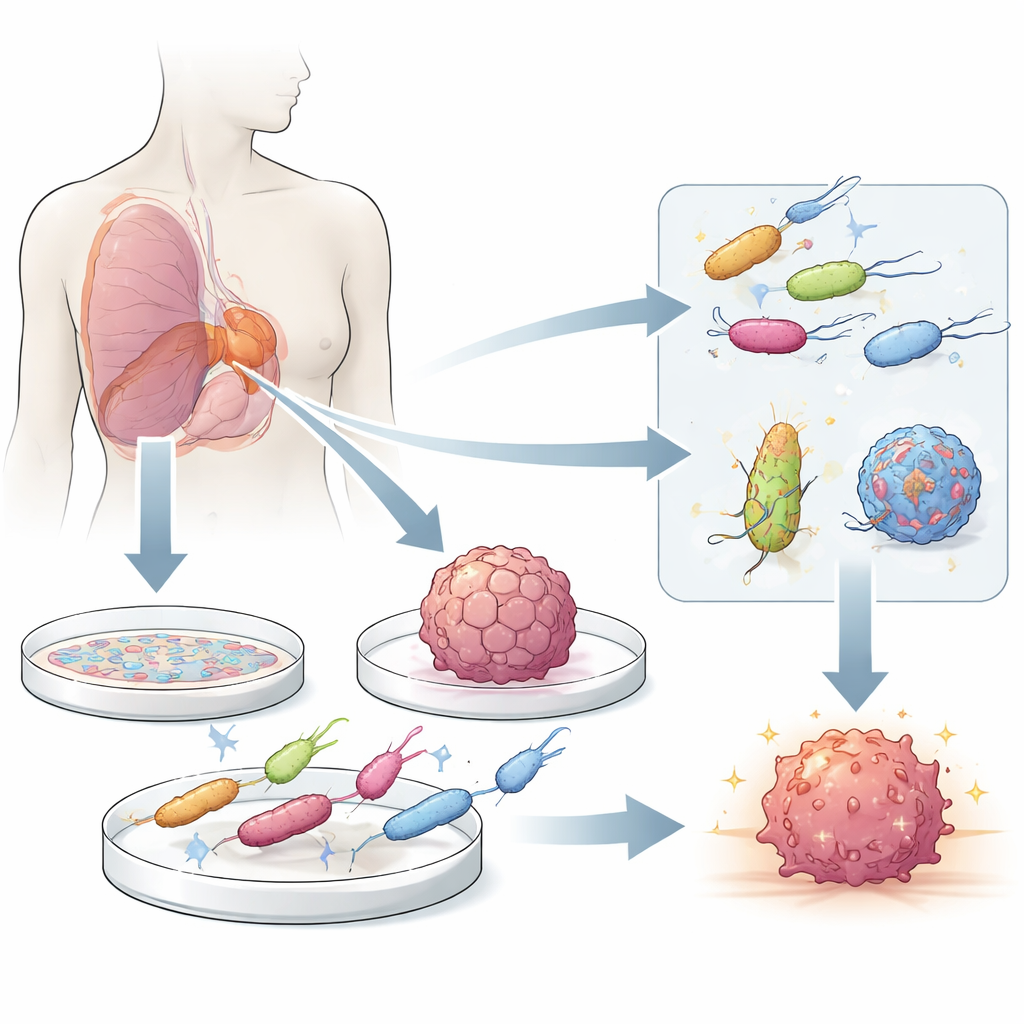
Bepaalde bacteriën geven van nature de voorkeur aan de harde, zuurstofarme omgeving in solide tumoren boven gezonde weefsels. Nadat ze door lekke tumorbloedvaten glippen of met immuuncellen meereizen, bewegen deze microben zich naar dode en stervende cellen in het tumorkerngebied, waar ze kunnen groeien en soms kankerceldood en lokale immuunreacties uitlokken. Moderne genetische engineering verandert deze natuurlijke “tumornavigerende” stammen in levende afleveringsvoertuigen die geneesmiddelen, immuunstimulatoren of andere ladingen precies daar kunnen vrijgeven waar ze het meest nodig zijn, terwijl inspanningen om hun schadelijke eigenschappen te verzwakken de veiligheid verbeteren.
Realistische mini-tumoren in het lab bouwen
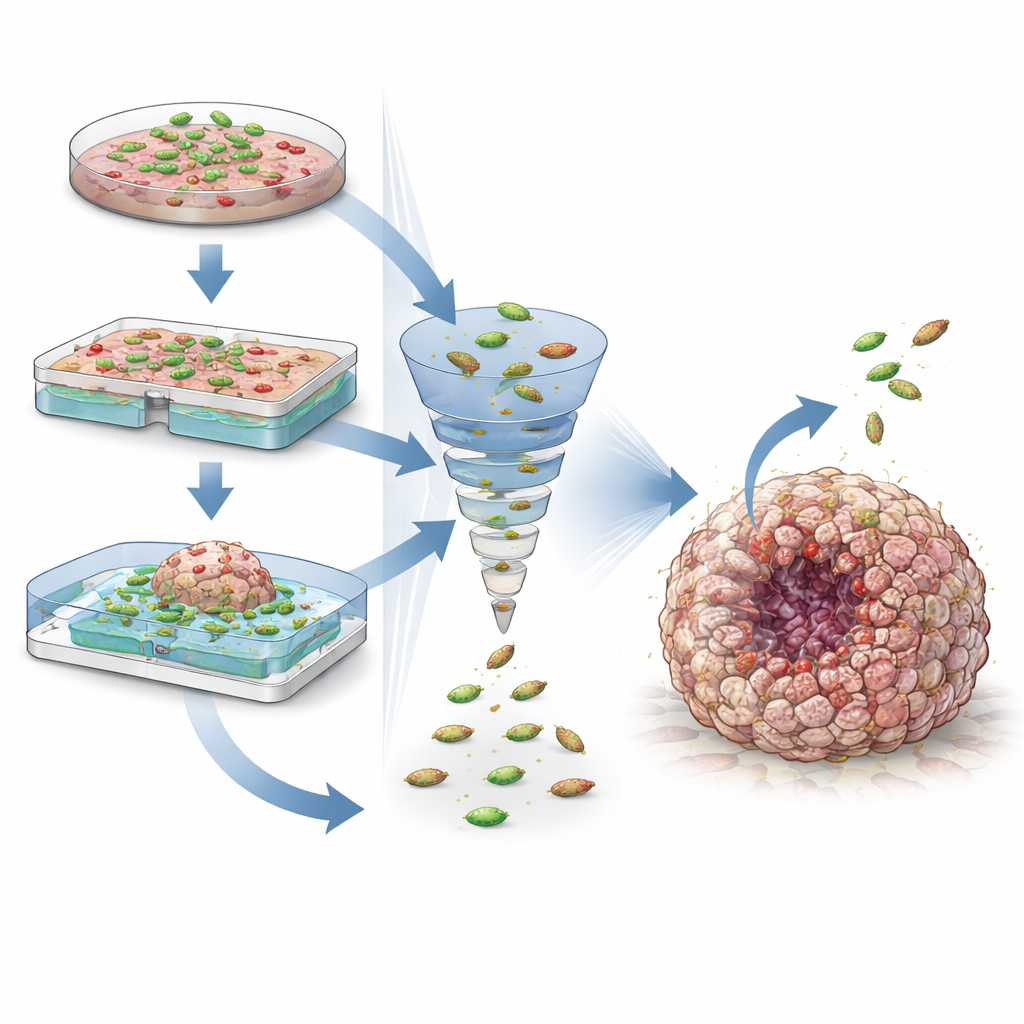
Om deze levende geneesmiddelen te begrijpen en te verbeteren, hebben wetenschappers testbanken nodig die zo dicht mogelijk bij wat in het menselijk lichaam gebeurt komen. Eenvoudige platte cellagen zijn gemakkelijk te kweken en nuttig voor snelle screenings, maar missen de complexe structuur en zuurstofgradiënten van echte tumoren. Drie-dimensionale modellen, zoals sferoïden gemaakt van kankercellijnen en organoïden gekweekt uit patiëntweefsel, reproduceren beter kernkenmerken zoals een levende buitenlaag, een stille binnenzone en een dode kern. Wanneer bacteriën direct met deze mini-tumoren worden gemengd, kunnen onderzoekers zien hoe ze binnendringen, waar ze ophopen en hoe goed ontworpen geneesmiddencircuits werken onder omstandigheden die lijken op die van de tumor van een patiënt.
Cellen scheiden om signalen te bestuderen
Andere co-cultuurontwerpen richten zich minder op fysiek contact en meer op de onzichtbare chemische uitwisselingen tussen bacteriën en menselijke cellen. In transwell-systemen verdeelt een poreus membraan twee kamers zodat kleine moleculen erdoorheen kunnen passen terwijl cellen op hun plaats blijven. Dit stelt wetenschappers in staat te testen, bijvoorbeeld, hoe een bacteriestam een onschuldig verbinding heeft omgezet in een tumor-dodend gas dat doorsijpelde naar naburige kankercellen. Microfluïdische chips—kleine apparaten met kanalen en compartimenten—voegen een extra laag realisme toe. Ze kunnen de stroming van vloeistoffen, zuurstofniveaus en timing regelen, waardoor gekweekte bacteriën kunnen groeien, in gesynchroniseerde cycli kunnen barsten en herhaaldelijk kankercellen kunnen doordrenken met therapeutische moleculen, terwijl nauwkeurig wordt gevolgd hoe beide partners in de loop van de tijd reageren.
In het tumorecosysteem kijken
Co-cultuurmodellen worden ook gebruikt om te bestuderen hoe bacteriën interageren met het bredere tumorecosysteem. Organoïden afgeleid van individuele patiënten kunnen veel van de genetische eigenaardigheden en geneesmiddelreacties van hun oorspronkelijke tumoren behouden, wat de deur opent naar gepersonaliseerde tests van bacteriële therapieën. Het toevoegen van immuuncellen aan deze kulturen onthult hoe bacteriën de antikankerimmuniteit kunnen versterken of onderdrukken en hoe ze mogelijk gecombineerd kunnen worden met checkpointremmers. Tegelijkertijd wijzen deze modellen op veiligheidszorgen, zoals bacteriële toxines die DNA beschadigen en mogelijk bijdragen aan het ontstaan van kanker. Door kweekomstandigheden, zuurstofniveaus en meetmethoden aan te passen—van live-imaging tot DNA-sequencing—kunnen onderzoekers systematisch deze voordelen en risico’s verkennen.
Van laboratoriumbank naar patiëntenbed
Ondanks veelbelovende resultaten in diermodellen hebben maar weinig bacteriële kankertherapieën duidelijke voordelen in menselijke onderzoeken aangetoond. De auteurs stellen dat slimmer gebruik van co-cultuur systemen deze kloof kan overbruggen. Door beter patiënt-tot-patiëntverschillen, tumorcomplexiteit en eerdere behandelingen vast te leggen, kunnen deze modellen identificeren welke gemodificeerde stammen het meest veelbelovend zijn, hoe ze gecombineerd kunnen worden met bestaande middelen en waar ze mogelijk falen. Ze benadrukken ook de noodzaak van gedeelde standaarden zodat laboratoria wereldwijd resultaten kunnen vergelijken en toezichthouders veiliger en effectiever kunnen beoordelen. In eenvoudige bewoordingen bieden zorgvuldig ontworpen labmini-tumoren, gekweekt naast bacteriën, een krachtig middel om deze “slimme beestjes” te verfijnen en zo de kans te vergroten dat toekomstige patiënten bacteriële therapieën ontvangen die zowel veiliger als effectiever zijn.
Bronvermelding: Foschini, S., Wright, J.A., Woods, S.L. et al. Use of in vitro co-culture models to inform bacterial engineering for the treatment of solid tumours. npj Biomed. Innov. 3, 21 (2026). https://doi.org/10.1038/s44385-026-00075-9
Trefwoorden: bacteriële kankertherapie, tumororganoïden, co-cultuurmodellen, synthese-biologie, tumormicro-omgeving