Clear Sky Science · nl
3D-biogefabriceerde in vitro‑modellen als nieuwe benaderingsmethoden voor alternatieven voor dierproeven
Het opnieuw bedenken van hoe we nieuwe medicijnen testen
Bijna een eeuw lang werden de meeste nieuwe geneesmiddelen eerst op dieren getest voordat ze in menselijke proeven kwamen. Toch falen meer dan 9 van de 10 geneesmiddelkandidaten die in dieren veilig lijken, nog steeds bij mensen. Dit artikel onderzoekt hoe een nieuwe generatie 3D‑"biogedrukte" menselijke weefsels dat verhaal kan veranderen—door nauwkeurigere, menswaardige manieren te bieden om te voorspellen hoe ons lichaam op medicijnen reageert, en mogelijk veilige behandelingen sneller naar patiënten te brengen.

Van proefdieren naar mensgerichte testen
Recente Amerikaanse wetgeving, bekend als de FDA Modernization Act 2.0, heeft de automatische verplichting om elk nieuw geneesmiddel op dieren te testen opgeheven. Regulators kunnen nu in plaats daarvan "New Approach Methodologies" accepteren—mensrelevante testsystemen die zijn ontworpen om echte patiëntreacties beter te voorspellen. Daarbij steekt 3D‑bioprinten er bovenuit. Het gebruikt gespecialiseerde printers om levende menselijke cellen en zachte, gelachtige materialen in ingewikkelde vormen te plaatsen die echte weefsels en mini‑organen nabootsen. Het proces begint vaak met medische beelden zoals CT‑ of MRI‑scans, die een blauwdruk leveren. Wetenschappers kiezen vervolgens geschikte biomaterialen, mengen de juiste celtypen tot een printbare "bio‑inkt" en drukken gelaagde of volumetrische structuren die in bioreactoren uitrijpen tot functionele weefselmodellen.
Hoe 3D‑bioprinten levende weefsels opbouwt
Bioprinten is geen enkele technologie maar een familie van methoden. Inkjet‑achtige printers verstuiven kleine druppeltjes celhoudende vloeistof om dunne lagen met fijne details op te bouwen, waardoor ze nuttig zijn voor kleine weefsels zoals huidpatches of longbarrières. Extrusieprinters persen continue strengen van dikkere bio‑inkten, die veel cellen en ondersteunende vezels kunnen bevatten, waardoor grotere, robuustere structuren mogelijk zijn, zoals hartkleppen, levertumormodellen of vaatnetwerken. Een nieuwere klasse, vatfotopolymerisatie genaamd, schijnt gepatterned licht in een vloeistof om complexe vormen te verharden zonder cellen door nozzles te persen. Varianten van deze methode kunnen micron‑schaal kenmerken beeldhouwen, een heel klein orgaan in seconden printen, of zelfs weefsels vormen binnen een transparant bad, terwijl de cellen levend blijven.
Geneesmiddeltests vervangen en verfijnen
Deze geprinte weefsels worden al gebruikt om de geneesmiddelenpipeline te herdenken. In vroege ontdekking laten patiënt‑ of ziekte‑specifieke constructen—zoals biogedrukte tumormodellen—onderzoekers veel kandidaat‑middelen testen in realistische 3D‑omgevingen die menselijke ziekten beter nabootsen dan platte cellagen op een schaal. In preklinische testen blijken geprinte huid-, long‑ en leverweefsels nauwkeuriger te zijn dan dieren voor het opsporen van mensspecifieke toxiciteit of bijwerkingen. Sommige studies gaan verder door "klinische proeven op een chip" te printen, waarbij weefsels gemaakt van cellen van verschillende donoren parallel aan een geneesmiddel worden blootgesteld, waardoor zichtbaar wordt wie baat kan hebben of schade kan ondervinden. Regulatoren moedigen bedrijven nu aan om gegevens uit deze modellen naast dierstudies in te dienen, en zo het bewijs op te bouwen dat nodig is voor bredere acceptatie.
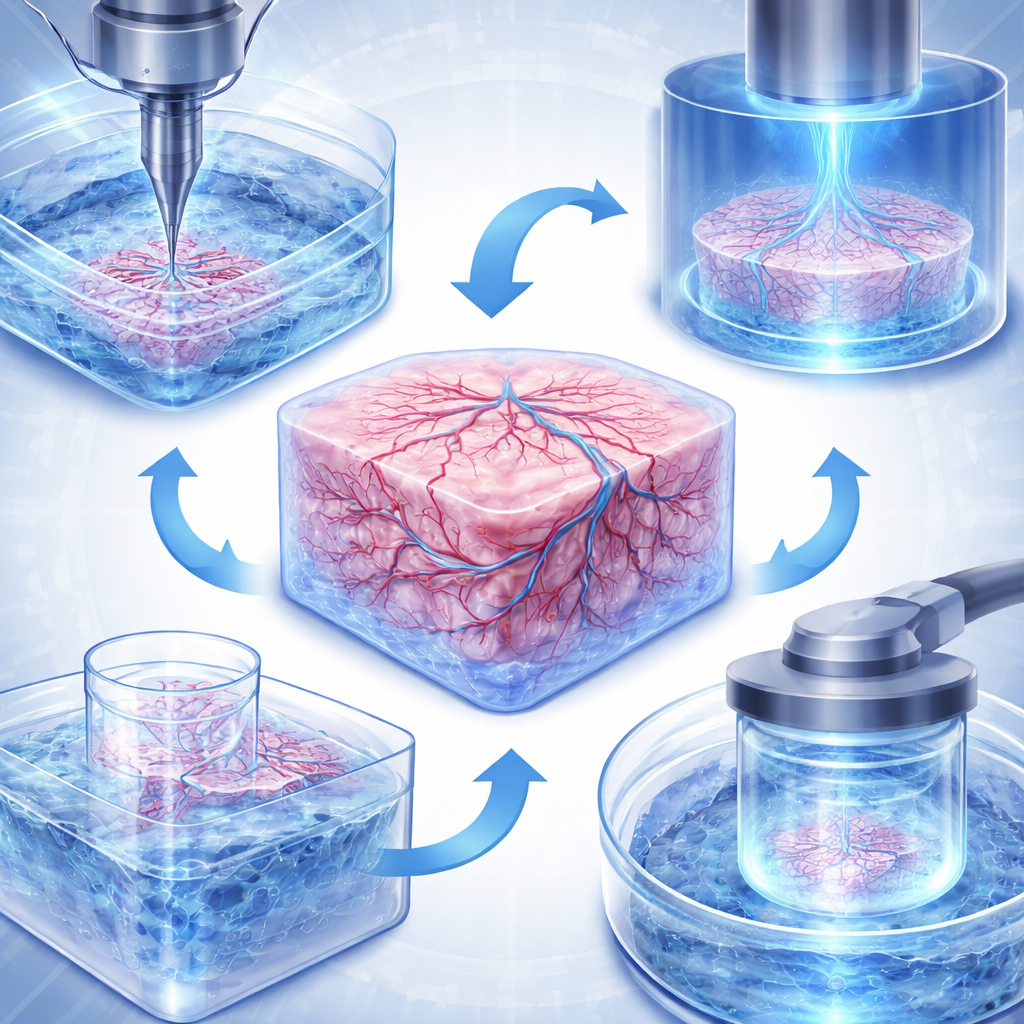
Organen ontwerpen zonder lichaam
Ondanks snelle vooruitgang blijven er meerdere obstakels voordat biogedrukte weefsels routinematig dierproeven kunnen vervangen. Een belangrijke uitdaging is de bloedvoorziening: echte organen bevatten vatenstelsels die variëren van grote slagaders tot haarfijne capillairen, terwijl geprinte constructen een natuurlijke limiet moeten overwinnen aan hoe ver zuurstof en voedingsstoffen kunnen diffunderen. Onderzoekers pakken dit aan met nieuwe printstrategieën die vertakkende kanalen creëren, met ondersteuningsbaden die zachte weefsels op hun plaats houden terwijl kleine vaten worden gevormd, en met razendsnelle volumetrische printers die dikke, celrijke structuren maken voordat cellen beginnen te lijden. Een andere uitdaging is realisme: levende weefsels bestaan uit mengsels van veel celtypen die worden omgeven door complexe chemische signalen en vaak worden beïnvloed door het microbioom en verre organen. Geavanceerde modellen combineren nu meerdere celpopulaties, gecontroleerde concentratiegradiënten van zuurstof en pH, en zelfs gekoppelde "multi‑orgaan"‑systemen die darm-, lever-, immuun‑ en hersenweefsels via stromende vloeistof verbinden om reacties van het hele lichaam na te bootsen.
Een menswaardige, predictieve toekomst voor geneesmiddelenontwikkeling
Alles bij elkaar suggereren deze ontwikkelingen een toekomst waarin hoog‑fideliteits, mensgebaseerde weefselmodellen centraal komen te staan in de evaluatie van geneesmiddelen. Het artikel concludeert dat 3D‑bioprinten zich ontwikkelt van een niche laboratoriumtechniek tot een kerninstrument voor het bouwen van gestandaardiseerde, regulator‑klare testsystemen. Om deze belofte volledig waar te maken, moeten wetenschappers en toezichthouders overeenkomen waar en hoe deze modellen moeten worden gebruikt, aantonen dat ze betrouwbaar menselijke uitkomsten voorspellen, en de resterende technische uitdagingen oplossen zoals het bouwen van stabiele vasculatuur en anatomisch complexe organen. Als dit lukt, kan deze verschuiving de afhankelijkheid van dierproeven verminderen, dure mislukkingen in latere stadia van geneesmiddelenontwikkeling terugdringen en veiligere, effectievere therapieën opleveren die beter de biologie weerspiegelen die het meest telt: die van onszelf.
Bronvermelding: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Trefwoorden: 3D-bioprinten, alternatieven voor dierproeven, geneesmiddelenontwikkeling, weefselmodellen, volumetrisch bioprinten