Clear Sky Science · nl
Macrofagen ontwerpen voor kankerimmunotherapie: opkomende inzichten en therapeutisch potentieel
De schoonmaakploeg van het lichaam ombouwen tot kankerkrijgers
Ons lichaam bevat veel macrofagen—zwerende “schoonmaak”-cellen die ziekteverwekkers en dood weefsel opeten. Dit overzichtsartikel onderzoekt hoe wetenschappers deze cellen leren ombuigen tegen kanker. Omdat macrofagen overvloedig aanwezig zijn in tumoren, ook in die tumoren die bestand zijn tegen de huidige toonaangevende immunotherapieën, kan begrip en engineering van deze cellen nieuwe opties openen voor patiënten met moeilijk behandelbare kankers.
De vele gezichten van één celtype
Macrofagen zijn geen enkel, vast celtype; ze zijn kameleons. Ze kunnen uit de bloedbaan komen of al in weefsels aanwezig zijn, en eenmaal gesetteld reageren ze op lokale signalen. In tumoren kunnen deze tumor-geassocieerde macrofagen ofwel helpen kankercellen te doden of, verwarrend genoeg, tumoren laten groeien en uitzaaien. Eerder probeerden onderzoekers ze in twee vakjes te schuiven—“M1” (aanvalstand) en “M2” (herstel- of ondersteuningsstand). Nieuwe genetische en ruimtelijke kaartwerkinstrumenten laten nu een veel rijker spectrum aan toestanden zien, met meerdere subgroepen en gedragingen die variëren per tumor en locatie. Zelfs cellen die vroeger als duidelijk “pro-tumor” werden gezien, kunnen in bepaalde contexten T-cellen mobiliseren en anti-kankerimmuniteit ondersteunen.
Hun omgeving voelen en kankercellen opeten
Macrofagen luisteren niet alleen naar chemische signalen; ze voelen ook de fysieke wereld om zich heen. Terwijl ze door het dichte eiwitweb van een tumor kruipen, tussen cellen persen en vloeistofkrachten weerstaan, detecteren ze stijfheid en rek via gespecialiseerde receptoren zoals Piezo1. Deze mechanische signalen, samen met klassieke immuunsignalen, kunnen macrofagen richting meer ontstekingsbevorderende of juist meer kalmerende rollen duwen. Functioneel kunnen macrofagen kankercellen insluiten, ze vervolgens afbreken en fragmenten (antigenen) tonen aan T-cellen, waarmee ze het aangeboren en adaptieve immuunsysteem verbinden. Kankercellen verzetten zich door “niet opeten”-signalen te sturen, met name via het oppervlakte-eiwit CD47 dat een rem op macrofagen activeert. Medicijnen die deze interactie blokkeren worden in veel klinische proeven getest; ze vergroten de opruiming van kankercellen maar vereisen zorgvuldige afstemming om gezonde cellen niet te schaden.
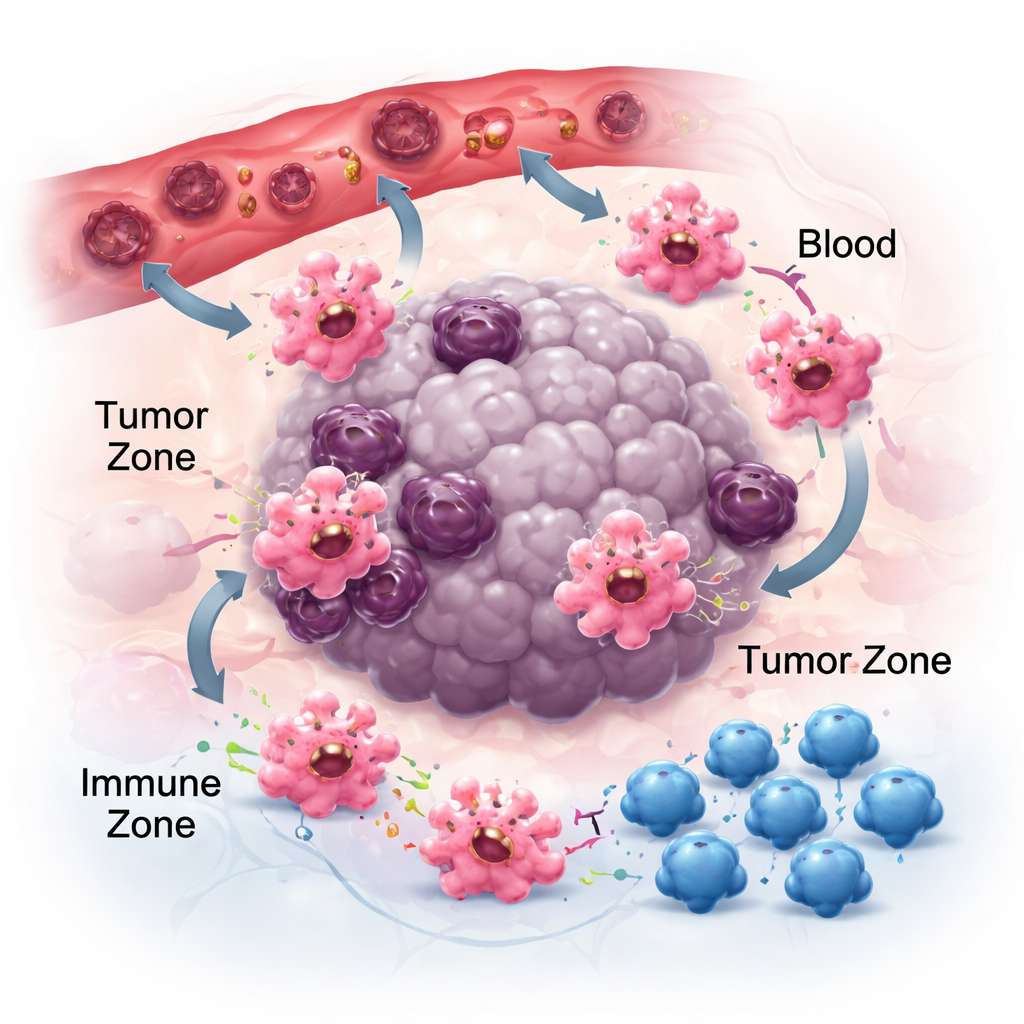
Bewegen, hechten en communiceren in de tumorbuurt
Om van belang te zijn bij kanker moeten macrofagen eerst tumoren bereiken en zich vervolgens in de juiste niches positioneren. Ze volgen chemische sporen—chemokinen en groeifactoren—die door kankercellen en omliggende cellen worden vrijgegeven. Paarvorming zoals CCR2–CCL2 helpt hen naar tumoren te trekken, en medicijnen die deze signalen blokkeren kunnen de opbouw van macrofagen verminderen, zij het niet volledig, wat wijst op andere aantrekkingselementen zoals CSF‑1 en VEGF. Eenmaal op plaats, bepaalt ook hoe macrofagen zich aan de lokale matrix hechten hun gedrag. Hun adhesiereceptoren, integrines genoemd, fungeren niet alleen als lijm; ze versterken ontstekingssignalen en kunnen cellen richting meer tumorbestrijdende toestanden duwen. Tegelijkertijd laten macrofagen kleine pakketjes los, extracellulaire vesikels, die RNA en eiwitten naar naburige cellen vervoeren. Afhankelijk van het tumortype kunnen deze vesikels ofwel de immuniteit dempen en verspreiding helpen, of de anti-tumorrespons versterken, wat het contextafhankelijke karakter van macrofaagcommunicatie benadrukt.
Macrofagen herprogrammeren met genen en materialen
Aangezien macrofagen van nature beter vastzitten in solide tumoren dan veel T-cellen, zetten onderzoekers ze nu om in levende medicijnen. Een genetische strategie leent van chimerische antigeenreceptor (CAR) T-celtherapie: het toevoegen van een synthetische receptor om CAR-macrofagen (CAR‑M) te creëren. Deze ontworpen cellen herkennen tumormarkers, nemen kankercellen efficiënter op, verteren de omringende matrix, geven ontstekingssignalen af en activeren T-cellen door tumorantigenen te presenteren. Vroege humane studies van HER2-gerichte CAR‑M tonen bemoedigende veiligheid en biologische activiteit, hoewel meer werk nodig is om sterke, duurzame voordelen aan te tonen. Parallel daaraan gebruiken niet‑genetische benaderingen deeltjes en “rugzakjes” gemaakt van lipiden of polymeren. Macrofagen kunnen geneesmiddelbeladen nanodeeltjes insluiten en diep in tumoren dragen als Trojaanse paarden, of oppervlakte-aangedragen patches dragen die langzaam immuunstimulerende signalen afgeven, waardoor ze een tumorbestrijdende identiteit behouden zonder hun binnenkant te overbelasten. Ook vesikels afgeleid van macrofagen worden getest als natuurlijke, zellvrije afleveringsvoertuigen.
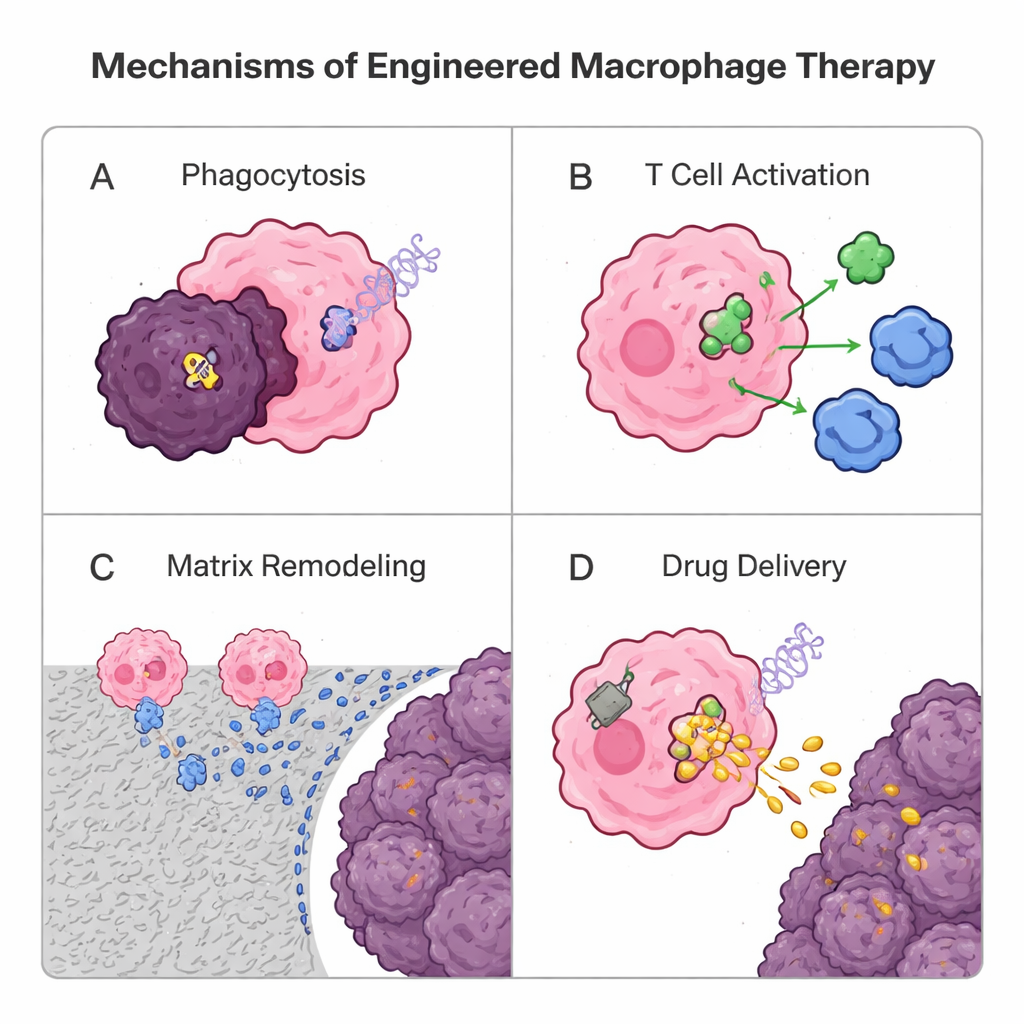
Uitdagingen en redenen voor hoop
Ondanks hun potentieel moeten macrofaagtherapieën praktische hindernissen overwinnen. Het kost tijd en geld om voldoende consistente cellen van patiënten te genereren, en eenmaal geïnfusioneerd leven deze cellen niet of vermenigvuldigen zich niet oneindig. Hun ingebouwde flexibiliteit, biologisch nuttig, kan het moeilijk maken ze verankerd te houden in een anti-tumorstand binnen een complexe, onderdrukkende tumormicro-omgeving. De auteurs betogen dat geavanceerde bio-engineerde modellen—3D-culturen, organoïden en organ-on-a-chip-systemen die echte weefselmechanica nabootsen—cruciaal zullen zijn om te begrijpen en te voorspellen hoe ontworpen macrofagen zich bij patiënten gedragen. Toch suggereert hun natuurlijke vermogen om solide tumoren binnen te dringen, kankercellen op te eten en T-cellen te wekken, gecombineerd met een vroege veiligheidsgeschiedenis, dat macrofaaggebaseerde therapieën een belangrijke nieuwe wapen kunnen worden, vooral tegen “koude” tumoren die momenteel de meeste immuunbehandelingen weerstaan.
Bronvermelding: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Trefwoorden: macrofagen immunotherapie, tumormicro-omgeving, CAR-macrofagen, fagocytose, nanodeeltje geneesmiddellevering