Clear Sky Science · nl
Versnelling van gepersonaliseerde geneeskunde: geminiaturiseerde patiënt-afgeleide organoïde medicijntests om kankerbehandelingsreacties en meer te voorspellen
Het lab sneller naar het bed van de patiënt brengen
Voor veel mensen met gevorderde kanker voelt het wekenlang wachten om te weten of een chemotherapie zal werken als bijzonder pijnlijk. Deze studie onderzoekt een manier om die termijn te verkorten met behulp van kleine, in het laboratorium gekweekte replica’s van iemands tumor—zogenaamde organoïden—om geneesmiddelen van tevoren te testen. Door de testprocedure te verkleinen en te automatiseren, willen de onderzoekers voorspellen welke behandelingen waarschijnlijk helpen, met veel minder weefsel en tijd dan huidige methoden vereisen.
Mini-tumoren in een schaaltje
Patiënt-afgeleide organoïden zijn driedimensionale celclusters gekweekt uit iemands eigen tumor. In tegenstelling tot klassieke platte celculturen behouden deze mini-tumoren veel van de oorspronkelijke genetische diversiteit en het gedrag van de kanker. Eerder werk heeft aangetoond dat wanneer organoïden in het laboratorium op een geneesmiddel reageren—of juist niet reageren—patiënten vaak een vergelijkbare reactie in de kliniek laten zien. Het probleem is dat standaard organoïde-medicijntests honderden organoïden per putje gebruiken, wat veel bioptiemateriaal vereist en weken duurt, waardoor hun praktische toepasbaarheid voor patiënten die snel met een behandeling moeten beginnen beperkt is.
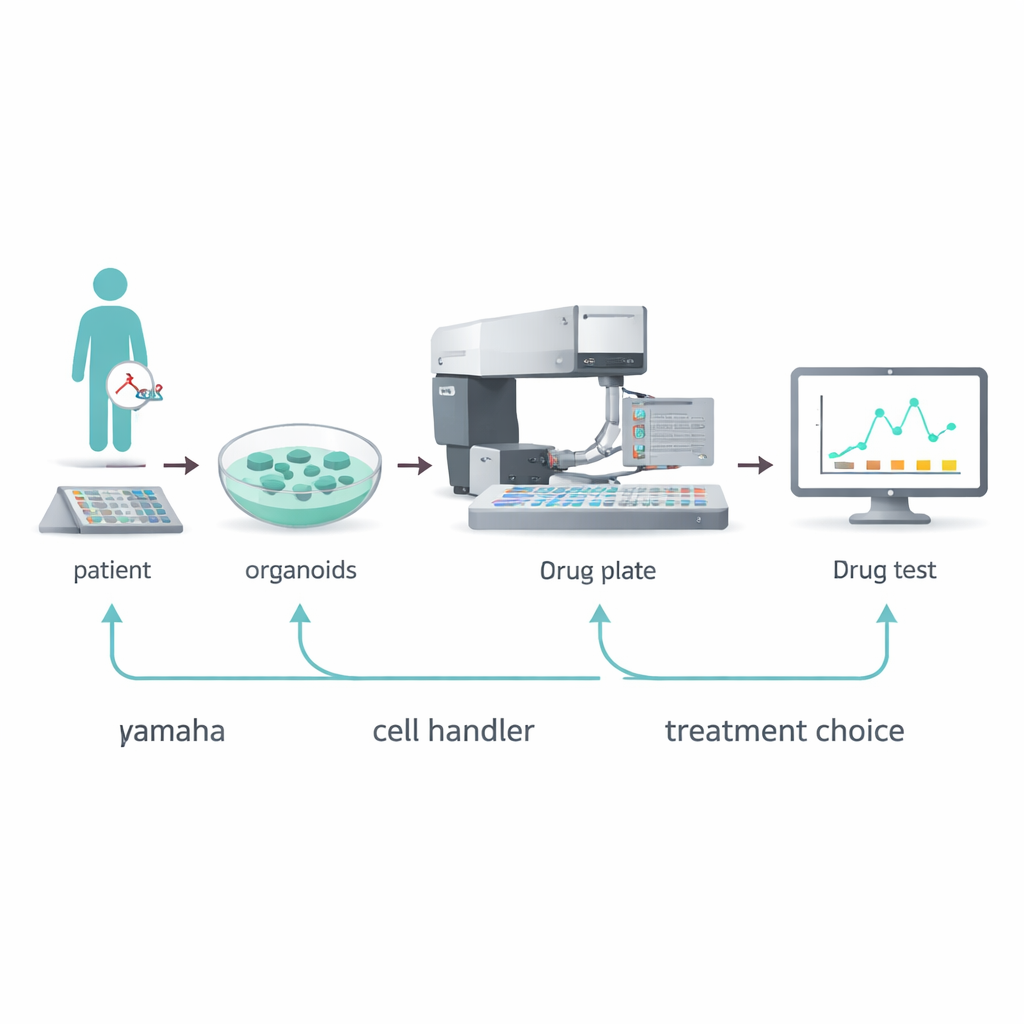
Een robotische picker voor mini-tumoren
Het team wendde zich tot een geautomatiseerd apparaat, de Yamaha Cell Handler, om deze knelpunten aan te pakken. Deze robot gebruikt een camera om individuele organoïden in een bronplaat te detecteren, analyseert hun grootte en vorm, en pakt daarna voorzichtig geselecteerde organoïden op om ze in de kleine putjes van een 384-putjesplaat te deponeren. Door af te stemmen hoeveel organoïden werden gezaaid, hoe ze werden ondersteund in een gelachtige matrix, en welke kleurstoffen en meetmethoden werden gebruikt, stelden de onderzoekers vast dat slechts 5 tot 10 organoïden per putje voldoende waren voor betrouwbare medicijntests. Ze optimaliseerden ook een DNA-gebaseerde fluorescentieassay die rapporteert hoeveel cellen na blootstelling aan een medicijn nog leven, waarmee sommige nadelen van oudere energiegebaseerde tests werden vermeden.
Meer doen met veel minder cellen
Na optimalisatie gebruikte het geminiaturiseerde systeem zo weinig als 0,5% tot ongeveer 5% van het materiaal dat voor conventionele schermen nodig is, waardoor de behoefte aan organoïden met een factor 25 verminderde. Ondanks de ingrijpende verkleining kwamen de patronen van medicijngevoeligheid die werden gemeten met 10 organoïden per putje goed overeen met die bij 250 organoïden per putje. Het platform kon zelfs verborgen verschillen binnen het tumormodel van één patiënt onthullen, zoals subgroepen organoïden die gevoelig of resistent waren voor een veelgebruikte chemotherapie. In een voorbeeld met een gerichte antilichaamtherapie gedroegen organoïden uit tumoren met een bekende resistentiemutatie zich zoals verwacht—ze reageerden niet—terwijl organoïden zonder die mutatie sterk werden geremd, zowel in de standaard- als in de geminiaturiseerde opzet.
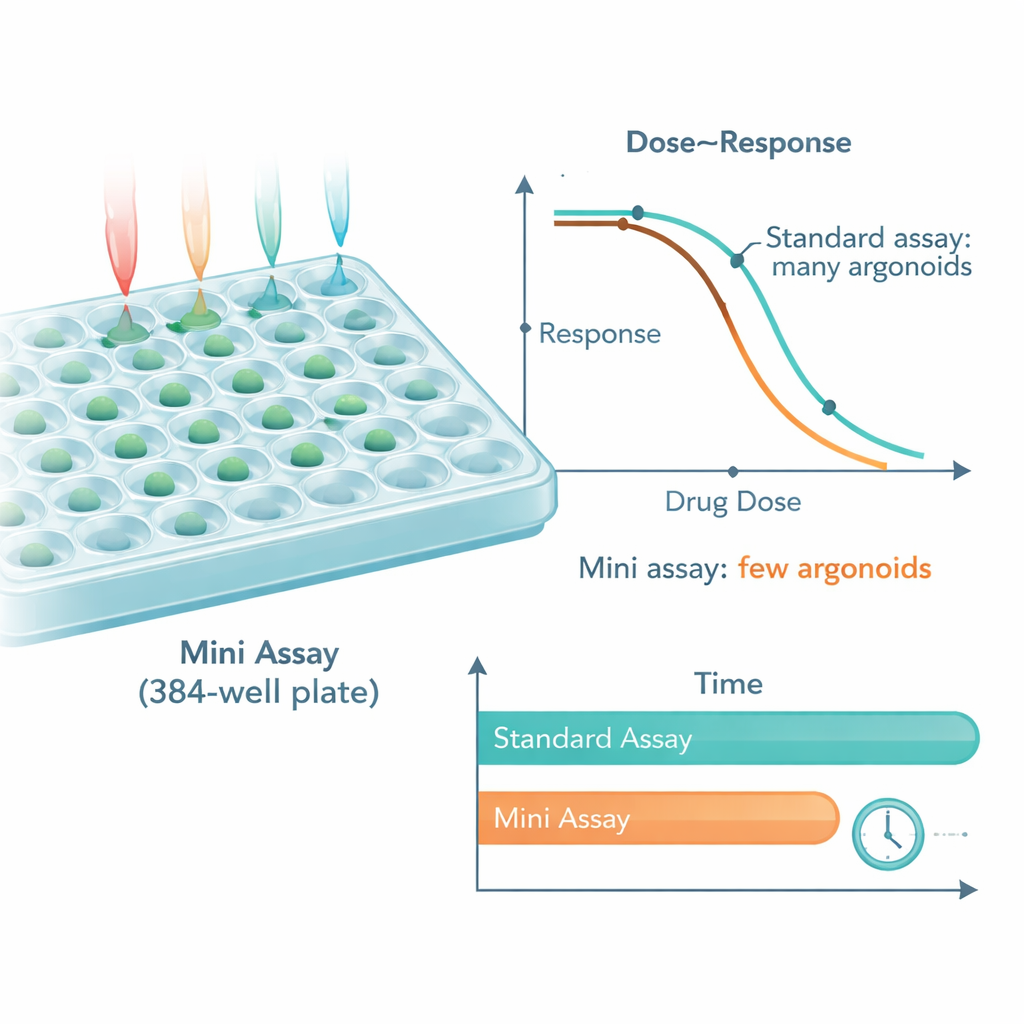
Van laboratoriumsignalen naar patiëntuitkomsten
De onderzoekers vroegen zich vervolgens af of deze zuinigere assay nog steeds echte patiëntervaringen weerspiegelde. Ze testten organoïden van mensen met gemetastaseerde dikkedarmkanker die in de kliniek standaardchemotherapie hadden gekregen. Zowel voor 5-fluorouracil als oxaliplatine kwamen de medicijnreacties gemeten in de geminiaturiseerde assays (met slechts 5–10 organoïden per putje en minder medicijnconcentraties) sterk overeen met de resultaten uit grotere, traditionele schermen. Belangrijker voor patiënten was dat de gevoeligheid van organoïden in de mini-assay correleerde met hoe lang de kanker van mensen onder controle bleef en in veel gevallen met de totale overleving. Het verminderen van het aantal organoïden verzwakte deze verbanden niet, wat suggereert dat de gestroomlijnde benadering klinisch informatief blijft.
Wat dit voor patiënten kan betekenen
Door te bewijzen dat nauwkeurige medicijn-responstests mogelijk zijn met veel minder organoïden en een snellere workflow, brengt deze studie organoïde-gebaseerde precisiegeneeskunde dichter bij routinematige klinische toepassing. Het nieuwe geautomatiseerde platform halveert zowel het aantal benodigde cellen als de doorlooptijd ongeveer, waardoor het realistischer wordt om organoïden uit een biopt te laten groeien, meerdere therapieën te testen en resultaten terug te geven in de tijd die nodig is om behandelbeslissingen te sturen. Hoewel verdere validatie over meer kankertypen nodig is, biedt deze geminiaturiseerde organoïde-screensstrategie een praktische route naar het kiezen van kankergeneesmiddelen op basis van hoe de tumor van een individu zich in het lab gedraagt, in plaats van alleen op populatiegemiddelden te vertrouwen.
Bronvermelding: Abouleila, Y., Smabers, L.P., Voskuilen, T. et al. Accelerating personalized medicine: miniaturized patient-derived organoid drug screening for predicting cancer treatment responses and beyond. npj Biomed. Innov. 3, 16 (2026). https://doi.org/10.1038/s44385-026-00067-9
Trefwoorden: kankerorganoïden, gepersonaliseerde geneeskunde, medicijntests, dikkedarmkanker, automatisering in oncologie