Clear Sky Science · nl
Het optimaliseren van de inductie van ontsteking in darmepitheliale organoïden afgeleid van te vroeg geboren zuigelingen
Waarom dit belangrijk is voor kwetsbare pasgeborenen
Bij vroeggeboren baby’s komt een gevaarlijke combinatie voor: een onrijpe darm en een snel veranderende gemeenschap van microben. Samen kunnen die een ongeremde ontstekingsreactie opwekken die de darm beschadigt en leidt tot levensbedreigende aandoeningen zoals necrotiserende enterocolitis. Omdat we niet rechtstreeks op te vroeg geboren zuigelingen kunnen experimenteren, hebben onderzoekers realistische labmodellen van hun darmen nodig om te testen wat ontsteking veroorzaakt en hoe die te stoppen. Deze studie verfijnt zo’n model met klein in het laboratorium gekweekt darmslijmvlies en biedt een duidelijker manier om te onderzoeken welke microbiële signalen de balans doen omslaan van normale afweer naar schadelijke ontsteking.
Een te vroeg geboren darm in het laboratorium kweken
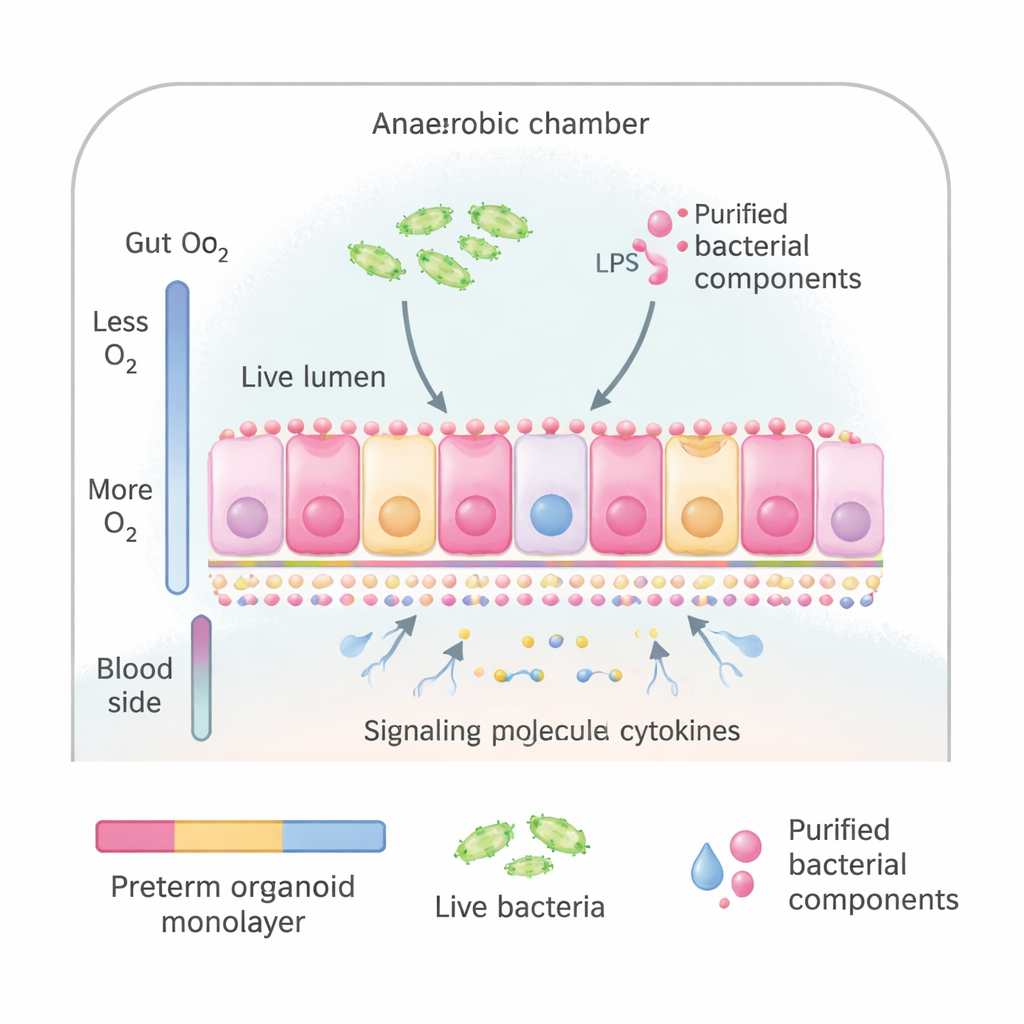
De onderzoekers gebruikten intestinale organoïden — miniatuurversies van het darmslijmvlies, gekweekt uit stamcellen die tijdens een operatie bij te vroeg geboren zuigelingen waren afgenomen. Deze organoïden kunnen worden afgevlakt tot een dun vel cellen dat eruitziet en zich gedraagt als de binnenkant van de dunne darm, inclusief de juiste bovenkant (richting darminhoud) en onderkant (richting bloedbaan). Het team plaatste deze vellen in een speciaal kweeksysteem dat de natuurlijke zuurstofgradiënt van de darm nabootst: weinig zuurstof aan de kant richting microben en meer zuurstof aan de bloedzijde. Zo konden ze het “darmoppervlak” blootstellen aan ofwel hele bacteriën afkomstig van te vroeg geboren baby’s, ofwel aan gezuiverde bacteriële componenten waarvan bekend is dat ze het immuunsysteem alarmeren.
Testen wat het beste een ontstekingssignaal triggert
De wetenschappers vergeleken meerdere manieren om ontsteking uit te lokken: een mengsel van levende bacteriën dat vaak voorkomt bij zieke vroeggeborenen; dezelfde bacteriën die door verhitting gedood waren; en twee gezuiverde bacteriële signalen, lipopolysaccharide (LPS) uit bacteriële celwanden en flagelline uit bacteriële zweepstaarten. Ze maten de afgifte van IL‑8, een signaalmolecuul dat immuuncellen aantrekt en als algemene ontstekingsmarker dient, en gebruikten grootschalige proteïneanalyse om te zien hoe de interne machinerie van de darmcellen veranderde. Verrassend genoeg verhoogden levende of dode bacteriën in dit systeem IL‑8 niet sterk, zelfs niet na 24 uur. Daarentegen veroorzaakten flagelline en vooral de combinatie van flagelline en LPS binnen slechts drie uur een duidelijke stijging van IL‑8, wat aantoont dat deze gezuiverde signalen betrouwbaar een ontstekingsstatus kunnen inschakelen.
Het meest realistische en efficiënte opzet vinden
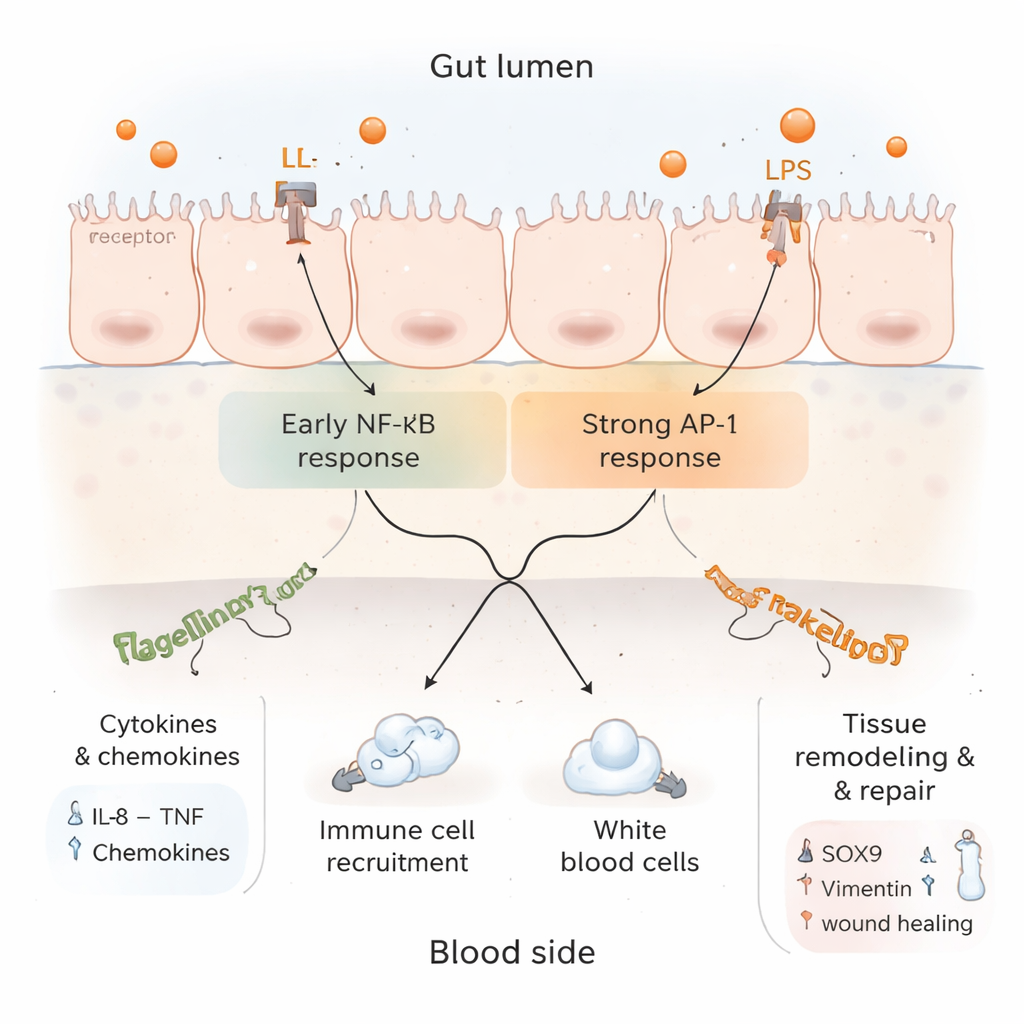
Om beter aan te sluiten bij de echte darmbiologie, richtte het team zich vervolgens op waar elk signaal van nature werkt. LPS wordt gewoonlijk waargenomen aan de kant van het darmslijmvlies die naar de darminhoud is gekeerd, terwijl flagelline vooral aan de weefselzijde wordt gedetecteerd. Met veel lagere, meer fysiologisch realistische doseringen dan in eerdere experimenten brachten ze LPS aan op de bovenkant (lumenzijde) en flagelline op de onderkant (bloedzijde) van het organoïdevel. Deze eenvoudige wijziging bracht binnen drie uur een sterke en brede respons teweeg: meerdere ontstekingsboodschappers — waaronder IL‑8, TNF en meerdere chemokines — werden van beide zijden van het weefsel afgescheiden. Tegelijkertijd veranderden honderden cellulaire eiwitten in hoeveelheid, wat duidt op grootschalige activatie van verdedigingsroutes.
Ontsteking, remmen en herstel in hetzelfde model
Diepere analyse van de eiwitgegevens liet een complex beeld zien. Enerzijds waren markers van actieve ontsteking en het aantrekken van immuuncellen verhoogd, en waren signaleringsroutes gekoppeld aan TNF en IL‑17 — beide centraal in de darmafwijrking — geactiveerd. Anderzijds waren verschillende componenten van de klassieke NF‑κB-route, die veel ontstekingsgenen aanstuurt, omlaag gereguleerd, terwijl een alternatieve route met AP‑1 actief bleef. Dit suggereert dat het weefsel na een initiële alarmfase remmen inzet om ongecontroleerde schade te voorkomen. Tegelijkertijd namen eiwitten toe die geassocieerd zijn met weefselregeneratie, structurele herinrichting en gecontroleerde celdood, wat aangeeft dat het darmslijmvlies niet alleen ontstoken was maar ook pogingen deed om zich te herstructureren en te genezen.
Wat dit betekent voor toekomstige behandelingen
Door systematisch verschillende microbiële stimuli, doseringen, posities en blootstellingstijden te vergelijken, concluderen de auteurs dat een drie uur durende blootstelling aan een lage dosis LPS aan de darmzijde samen met flagelline aan de bloedzijde de meest robuuste en reproduceerbare manier is om ontsteking te induceren in intestinale organoïden afkomstig van te vroeg geboren zuigelingen. Dit verfijnde model omvat niet alleen de uitbarsting van ontsteking, maar ook de ingebouwde remmen, tolerantiemechanismen en herstelreacties van de kwetsbare vroeggeboren darm. Het biedt een praktisch stappenplan voor andere laboratoria om te bestuderen hoe specifieke microben, geneesmiddelen of voedingsfactoren darmontsteking bij zeer vroeggeborenen kunnen verergeren of dempen — een essentiële stap richting veiligere, gerichte strategieën om verwoestende darmaandoeningen in deze kwetsbare groep te voorkomen.
Bronvermelding: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Trefwoorden: darm van te vroeg geboren zuigelingen, intestinale organoïden, darmontsteking, microbioom, necrotiserende enterocolitis