Clear Sky Science · nl
Ultrasensitieve niet-enzymatische proteïne-detectie met proximity-immunoassay en photonic resonator absorption microscopy
Waarom het vinden van sporen van proteïnen belangrijk is
Artsen en onderzoekers vertrouwen steeds vaker op eiwitten in het bloed als waarschuwing voor kanker, hartziekten, infecties of schadelijke ontsteking, vaak lang voordat symptomen ernstig worden. Veel van deze moleculaire waarschuwingssignalen komen echter in zó lage concentraties voor dat de gangbare laboratoriumtests ze vandaag de dag lastig, traag of duur detecteren. Deze studie introduceert een nieuwe testmethode, genoemd PINATA, die extreem kleine hoeveelheden van een aan ontsteking gelinkt eiwit kan opsporen met eenvoudige apparatuur en bij kamertemperatuur uitgevoerde stappen, wat de weg vrijmaakt voor toegankelijkere en gevoeliger diagnostiek.
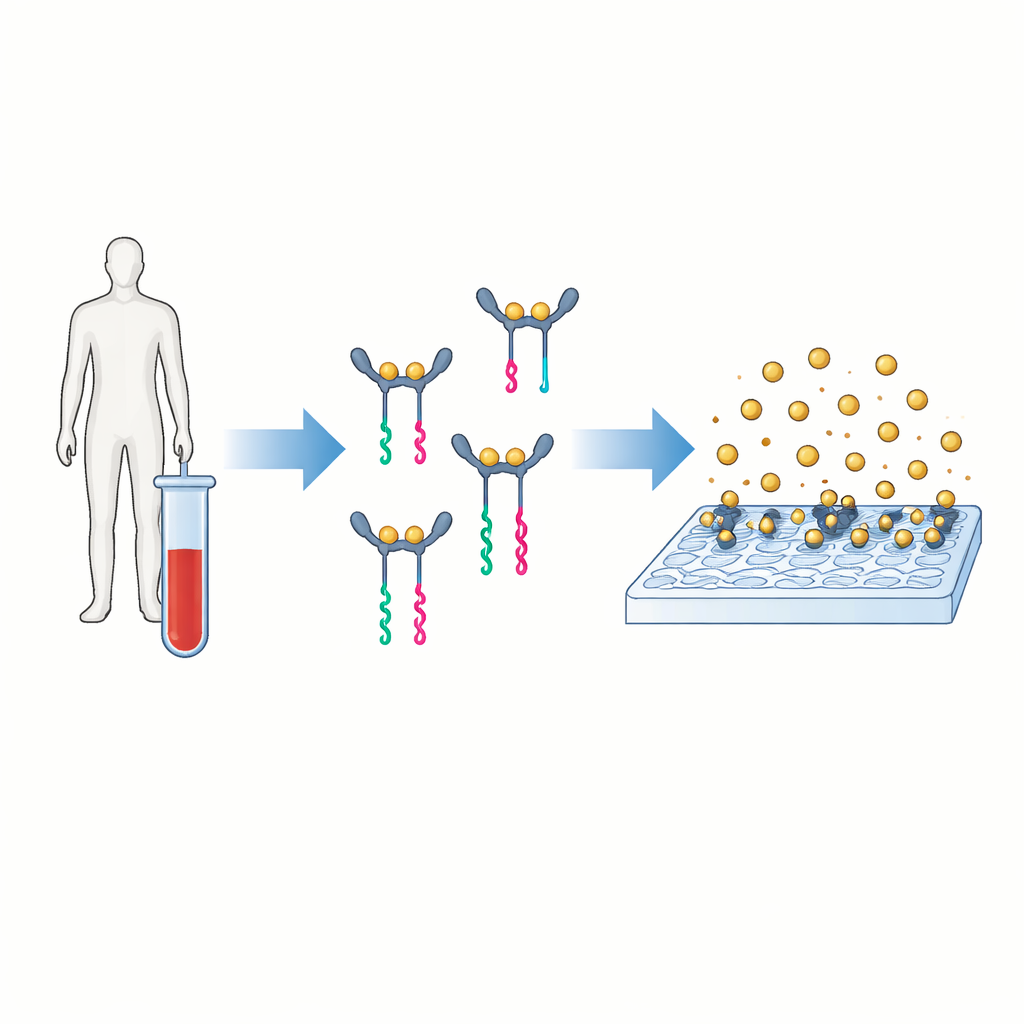
Een nieuwe manier om proteïnen in leesbare signalen om te zetten
Het kernidee van PINATA is het vertalen van de aanwezigheid van een eiwit naar een kort stukje DNA dat gemakkelijk te versterken en te tellen is. De auteurs richten zich op interleukine‑6, een signaalmolecuul in het bloed dat stijgt bij uiteenlopende aandoeningen, van infectie tot kanker. In conventionele tests hechten twee antilichamen zich aan het eiwit en dragen ze een enzym dat een gekleurd of fluorescent signaal genereert. PINATA behoudt het basisprincipe van twee antilichamen die hetzelfde eiwit herkennen, maar in plaats van enzymen worden korte DNA-strengen aan elk antilichaam gekoppeld. Wanneer beide antilichamen aan hetzelfde eiwit binden en hierdoor dicht bij elkaar komen, werken hun DNA-delen samen om een apart DNA-fragment, de reporter, vrij te geven. Elk eiwitmolecuul kan zo de vrijgave van vele identieke DNA-reporters triggeren.
DNA ‘verkeersregels’ gebruiken in plaats van enzymen
De kern van de methode bestaat uit zorgvuldig ontworpen DNA-circuits die zich gedragen als moleculaire verkeerssystemen en bepalen wanneer strengen kunnen binden, loslaten of van partner wisselen. Deze circuits zijn zodanig opgebouwd dat, tenzij een eiwit de twee aan antilichamen gekoppelde DNA-stukken bij elkaar brengt, het reporter-DNA vergrendeld blijft en er geen signaal ontstaat. Wanneer het eiwit aanwezig is, maakt de brugfunctie het reporter vrij. Dit vrijgegeven reporter neemt vervolgens deel aan een secundair amplificatieproces op een voorbereide oppervlakte. Daar gaat het herhaaldelijk strand-uitwisselingsreacties aan, waardoor één reportermolecuul veel goudnanodeeltjes naar het oppervlak kan rekruteren en zo een sterk digitaal signaal creëert zonder enzymen of temperatuurcycli te gebruiken.
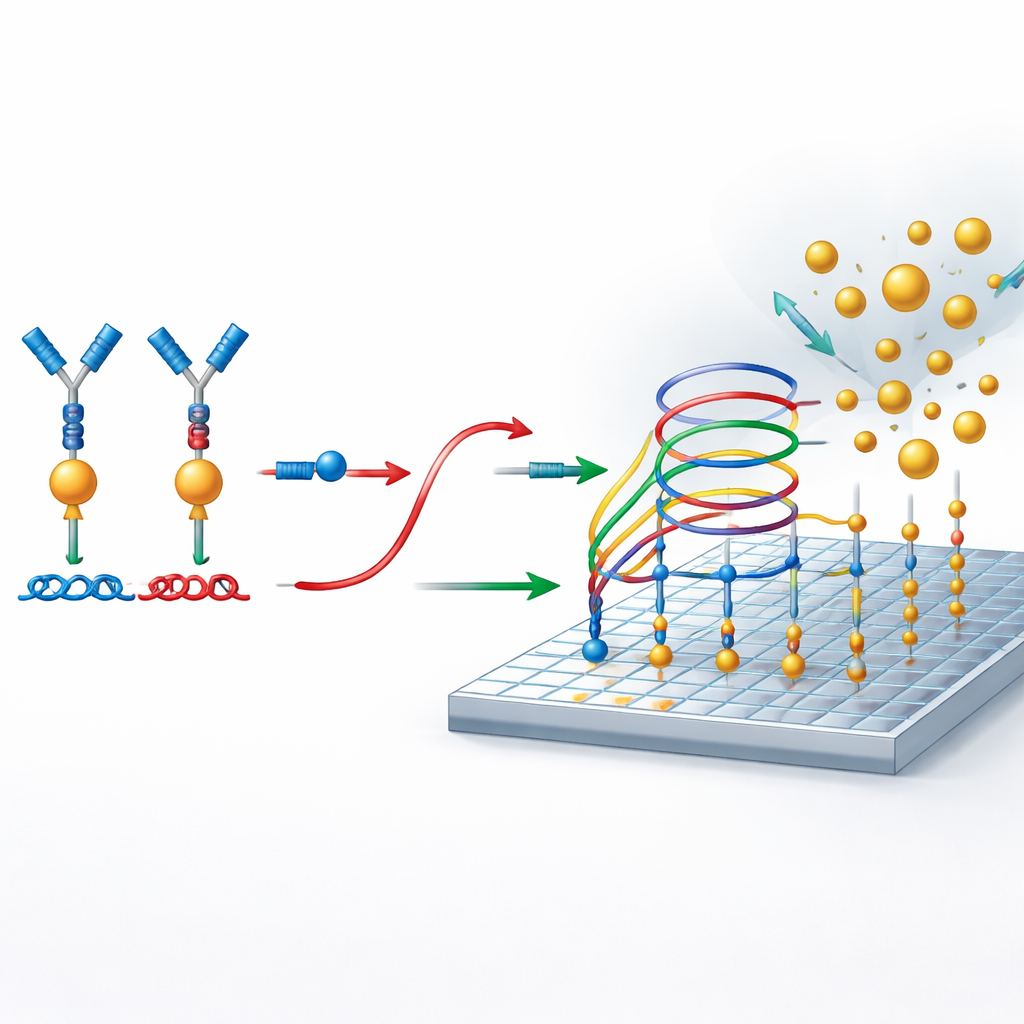
Enkele nanodeeltjes tellen als ja‑of‑nee gebeurtenissen
Om het resultaat uit te lezen gebruiken de onderzoekers photonic resonator absorption microscopy, of PRAM. Het detectieoppervlak is een speciaal gepatenteerd materiaal dat licht bij een bepaalde kleur sterk reflecteert. Wanneer goudnanodeeltjes op dit oppervlak landen, absorberen ze dat licht en verschijnen ze als donkere stippen in het microscoopbeeld. Omdat het systeem zo is ontworpen dat nanodeeltjes alleen binden wanneer reporter-DNA aanwezig is, vertegenwoordigt elke donkere stip een succesvolle detectiegebeurtenis die terug te voeren is op een eiwitmolecuul. Een eenvoudige, goedkoop te bouwen optische opstelling en beeldverwerkingssoftware worden vervolgens gebruikt om deze stippen over het oppervlak te tellen, waardoor het aantal nanodeeltjes wordt omgezet in een nauwkeurige maat voor de eiwitconcentratie.
Hoe gevoelig en selectief is de test?
Met deze aanpak tonen de onderzoekers aan dat ze interleukine‑6 kunnen detecteren tot concentraties van ongeveer 37 femtogram per milliliter — ruwweg enkele tientallen moleculen in een druppel — over een dynamisch bereik van zes logaritmische eenheden. De assay werkt in een eenvoudige twee‑stappen, 90‑minuten protocol dat volledig bij kamertemperatuur wordt uitgevoerd. De auteurs laten ook zien dat de test nauwkeurig blijft wanneer interleukine‑6 wordt toegevoegd aan complexe monsters zoals humaan serum en plasma, die doorgaans gevoelige metingen verstoren. Daarnaast bevestigen ze dat de antilichamen gericht tegen interleukine‑6 niet reageren op andere, verwante eiwitten, wat de selectiviteit van de assay benadrukt.
Wat dit kan betekenen voor toekomstige diagnostiek
Voor een niet‑specialist is de belangrijkste conclusie dat PINATA een manier biedt om ziektegerelateerde eiwitten op extreem lage niveaus te detecteren met een compact optisch instrument in plaats van omvangrijke, dure laboratoriumapparatuur. Door slimme DNA-circuits te combineren met digitale telling van nanodeeltjes, vermijdt de methode kwetsbare enzymen en verwarmingsstappen, en bereikt of overtreft toch de gevoeligheid van veel geavanceerde proteïnetests. Met verdere ontwikkeling en aanpassing aan andere doelmoleculen kan deze strategie eerder diagnose, vaker monitoring en point‑of‑care testing mogelijk maken voor een breed scala aan aandoeningen waarbij kleine veranderingen in eiwitniveaus grote klinische betekenis hebben.
Bronvermelding: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Trefwoorden: detectie van proteïne-biomarkers, ultrasensitieve diagnostiek, DNA-strengverplaatsing, interleukine-6 assay, digitale biosensing