Clear Sky Science · nl
Microfluïdisch nanomagnetisch geïsoleerde extracellulaire blaasjes afkomstig van neuronen en astrocyten om Lewy-body- en de ziekte van Alzheimer te onderscheiden
Waarom dit belangrijk is voor families en artsen
Dementie is een parapluterm die meerdere hersenziekten omvat met vergelijkbare symptomen maar heel verschillende oorzaken. Twee van de meest voorkomende, de ziekte van Alzheimer en Lewy-bodyziekte, kunnen klinisch bijna hetzelfde lijken, maar reageren anders op medicijnen en brengen andere risico’s met zich mee. Tegenwoordig is de enige manier om met zekerheid vast te stellen welke ziekte iemand had, het onderzoeken van de hersenen na overlijden. Deze studie beschrijft een nieuw soort bloedtest die kleine boodschappers losgelaten door hersencellen leest, met als doel deze twee vormen van dementie bij levenden van elkaar te kunnen onderscheiden.
Piepkleine pakketjes die van hersenen naar bloed reizen
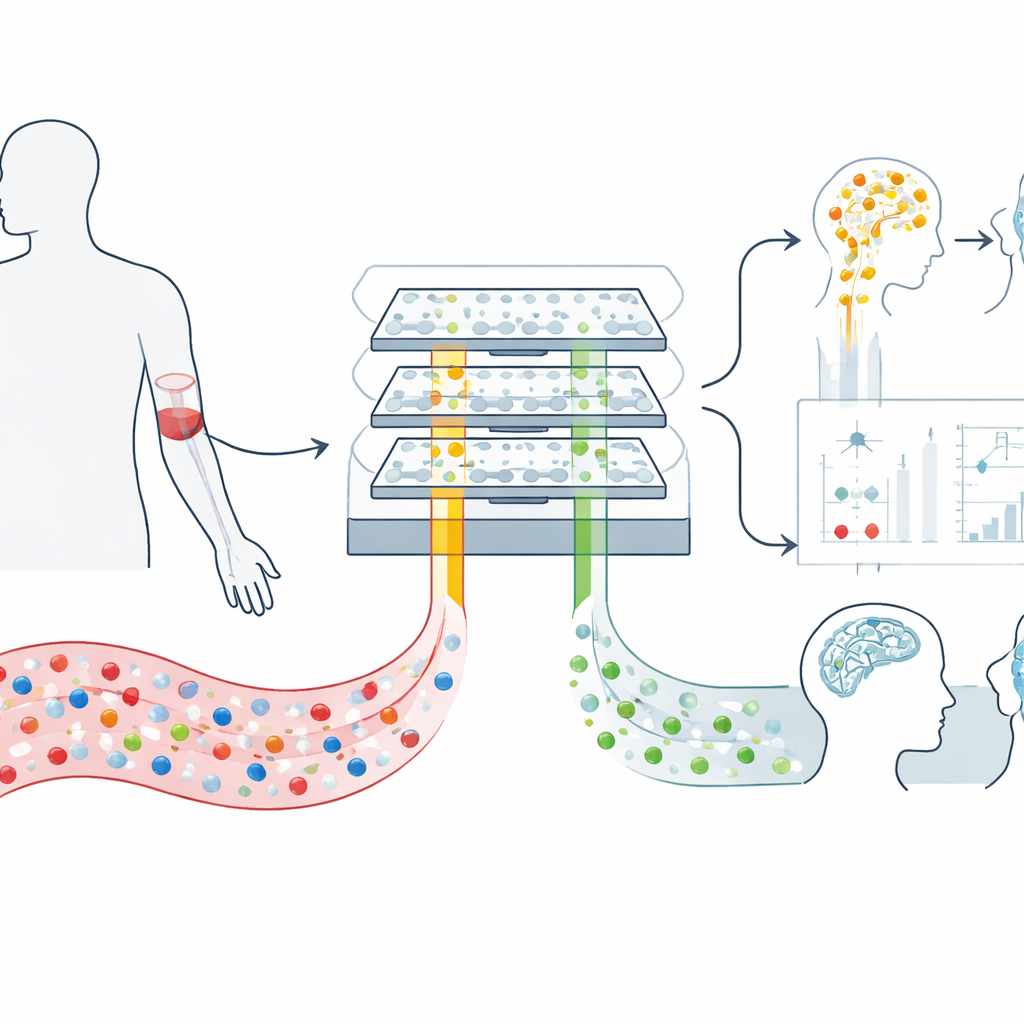
Onze hersenen stoten voortdurend microscopische blaasjes, zogenaamde extracellulaire vesikels, uit in de bloedbaan. Deze vesikels zijn als gewatteerde enveloppen die zenuwcellen en hun ondersteunende cellen versturen, en bevatten stukjes genetisch materiaal en eiwitten die weerspiegelen wat er in de hersenen gebeurt. Omdat ze de bloed-hersenbarrière kunnen passeren en in circulatie overleven, bieden ze een zeldzaam, weinig invasief venster op hersenbiologie. De uitdaging is dat een milliliter bloed honderden miljarden vesikels uit het hele lichaam bevat, waardoor die afkomstig van de hersenen sterk ondervertegenwoordigd zijn en moeilijk te isoleren met standaardlabmethoden.
Een magnetische chip die hersensignalen sorteert
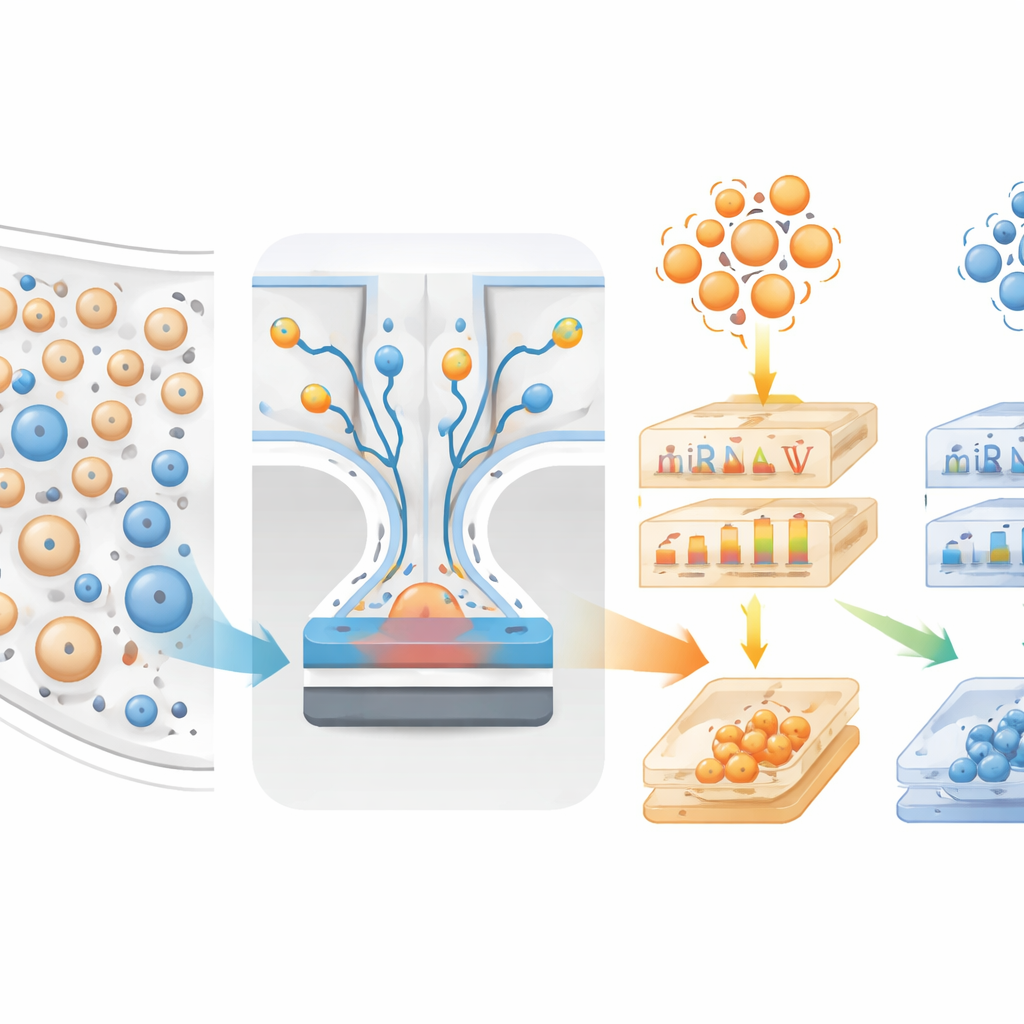
Om dit aan te pakken bouwden de onderzoekers een microfluïdisch apparaat genaamd mTENPO dat een kaartje-achtige chip combineert met een sterk magneetveld. Voordat een bloedmonster de chip binnenstroomt, worden vesikels gemarkeerd met magnetische nanodeeltjes met behulp van antilichamen die zich hechten aan oppervlakte-eiwitten die typisch zijn voor vesikels van zenuwcellen (GluR2) of astrocyten (GLAST). Terwijl het gemarkeerde mengsel door miljoenen kleine poriën in de chip stroomt, trekt het magneetveld de sterk gemarkeerde hersenvesikels naar de poriewanden en houdt ze vast terwijl de rest doordruppelt. Op deze manier kan het team twee vesikelpopulaties onafhankelijk verrijken—hoofdzakelijk van neuronen en hoofdzakelijk van astrocyten—direct uit een klein plasmamonster.
De moleculaire vingerafdrukken lezen
Van 137 vrijwilligers bij wie de hersendiagnoses achteraf werden bevestigd, isoleerde het team deze twee vesikeltypen en mat ook klassieke Alzheimer-bloedproteïnen zoals verschillende vormen van beta-amyloïd en tau. Ze sequentieerden korte regulatorische RNA’s (miRNA’s) binnen de vesikels en onderzochten welke ervan verschilden tussen mensen met zuivere Lewy-bodyziekte, zuivere Alzheimer, gemengde pathologieën of geen dementie. Meerdere miRNA’s gedragen door neuron-afgeleide en astrocyt-afgeleide vesikels, samen met enkele tau-gerelateerde eiwitten in plasma, toonden onderscheidende patronen tussen Lewy-body- en Alzheimergroepen. Toen de onderzoekers de genen in kaart brachten die door deze miRNA’s worden gereguleerd, vonden ze sterke verbanden met routes die betrokken zijn bij celoverleving, ontsteking en eiwitverwerking—processen die al in verband worden gebracht met neurodegeneratie.
Het bouwen van een krachtig gecombineerd bloedonderzoek
Aangezien geen enkele marker de ziekten zuiver scheidde, gebruikte het team machine-learningtools om een compact panel samen te stellen van de meest informatieve signalen afkomstig uit alle drie de compartimenten: neuronvesikels, astrocytenvesikels en bloedproteïnen. Het resulterende 15-kenmerkspanel omvatte 14 specifieke vesikel-miRNA’s plus twee gefosforyleerde tau-eiwitten. Getest met herhaalde kruisvalidering om overfitting te beperken, onderscheidde dit multimarkerpanel Lewy-bodyziekte van Alzheimer met ongeveer 95% nauwkeurigheid en een area under the curve van 0,96—aanzienlijk beter dan elke individuele maat alleen. Mensen wiens hersenen mengvormen van pathologie vertoonden hadden doorgaans tussenliggende markerniveaus, wat suggereert dat zulke panelen op termijn kunnen helpen gemengde ziekte te herkennen in plaats van te kiezen voor een óf–óf-label.
Van proof of concept naar toekomstig klinisch gebruik
De studie is een vroege maar belangrijke demonstratie dat hersencelvesikels in bloed voldoende gedetailleerde informatie kunnen dragen om hoofdtypen dementie te scheiden. Het werk moet nog worden bevestigd in grotere, diversere groepen en bij patiënten die in de tijd worden gevolgd, en de auteurs benadrukken huidige beperkingen bij het exact toewijzen van de cel van oorsprong voor elke vesikel. Niettemin biedt de combinatie van een schaalbare magnetische chip en een zorgvuldig gekozen multimarkerpanel een routekaart voor toekomstige bloedtests die behandelingskeuzes kunnen sturen, klinische trials kunnen verbeteren en families veel duidelijkere antwoorden kunnen geven over de specifieke ziekte achter de dementie van een dierbare.
Bronvermelding: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Trefwoorden: extracellulaire blaasjes, Lewy-bodyziekte, ziekte van Alzheimer, bloedgebaseerde biomarkers, microfluïdische diagnostiek