Clear Sky Science · nl
Plasmon-versterkte bioassay voor amplificatievrije detectie en kwantificering van SARS-CoV-2 RNA
Waarom snellere, eenvoudigere virustests ertoe doen
De COVID-19-pandemie maakte duidelijk hoezeer we afhankelijk zijn van laboratoriumtests die traag, duur en moeilijk op te schalen zijn wanneer miljoenen mensen snel een uitslag nodig hebben. Het hier beschreven werk presenteert een nieuw soort labtest die zeer kleine hoeveelheden coronavirus-genetisch materiaal kan opsporen en tellen zonder de gebruikelijke amplificatiestap die bij PCR wordt gebruikt. Deze benadering probeert ziekenhuisniveau-nauwkeurigheid dichterbij eenvoudige, goedkope tests te brengen die breder inzetbaar zouden kunnen zijn bij toekomstige uitbraken.
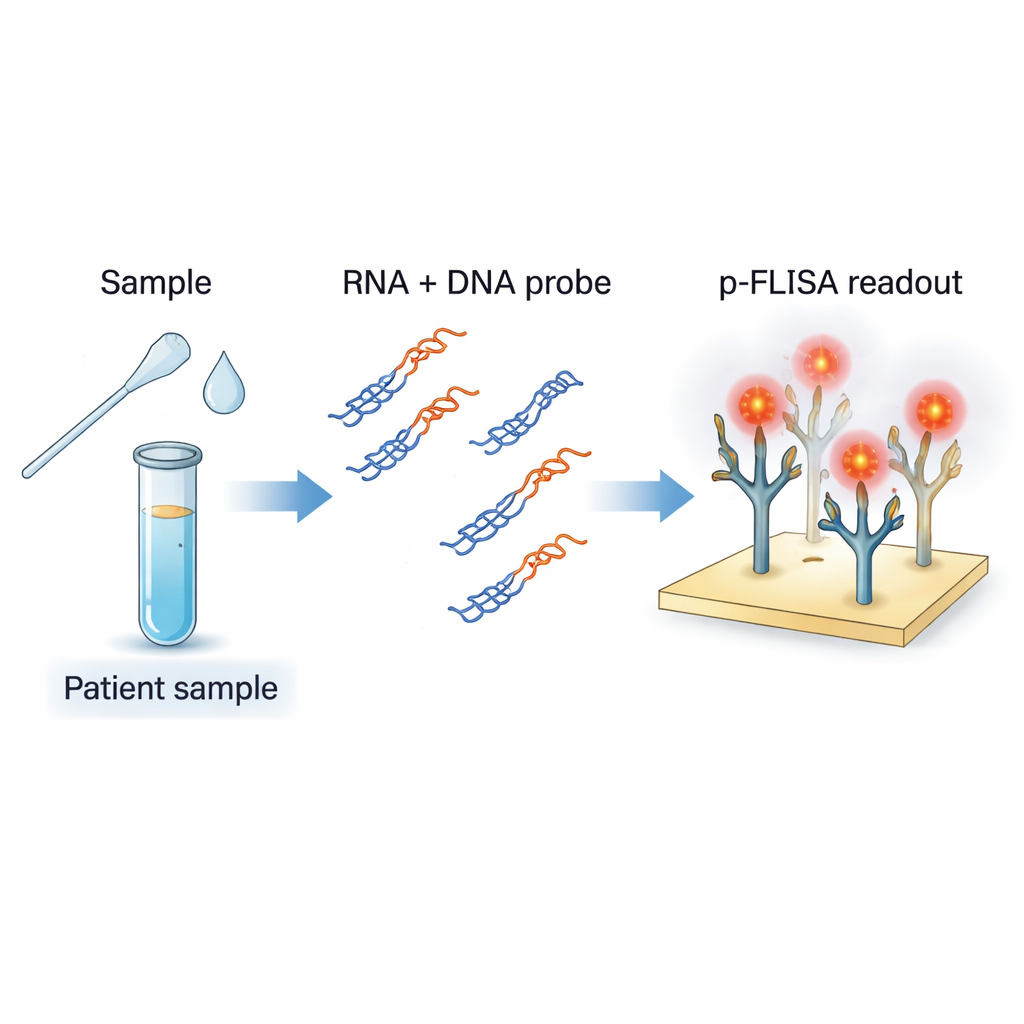
Een nieuwe manier om virale genetische sporen te zien
De standaarddiagnose van COVID-19 gebruikt RT-PCR, waarbij veel kopieën van fragmenten van viraal RNA worden gemaakt zodat ze kunnen worden gedetecteerd. Hoewel zeer gevoelig, vereist PCR complexe apparatuur, getraind personeel en tijd, en geeft meestal een 'ja of nee'-antwoord in plaats van een precieze virusload. De auteurs wilden een assay ontwikkelen die meer werkt als een sterk verbeterde versie van een ELISA-bloedtest: een eenvoudige plaat-gebaseerde opzet, maar afgestemd op directe detectie van viraal RNA en het kwantificeren van de aanwezige hoeveelheid. Hun methode is gericht op SARS-CoV-2 RNA in monsters zoals neusswabs en speeksel, maar is ontworpen om eenvoudig aan te passen aan andere RNA-virussen.
RNA omzetten in een vangbaar doelwit
Het team gebruikt korte DNA-stukjes die zijn ontworpen om overeen te komen met specifieke regio’s van het SARS-CoV-2-genoom. Wanneer deze worden gemengd met RNA dat uit een patiëntmonster is geëxtraheerd en zachtjes verwarmd en afgekoeld, paren deze DNA-probes met elk overeenkomend viraal RNA om DNA–RNA-hybriden te vormen, als een kleine rits met een RNA-streng en een DNA-streng. Een speciaal antistof, S9.6, fungeert als de vanger: het herkent en bindt sterk aan deze hybriden, maar niet aan gewone enkel- of dubbelstrengs DNA of aan niet-gerelateerd RNA. Door de bodem van een plaat met S9.6 te coaten, pakt de assay selectief alleen die hybriden die de genetische sequenties van het virus bevatten, en filtert zo de rest van het genetische 'ruis' uit het monster weg.
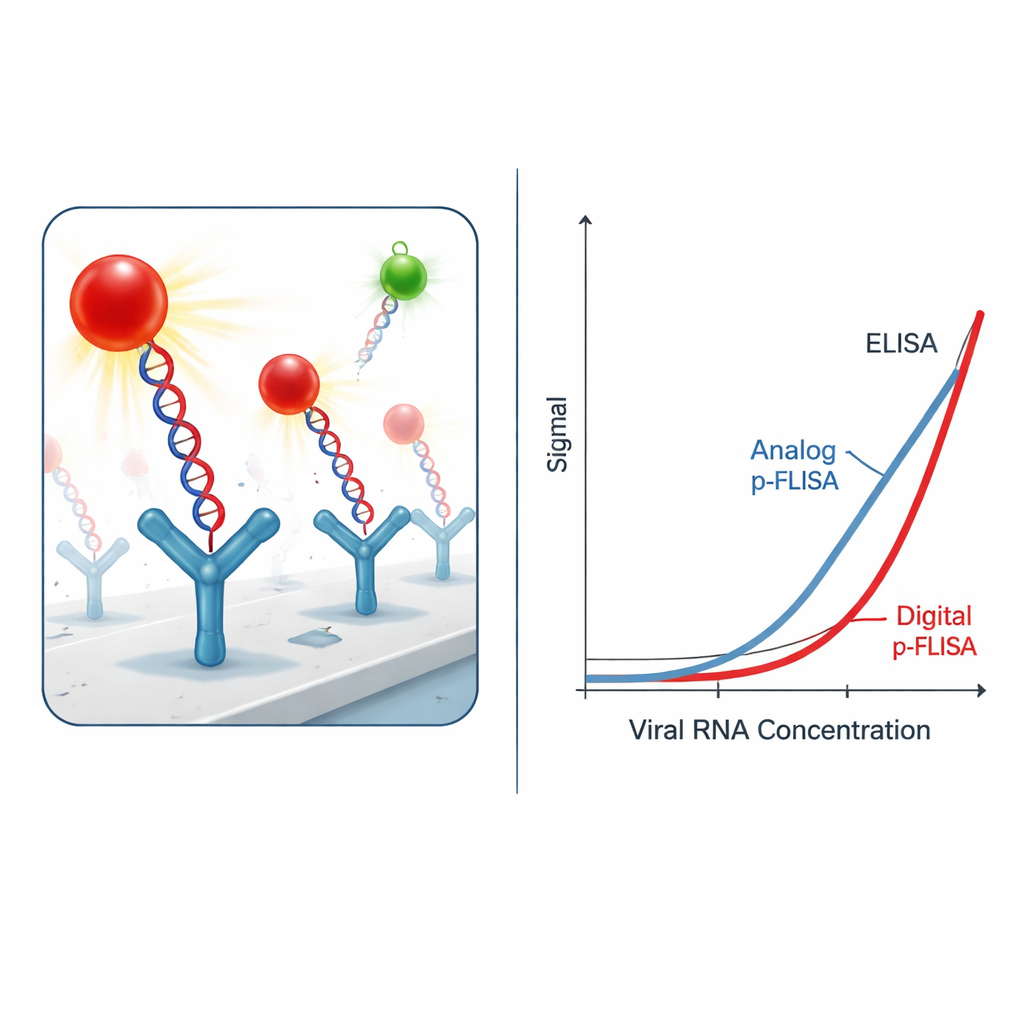
Het signaal ultrafel maken
Het simpelweg vangen van de virale hybriden is niet genoeg; de uitdaging is ze boven de achtergrondruis te zien. In plaats van conventionele fluorescentiedefstoffen gebruiken de onderzoekers "plasmonic-fluor" nanolabels — ontworpen nanodeeltjes die als kleine antennes voor licht fungeren. Elk label combineert een metalen nanostaaf met meerdere fluorescentiemoleculen en een coating die het mogelijk maakt zich vast te hechten aan biotine-tags op het DNA of antistof. Deze plasmonische labels zenden meer dan duizendmaal helderder licht uit dan standaardkleuringen onder dezelfde omstandigheden. In de praktijk betekent dat dat veel minder virale hybriden nodig zijn om een detecteerbare gloed te produceren, waardoor de gevoeligheid van de test dramatisch verbetert en de minimale meetbare concentratie viraal RNA wordt verlaagd.
Van analoge gloed naar digitale telling
In de eenvoudigste "analoge" vorm meet de assay de totale helderheid van elk putje van de plaat, vergelijkbaar met een klassieke fluorescentietest. Zelfs in deze modus verbetert het plasmon-versterkte systeem de detectielimiet en het laagst betrouwbaar kwantificeerbare niveau van SARS-CoV-2 RNA met één tot drie orde van grootte vergeleken met een traditionele ELISA die enzymen of standaardfluoroforen gebruikt. De auteurs gaan vervolgens een stap verder door over te schakelen naar een "digitale" opzet: in plaats van het licht over het hele putje te middelen, beelden ze het oppervlak met een fluorescentiemicroscoop en tellen individuele felle nanolabels met behulp van aangepaste beeldanalysetools. Deze single-particle telling levert nog eens een tien- tot dertigvoudige winst in gevoeligheid op, wat in totaal leidt tot ongeveer 2.300 maal betere detectielimieten en 460 maal betere kwantificeringslimieten dan ELISA.
De test toepassen op echte monsters
Om te zien of de methode ook buiten gecontroleerde labmengsels standhoudt, testten de onderzoekers RNA geëxtraheerd uit neusswabs en speeksel van patiënten met COVID-19, inclusief infecties door verschillende virale varianten zoals alpha/beta en delta, en ook monsters van mensen met andere luchtwegvirussen. Hun plasmon-versterkte assay detecteerde SARS-CoV-2 RNA in alle PCR-positieve monsters, zonder signaal boven de achtergrond in PCR-negatieve monsters of die met andere virussen, wat wijst op uitstekende klinische gevoeligheid en specificiteit vergelijkbaar met RT-PCR. Bovendien vertoonden de gemeten RNA-concentraties een inverse relatie met de PCR-cycle-thresholdwaarden: monsters die minder PCR-cycli nodig hadden (wat op een hogere virusload wijst) hadden hogere RNA-niveaus volgens de nieuwe assay, consistent met biologische verwachtingen en aanwijzend dat het zinvolle kwantitatieve informatie over virusload kan leveren.
Wat dit kan betekenen voor toekomstige uitbraken
Voor niet-specialisten is de kernboodschap dat deze assay een manier biedt om af te lezen hoeveel virus aanwezig is zonder de extra kopieerstap die PCR traag en apparatuur-intensief maakt. Door een selectief antistof voor RNA–DNA-hybriden te combineren met ultrafelle nanoschaalde lichtbronnen en digitale telling, benadert de methode de prestaties van PCR terwijl ze een eenvoudige, plaatgebaseerde workflow behoudt. Met verdere validatie en engineering zouden dergelijke plasmon-versterkte assays aangepast kunnen worden aan veel RNA-doelen en mogelijk worden omgevormd tot snelle, point-of-care formats, waarmee clinici niet alleen infecties kunnen diagnosticeren maar ook ziektefase en besmettelijkheid kunnen inschatten op basis van een absolute maat voor viraal RNA.
Bronvermelding: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Trefwoorden: SARS-CoV-2 RNA-detectie, plasmonische nanolabels, digitale immunoassay, amplificatievrije diagnostiek, kwantificering van virusload