Clear Sky Science · nl
Een micro-organisme-gebaseerde microfluidische biosensor voor continue monitoring van glucosewaarden in vivo
Waarom dit belangrijk is voor mensen met diabetes
Voor mensen met type 1 diabetes vereisen de huidige “kunstmatige alvleesklier”-systemen nog steeds constante aandacht: maaltijden moeten worden aangekondigd, alarmen afgehandeld en ’s nachts bestaat de zorg voor hypoglykemie. Deze studie onderzoekt een radicaal ander type glucosesensor die niet vertrouwt op één enkel enzym of een computerformule, maar een klein levend stukje van het lichaamseigen suikerregulerende mechanisme leent: clusters van pancreascellen, de zogeheten eilandjes. Door deze mini-organen te laten doen waar de evolutie ze voor heeft geoptimaliseerd, streven de onderzoekers ernaar slimere, veiligere glucosesensoren te bouwen die op termijn meer zelfstandig op de achtergrond kunnen functioneren.
Een klein orgaan als levende sensor
De meeste huidige biosensoren detecteren chemicaliën met gezuiverde moleculen of een enkele celijn. Ze reageren op één specifieke stof en geven het ruwe signaal door aan software die probeert het te interpreteren. De auteurs betogen dat deze benadering een krachtig ingebouwd “computer”-mechanisme negeert: micro-organen, zoals alvleesklier-eilandjes, die van nature veel signalen tegelijk waarnemen en omzetten in een gecoördineerde respons. Elk eilandje bevat meerdere hormoonproducerende celtypen die continu met elkaar communiceren. Samen houden ze de bloedsuiker binnen een smalle, veilige marge en reageren ze niet alleen op glucose maar ook op aminozuren, darm- en stresshormonen en op de recente geschiedenis van pieken en dalen in het lichaam. Deze ingebouwde complexiteit, zo suggereren ze, kan benut worden om rijkere, betrouwbaardere informatie te leveren dan een eenvoudige glucose-oxidase-sensor.
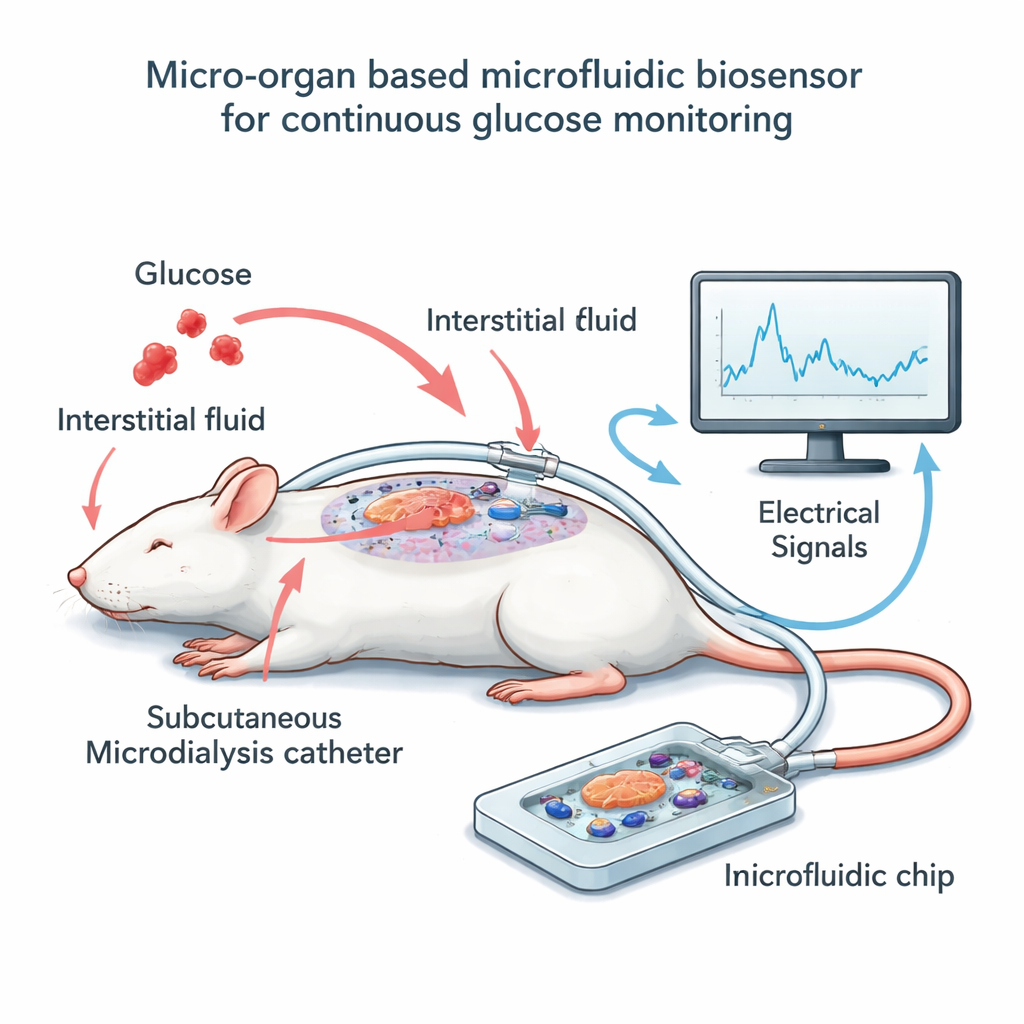
Het bouwen van het chip-en-katheter systeem
Om dit idee te testen bouwde het team een klein extern apparaat dat enkele tientallen muiseilandjes huisvest bovenop een raster van microscopische elektroden. In plaats van deze cellen direct in bloed te dompelen, gebruikten ze een techniek genaamd microdialyse: een dun, flexibel kathetertje ligt net onder de huid van geïntubeerde ratten en verzamelt langzaam de omringende weefselvloeistof, die de bloedsuiker nauw volgt maar met een korte vertraging. Een lage, constante stroming voert deze vloeistof door een smal kanaal over de eilandjes op de chip. Naarmate de glucosespiegels in het dialysaat stijgen en dalen, veranderen de eilandjes hun elektrische activiteit, die de elektroden vastleggen als langzame, golfachtige signalen. Parallel daaraan maten de onderzoekers periodiek glucose in het bloed van de ratten en in het dialysaat, waardoor ze de elektrische uitlezing in de tijd konden afstemmen op de werkelijke suikerwaarden.
Hoe de levende sensor op veranderende suiker reageerde
Eerst testten de wetenschappers of eilandjes op de elektroden konden reageren op echte bloedeigenschappen in plaats van simpele laboplossingen. Ze stelden ze bloot aan menselijk en ratsserum met verschillende glucosewaarden en zagen duidelijke, graduele veranderingen in zowel de frequentie als de grootte van hun elektrische golven. De reacties waren sterk genoeg om kleine stapjes in suikerconcentratie te onderscheiden binnen het bereik dat relevant is voor diabetes. Vervolgens gingen ze over op ratexperimenten, waarbij ze eerst een glucose-injectie gaven om de bloedsuiker te verhogen en later insuline injecteerden om deze te verlagen. Na rekening te hebben gehouden met de tijd die glucose nodig heeft om van bloed naar weefselvloeistof en door de tubing te bewegen, vonden ze dat de frequentie van de langzame elektrische signalen van de eilandjes vrijwel synchroon steeg en daalde met de bloedsuiker. Statistische analyse over meerdere dieren toonde een opmerkelijk strakke, reproduceerbare relatie tussen signaalfrequentie en glucosewaarde, terwijl signaalamplitude, hoewel informatief, wat variabeler was.
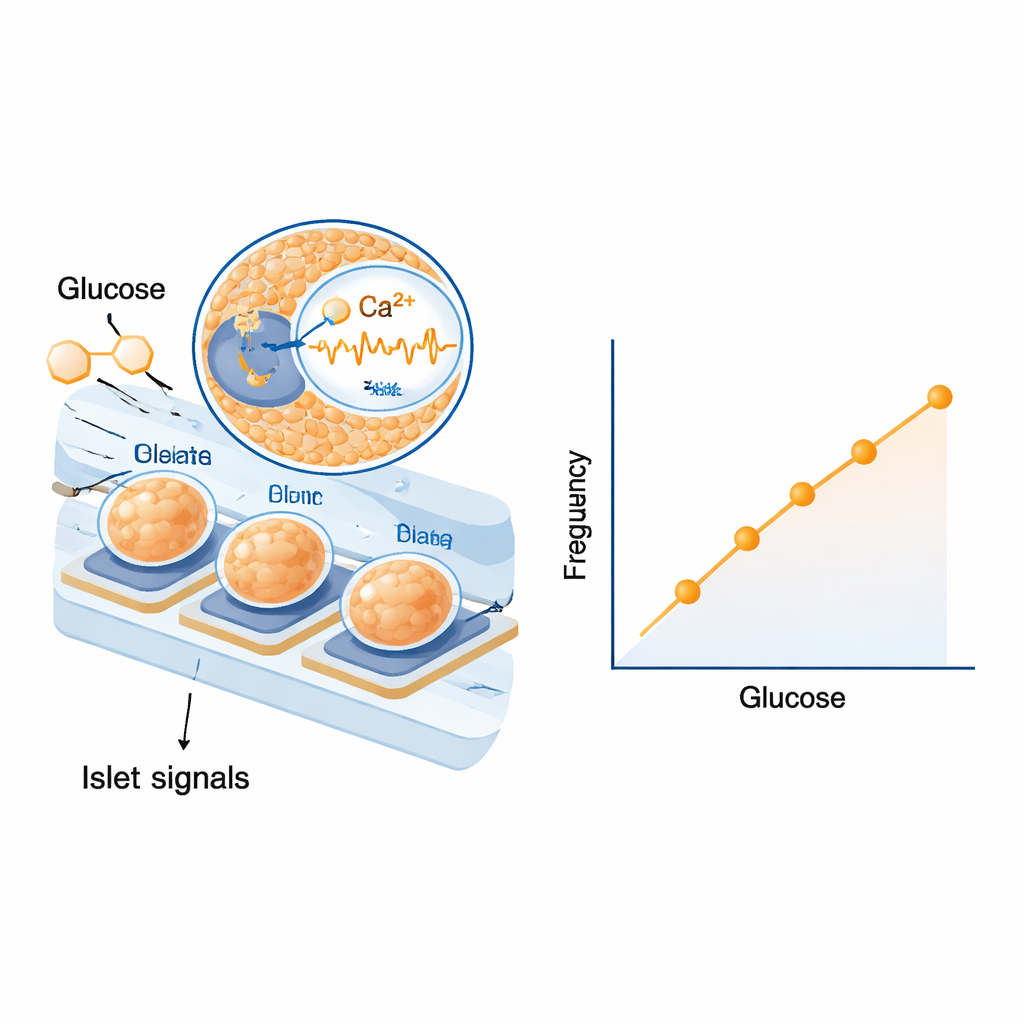
Ingebouwde veiligheidskenmerken vanuit de biologie
Een belangrijk voordeel van het gebruik van hele eilandjes in plaats van één enkel molecuul is dat hun gedrag al veiligheidsmechanismen bevat die door de evolutie zijn gevormd. Eerder werk, en aanwijzingen uit deze studie, tonen dat eilandjes sterker reageren wanneer glucose daalt dan wanneer het stijgt — een vorm van “hysterese” die helpt beschermen tegen gevaarlijke hypoglykemie. De elektrische patronen worden ook beïnvloed door naburige celtypen die de insuline-afgifte kunnen versterken of dempen afhankelijk van de behoeften van het lichaam. Omdat de chip simpelweg naar deze geïntegreerde signalen luistert zonder kleurstoffen of genetische modificaties toe te voegen, kunnen ze dagenlang opnemen zonder de cellen te schaden. De auteurs benoemen technische uitdagingen voor de toekomst, zoals het vermijden van luchtbellen, het verzekeren van langdurige microdialyseprestaties en het beslissen welk soort menselijke of stamcel-afgeleide eilandjes uiteindelijk gebruikt moet worden. Toch suggereren computersimulaties met een gevestigd diabetessmodel dat een dergelijke eiland-gebaseerde sensor onder moeilijke omstandigheden mee kan doen met — of zelfs beter kan presteren dan — de huidige glucosesensoren.
Wat dit zou kunnen betekenen voor toekomstige diabeteszorg
Dit werk toont aan dat een handvol pancreasmicro-organen, levend gehouden op een kleine chip en verbonden met het lichaam via een dunne katheter, continu de bloedsuiker kan volgen in levende dieren door hun natuurlijke elektrische ritmes. Voor niet-specialisten is de kernboodschap dat in plaats van een simpele chemische sensor te vragen glucose te meten en een computer te laten raden wat dat voor het lichaam betekent, deze benadering direct luistert naar hetzelfde type levend weefsel dat normaal bepaalt hoeveel insuline moet worden afgegeven. Als dit verfijnd wordt en praktisch toepasbaar wordt gemaakt voor mensen, zouden zulke levende biosensoren de kern kunnen vormen van werkelijk autonome kunstmatige-alvleesklier-systemen — apparaten die stilletjes anticiperen op de behoeften van het lichaam en de dagelijkse last van diabetesmanagement verminderen.
Bronvermelding: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Trefwoorden: continue glucosesurveillance, kunstmatige alvleesklier, alvleesklier-eilandjes, microfluidische biosensor, type 1 diabetes