Clear Sky Science · nl
Een verhalende review van de invloed van apolipoproteïnen op atherosclerotische kransslagaderplaques
Waarom de vetten in uw bloed nog steeds van belang zijn
Hartaanvallen en beroertes beginnen vaak met stille veranderingen in de bloedvaten die het hart van bloed voorzien. Dit artikel kijkt verder dan het bekende beeld van “goede” en “slechte” cholesterol naar de eiwitomhulsels die vetten door de bloedbaan vervoeren, de zogeheten apolipoproteïnen. Door te volgen hoe vier van deze eiwitten de groei, samenstelling en behandeling van kransslagaderplaques — de vetophopingen die hartkransslagaders verstoppen — beïnvloeden, tonen de auteurs aan waarom sommige mensen een hoog risico op hartziekten behouden, zelfs wanneer hun cholesterolwaarden ideaal lijken.
De verborgen spelers op cholesterol
De meesten van ons horen over LDL- en HDL-cholesterol, maar elk van deze deeltjes is omgeven door een of meer apolipoproteïnen die helpen bepalen waar het deeltje naartoe gaat en hoe gevaarlijk het is. Deze review richt zich op vier belangrijke types: apolipoproteïne(a), apolipoproteïne A‑I, apolipoproteïne B en apolipoproteïne C‑III. Gezamenlijk bepalen ze hoe vetdeeltjes worden samengesteld, hoe lang ze in circulatie blijven en hoe gemakkelijk ze de vaatwand binnendringen en schade aanrichten. Moderne beeldvormingstechnieken — echografie in de slagader, hoogresolutie lichtgebaseerde scans en CT-angiografie — stellen artsen nu in staat niet alleen te zien hoe vernauwd een slagader is, maar of de plaques zacht en scheurgevoelig of dicht en verkalkt zijn. 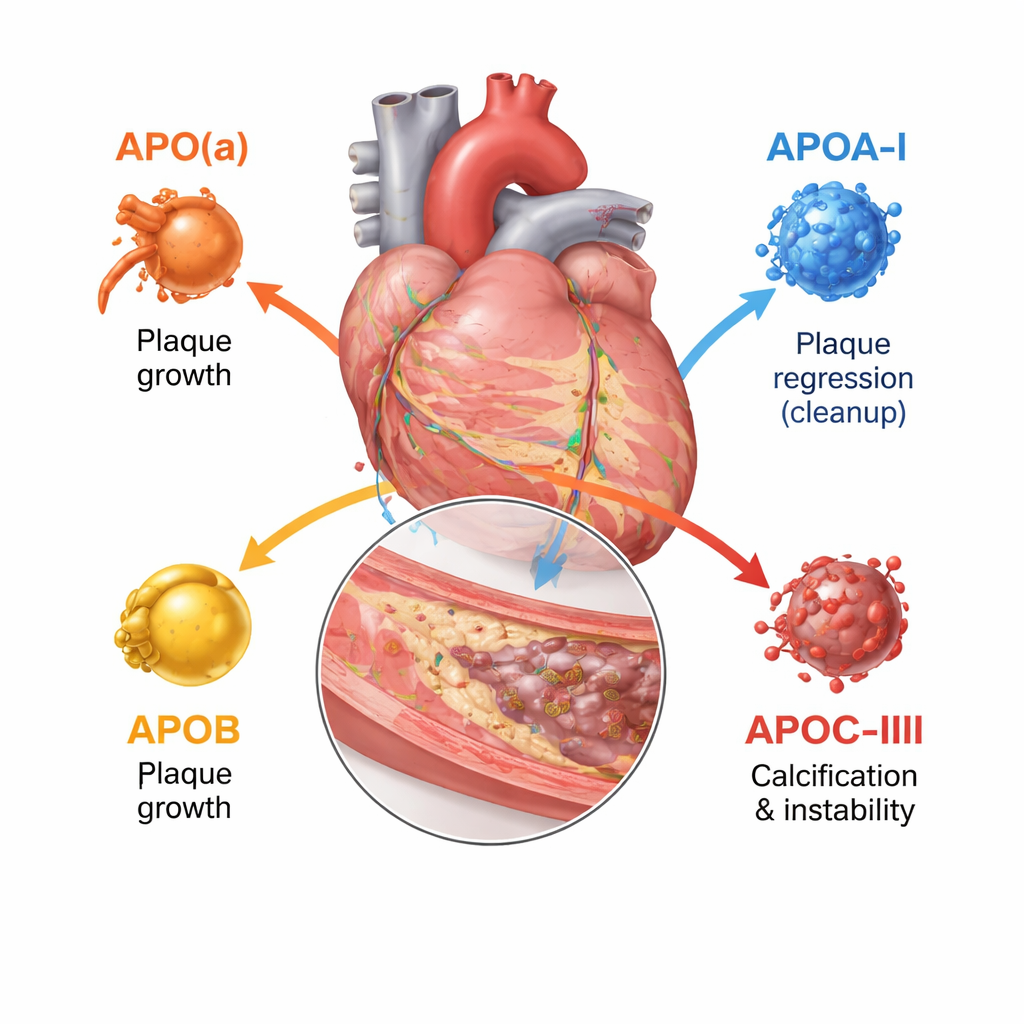
Hoe vier eiwitten gevaarlijke plaques vormen
Apolipoproteïne B zit op elk LDL-achtig deeltje en telt feitelijk hoeveel atherogene — slagaderverstopende — deeltjes er in het bloed aanwezig zijn. Hoe meer ApoB-dragers iemand heeft en hoe langer ze circuleren, hoe groter de totale plaque‑belasting in de kransslagaders. Beeldvormingsstudies in de kransslagaders tonen dat hogere ApoB-waarden samengaan met grotere plaques, langere laesielengte, meer zachte, necrotische kernen en minder stabiliserende calciumafzettingen. Daarentegen helpt apolipoproteïne A‑I, het belangrijkste eiwit op HDL, cholesterol uit plaquecellen te verwijderen en terug te vervoeren naar de lever. Hogere functionele ApoA‑I-activiteit en een gunstige verhouding van HDL-cholesterol tot ApoA‑I worden geassocieerd met tragere plaquegroei en meer vezelig, stabiel weefsel, hoewel het louter verhogen van HDL-cholesterol in het bloed zich niet heeft vertaald in minder hart‑ en vaatgebeurtenissen.
Een risicovol speciaal eiwit en een bevorderaar van verharding
Apolipoproteïne(a) vormt een deeltje genaamd lipoproteïne(a), of Lp(a), wanneer het zich aan een LDL‑achtig kern bindt. Lp(a) wordt vrijwel volledig door genen bepaald en verandert doorgaans niet door dieet. Beeldvormingsstudies bij duizenden patiënten tonen dat mensen met hoge Lp(a)-waarden meer totale plaque hebben, meer gebieden met lage dichtheid en vetrijke regio’s, en meer focale “hoogrisico” plaques die gevoelig zijn voor ruptuur, zelfs wanneer LDL-cholesterol al agressief wordt behandeld. De review concludeert dat Lp(a) een belangrijk “residu‑risico” vertegenwoordigt dat standaard cholesterolverlagende therapieën niet volledig wegneemt. Apolipoproteïne C‑III, vooral aangetroffen op triglyceridenrijke deeltjes, vertraagt hun klaring en zet ontsteking in gang. Mensen met hogere ApoC‑III hebben meer coronaire calcium en complexere, verkalkte knobbels in plaques — kenmerken die samenhangen met gevorderde ziekte en verharding van de vaten.
Nieuwe medicijnen die op de juiste doelen mikken
Omdat deze eiwitten het risico nauwkeuriger volgen dan cholesterol alleen, worden ze directe medicijndoelen. Voor Lp(a) kunnen verschillende injecteerbare genetische middelen — antisense- en small‑interfering RNA‑middelen — niveaus in vroege studies met 80–95% verlagen, en een pil die de assemblage van het deeltje blokkeert laat ook grote verminderingen zien. Voor ApoC‑III kunnen recent goedgekeurde therapieën triglyceriden en ApoC‑III zelf sterk verlagen, en vroege gegevens suggereren dat ze pancreatitis kunnen verminderen en mogelijk de plaque‑verkalking kunnen beïnvloeden. 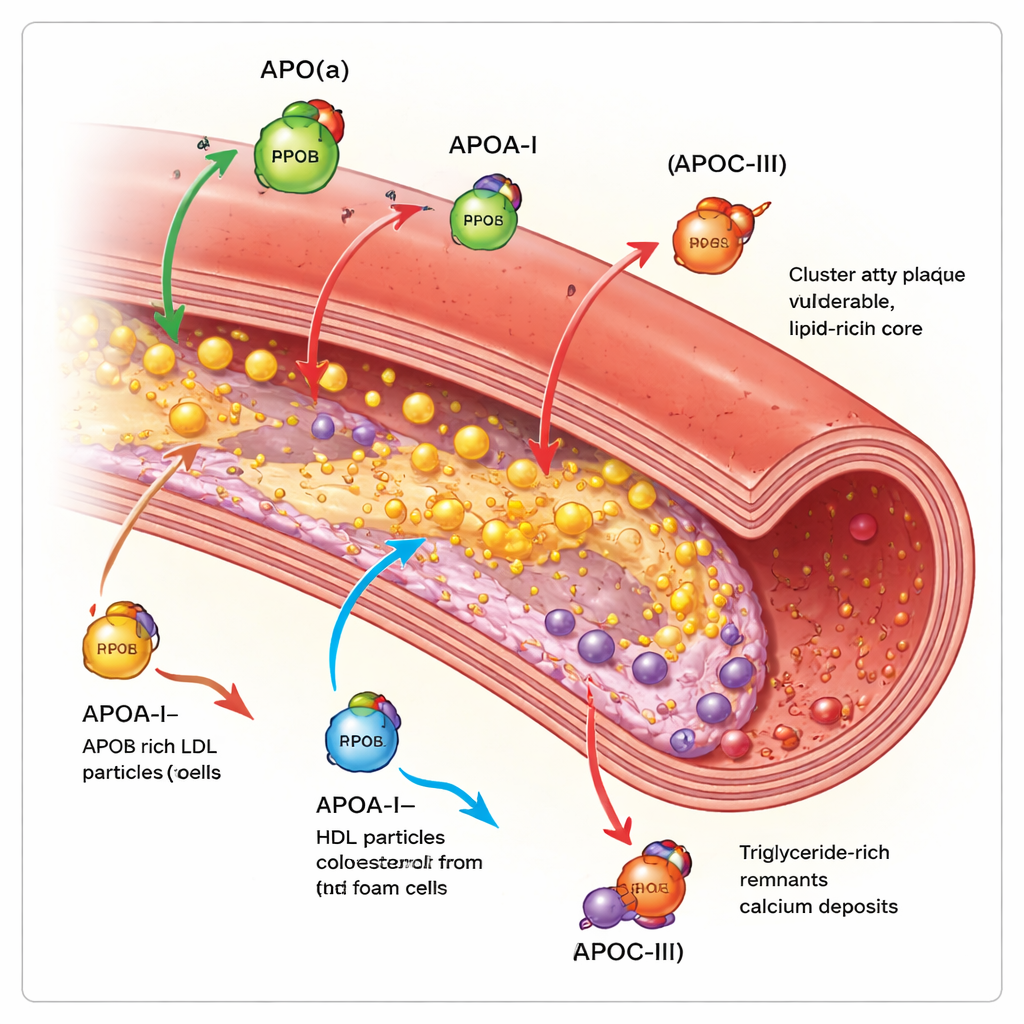
Wat dit betekent voor het beschermen van uw hart
In eenvoudige bewoordingen betoogt deze review dat wie een hartaanval krijgt niet alleen wordt bepaald door cholesterolwaarden, maar door de mix en het gedrag van de eiwitomhulde deeltjes die dat cholesterol vervoeren. ApoB weerspiegelt hoeveel “slechte” deeltjes de vaatwand bestoken, ApoA‑I weerspiegelt het systeem dat cholesterol afvoert, Lp(a) voegt een extra, genetisch bepaalde risicofactor toe, en ApoC‑III bevordert verharde, ontstoken plaques. Opkomende geneesmiddelen die specifiek Lp(a) en ApoC‑III verlagen, en een preciezer gebruik van ApoB en ApoA‑I in routinetests, kunnen artsen in staat stellen preventie af te stemmen op de individuele plaquebiologie van elke patiënt en verborgen risico’s op te sporen die standaard lipidenpanelen missen.
Bronvermelding: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
Trefwoorden: lipoproteïne(a), apolipoproteïne B, apolipoproteïne A-I, apolipoproteïne C-III, kransslagader plaque‑beeldvorming