Clear Sky Science · nl
Correlatieve multimodale beeldvorming voor microscopische ruimtelijke inkaartbrenging van interacties tussen collageen en genactiviteit in menselijk weefsel
Waarom het belangrijk is om in spieren te kijken
Ziekten die onze organen geleidelijk doen litteken vormen, zoals Duchenne-spierdystrofie (DMD), spelen zich af op schalen die te klein zijn voor het blote oog. Genactiviteit vindt plaats in individuele cellen, terwijl het steunweefsel daaromheen is opgebouwd uit piepkleine eiwitvezels. Tot nu toe konden wetenschappers deze twee werelden zelden samen in exact hetzelfde weefselvlak bekijken. Deze studie introduceert een methode om precies dat te doen en toont hoe genboodschappen en het structurele skelet van het lichaam op microschaal met elkaar in wisselwerking staan.
Twee ‘camera’s’ op hetzelfde stukje weefsel
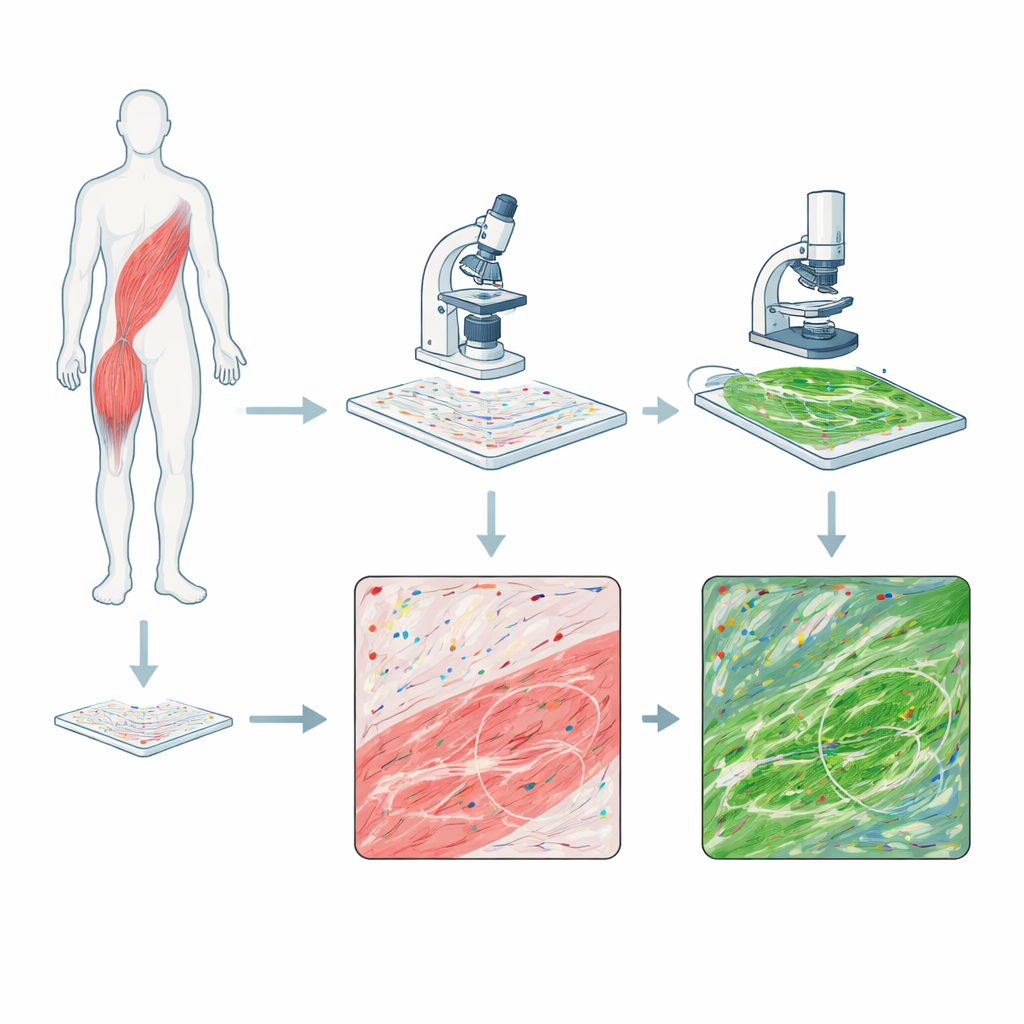
De onderzoekers combineerden twee krachtige beeldvormingstechnieken op afzonderlijke secties van menselijke skeletspierbiopten van mensen met DMD en van een gezonde vrijwilliger. De ene techniek, RNAscope, kleurt individuele RNA-moleculen—de werkende kopieën van genen—in als gekleurde stippen en laat zien waar specifieke genetische boodschappen aanwezig zijn. De tweede techniek, multiphotonmicroscopie, gebruikt laserlicht om collageenvezels in het weefsel te laten opgloeien zonder extra kleurstoffen en legt zo de architectuur van het bindweefsel vast dat tijdens littekening en fibrose verdikt. Door eerst de RNA-signalen en daarna de collageensignalen op exact dezelfde microscoopglaasje te beelden, konden ze de twee beelden uitlijnen zodat elke stip van genactiviteit pixel voor pixel vergeleken kon worden met het omliggende vezelnetwerk.
Wat de afzonderlijke beelden al aangeven
Het bekijken van elk beeldvormingsmethode afzonderlijk legde al duidelijke verschillen bloot tussen ziek en gezond spierweefsel. RNAscope liet zien dat spieren van de DMD-patiënten minder dystrofine-transcripten bevatten—de RNA-boodschappen die nodig zijn om het ontbrekende dystrofine-eiwit te maken—dan de gezonde sample. De resterende signalen verschilden ook in grootte afhankelijk van welk deel van het gen werd gericht, wat duidt op verschillen in de verwerking van het lange dystrofinemolecuul. Ondertussen toonden multiphotonbeelden dat DMD-spieren vol lagen lange, dichte collageenvezels zaten, een visueel teken van fibrotische littekenvorming, terwijl de gezonde spier minder en gelijkmatiger verdeelde vezels had. Deze bevindingen komen overeen met klinische ervaring: bij DMD wordt spierweefsel geleidelijk vervangen door vet en littekenweefsel.
Uitzoomen: brede patronen door het weefsel
Nadat de twee soorten beelden digitaal waren geregistreerd, verdeelde het team elke weefselsectie in een raster en behandelde elk vakje als een klein buurtgebied. In elk vakje maten ze zowel collageenkenmerken—vezellengte, oriëntatie en hoe kronkelig of recht de vezels waren—als de lokale dichtheid van dystrofine-RNA-stippen. Deze ‘warmtekaart’-weergave liet vlekkerige, regio-tot-regio variatie zien in zowel genactiviteit als collageenstructuur binnen DMD-spier. Toen deze maten met statistische tests werden vergeleken, toonden transcripthoeveelheid en collageeneigenschappen echter vrijwel geen consistente relatie op deze grove schaal. Met andere woorden: wanneer werd gemiddeld over relatief grote regio’s, waren gebieden met veel dystrofine-RNA niet betrouwbaar meer of minder fibrotisch dan gebieden met minder RNA-signalen.
Inzoomen: relaties op cellulaire schaal
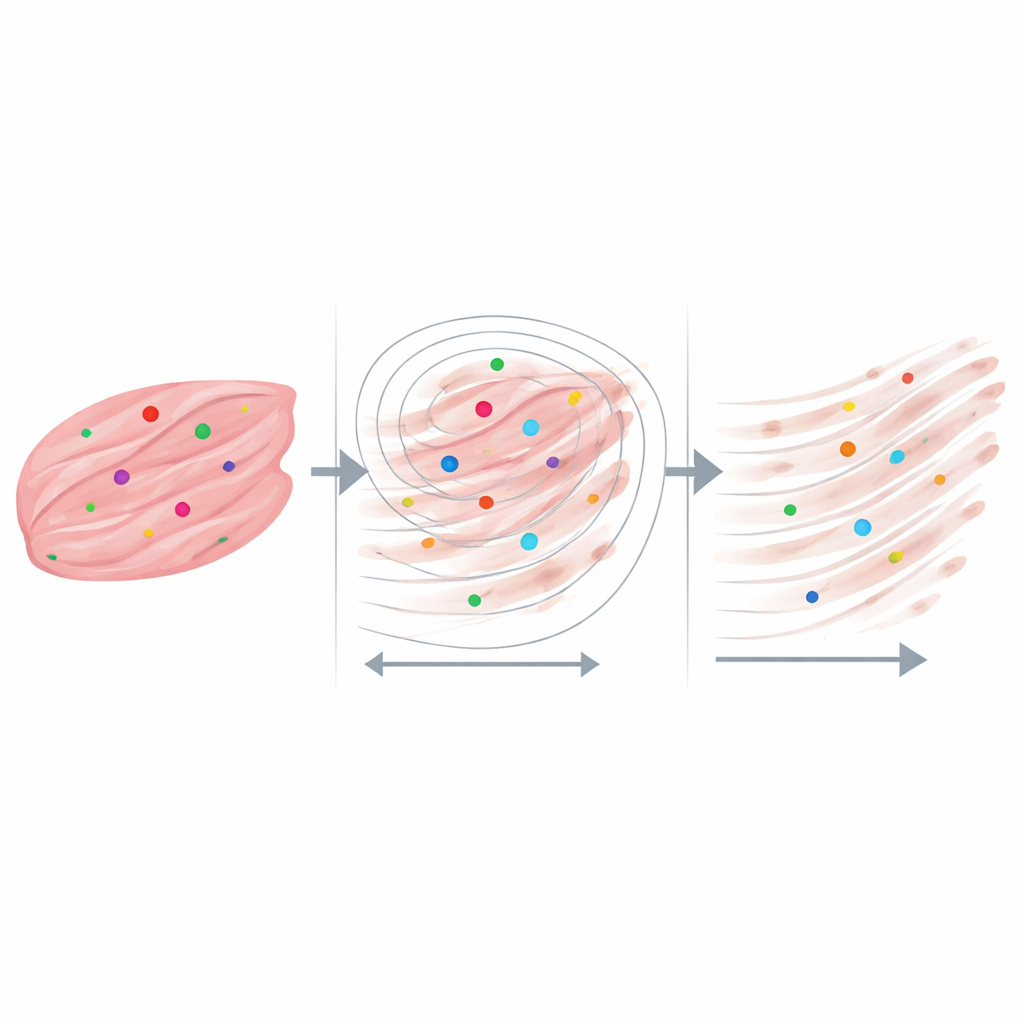
De meest onthullende resultaten ontstonden toen de wetenschappers zich concentreerden op buurtgebieden van slechts enkele tientallen micrometers—ongeveer de grootte van individuele spiervezels en hun directe omgeving. Voor elke RNA-stip trokken ze een reeks rondgroeiende cirkels en vroegen ze hoeveel collageenvezels zich binnenin lagen en hoe lang die vezels waren. Zowel in DMD- als in gezond weefsel waren de collageenvezels het langst vlak naast de dystrofine-RNA-signalen en werden ze geleidelijk korter verder weg. In de ernstigst verkrachte monsters hadden transcriptstippen vrijwel altijd collageen in de directe nabijheid, zelfs op zeer korte afstanden, terwijl in het gezonde monster veel RNA-stippen in gebieden lagen met weinig of geen collageen dichtbij. Controleanalyses met willekeurig geplaatste punten en licht aangepaste beeldverwerkingsinstellingen lieten zien dat dit patroon niet eenvoudigweg door toeval of door eigenaardigheden van de software kon worden verklaard.
Wat dit kan betekenen voor spierziekten en daarbuiten
Deze bevindingen suggereren dat belangrijke verbanden tussen genboodschappen en weefselstructuur verborgen kunnen blijven wanneer men alleen naar grote gemiddelden kijkt, maar zichtbaar worden bij onderzoek op cellulaire schaal. In deze proof-of-conceptstudie lagen gebieden verrijkt in specifieke dystrofine-transcripten vaak dicht bij langere, dichtere collageenvezels, wat suggereert dat lokale genactiviteit en fibrotische remodelering elkaar binnen kleine microomgevingen van spier kunnen beïnvloeden. De auteurs benadrukken dat hun patiëntengroep klein is en dat het werk nog geen klinische test is. In plaats daarvan presenteren ze een flexibel platform dat kan worden uitgebreid naar andere genen, weefseltypen en beeldvormingstechnieken. Door te koppelen waar genen actief zijn en hoe het weefselraamwerk is opgebouwd, opent deze aanpak de deur naar het ontdekken van nieuwe ruimtelijke biomarkers voor fibrose, regeneratie en reacties op op RNA gebaseerde nieuwe therapieën.
Bronvermelding: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Trefwoorden: multimodale beeldvorming, Duchenne-spierdystrofie, collageenfibrose, ruimtelijke genexpressie, skeletspierbiopsie