Clear Sky Science · nl
Een éénstaps radiolabelingstrategie voor PET-, SPECT- en therapeutische radionucliden met nanodeeltjes als universele chelator
Waarom kleine radioactieve deeltjes ertoe doen
De moderne kankerzorg vertrouwt steeds meer op radioactieve geneesmiddelen die tumoren zichtbaar maken voor beeldvorming en die in sommige gevallen van binnenuit beschadigen. Het ontwikkelen van elk nieuw radioactief middel is echter traag en gevoelig, omdat de meeste ontwerpen rondom een specifiek radioactief metaal op maat moeten worden gemaakt. Deze studie onderzoekt een heel ander principe: het gebruik van één type ijzerhoudend nanodeeltje als een "universeel stopcontact" dat veel verschillende medische isotopen voor beeldvorming en therapie kan dragen, waardoor het proces van maken en verfijnen van zulke middelen mogelijk wordt versneld.
Van veel sleutels naar één slot
Huidige radioactieve geneesmiddelen vertrouwen meestal op chemische grijpers, chelatoren genoemd, die metaalatomen vasthouden en koppelen aan antilichamen of andere doelgerichte moleculen. Elk radioactief metaal heeft vaak zijn eigen chelator en procedure nodig—condities zoals temperatuur, zuurgraad en reactietijd variëren. Voor sommige medisch belangrijke metalen, met name die gebruikt worden voor krachtige alfa‑deeltje therapieën, bestaat nog geen ideale chelator. De auteurs stellen dat dit metaal‑voor‑metaal‑paradigma een knelpunt is: de lijst van bruikbare isotopen groeit, maar de chemie om ze veilig te hanteren kan niet snel genoeg meekomen.
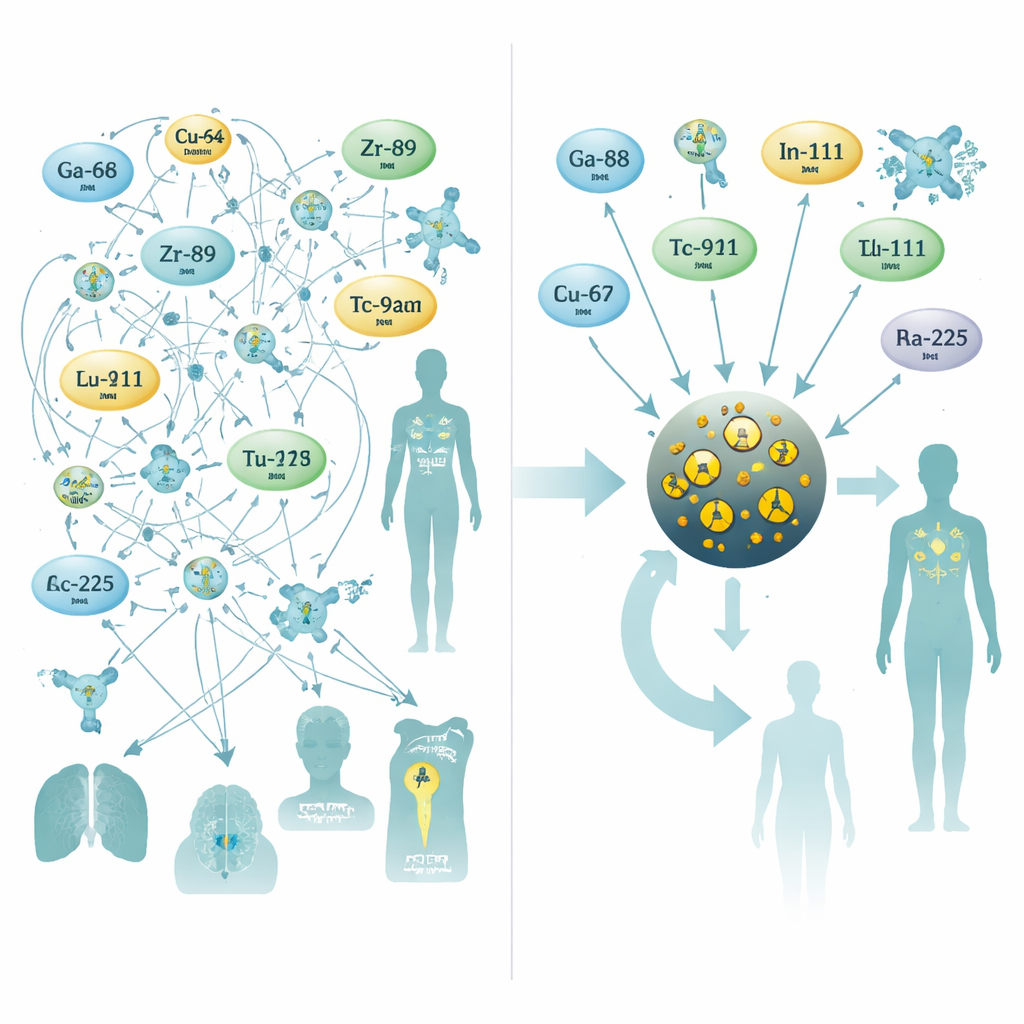
Nanodeeltjes als universeel stopcontact
Om dit aan te pakken, richtten de onderzoekers zich op zeer kleine ijzeroxide‑nanodeeltjes, een materiaal dat al onderzocht is als MRI‑contrastmiddel. Ze ontwierpen deeltjes met een ijzeroxidekern van ongeveer drie nanometer breed, omhuld met een coating van citraatmoleculen die ze stabiel houdt in de bloedbaan. Tijdens een enkele, tien minuten durende microwave‑geassisteerde synthesestap doopten ze de kern met één van tien verschillende radioactieve metalen die vaak worden gebruikt voor PET, SPECT of interne radiotherapie. Dit éénpotproces leverde consistent gevormde deeltjes met hoge opbrengsten en, cruciaal, uitstekende stabiliteit in menselijk serum—even voor uitdagende therapieisotopen zoals radium‑223 en actinium‑225, waarvan de vervalproducten vaak ontsnappen aan traditionele chelatoren.
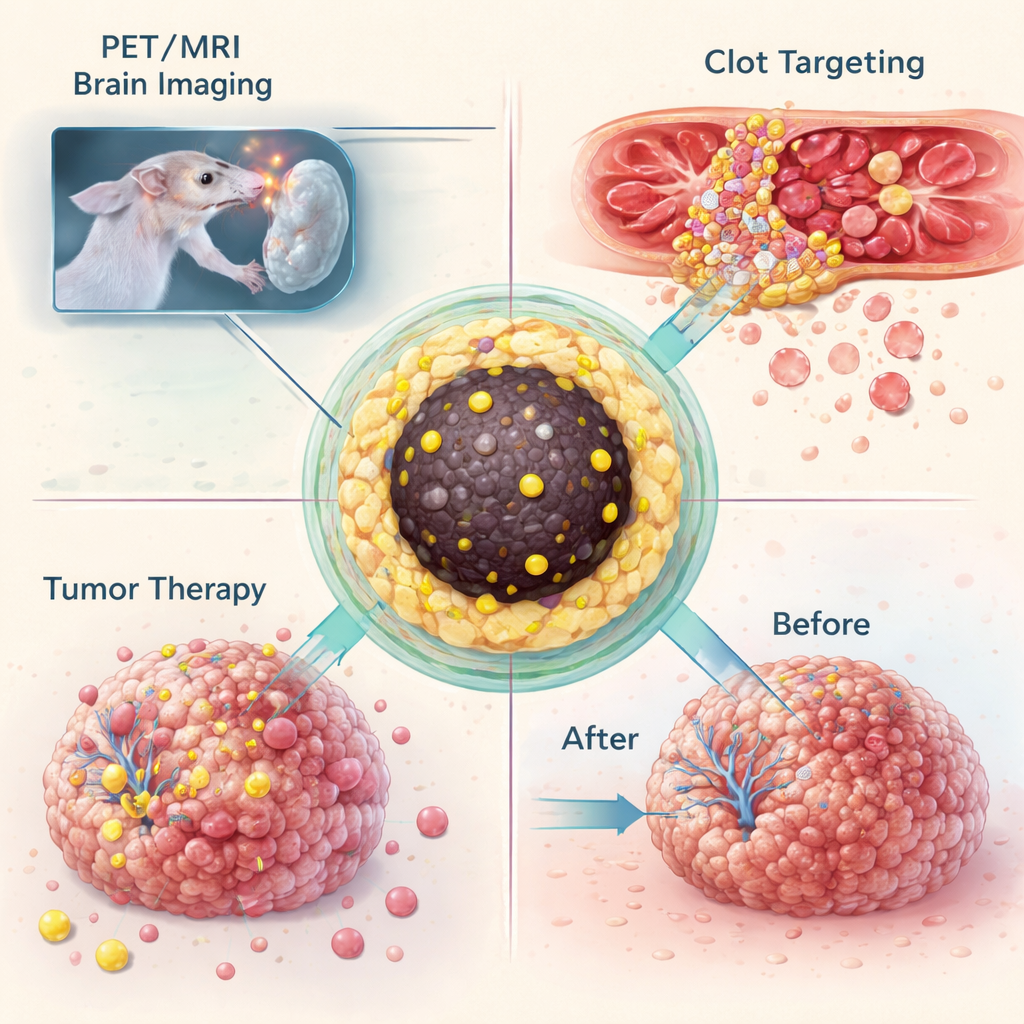
Beeldvorming van stolsel en hersentumoren
Nadat ze hadden aangetoond dat ze veel verschillende isotopen in hetzelfde nanodeeltjeontwerp konden vasthouden, testte het team wat deze "nanotracers" in levende dieren konden doen. In een muismodel van glioblastoom, een dodelijke hersentumor, werden deeltjes gelabeld met gallium‑68 in de bloedbaan geïnjecteerd en afgebeeld met gecombineerde PET en MRI. De deeltjes stapelden zich op in tumoren die groot genoeg waren om de bloed‑hersenbarrière te verstoren, waardoor dezelfde formulering zowel helder MRI‑contrast als een gevoelig PET‑signaal kon leveren. In een afzonderlijk experiment werden de deeltjes chemisch aangepast zodat ze via een zeer selectieve click‑reactie aan een antilichaam konden koppelen dat zich richt op geactiveerde bloedplaatjes in bloedstolsels. In muizen met een beschadigde halsslagader leverde deze tweestaps "pretargeting"‑strategie duidelijke PET‑signalen op de stolselplaats, terwijl controledieren geen dergelijk hotspot toonden.
Van diagnose naar behandeling en veiligere uitscheiding
Hetzelfde platform werd ook gebruikt om behandeling te leveren. Toen nanopartikels beladen met lutetium‑177 direct in glioblastoomtumoren van muizen werden geïnjecteerd, bleven de deeltjes grotendeels in de tumormassa voor ten minste twee weken aanwezig. In die periode groeiden onbehandelde tumoren tot meerdere keren hun oorspronkelijke grootte, terwijl behandelde tumoren stopten met groeien, wat suggereert dat de gelokaliseerde stralingsdosis voldoende was om de progressie te stoppen. Met het oog op het feit dat herhaalde behandelingen de lever en milt met ijzer kunnen overbelasten, stelden de onderzoekers daarna de synthesecondities bij om nog kleinere deeltjes te maken—ongeveer vier tot vijf nanometer groot—die klein genoeg zijn om door de nieren gefilterd te worden. Deze verkleinde deeltjes hielden hun radioactieve lading nog steeds goed vast maar werden snel in de blaas uitgescheiden, waardoor langdurige ophoping in belangrijke organen werd verminderd.
Wat dit kan betekenen voor toekomstige kankerzorg
Voor niet‑specialisten is de kernboodschap dat de onderzoekers een enkel, flexibel nanodeeltjesplatform hebben ontwikkeld dat met veel verschillende radioactieve metalen gecombineerd kan worden zonder de chemie telkens opnieuw uit te vinden. In diermodellen kan hetzelfde basale deeltje helpen bij het opsporen van hersentumoren, het belichten van bloedstolsels, het rechtstreeks afleveren van straling in tumoren en zelfs worden afgestemd om het lichaam via de nieren te verlaten. Hoewel er meer werk nodig is voordat deze aanpak patiënten bereikt, biedt het een veelbelovende route naar het ontwerpen van families van diagnostische en therapeutische middelen die hetzelfde gedrag in het lichaam delen en alleen verschillen in het soort straling dat ze dragen. Die consistentie kan ontwikkeling vereenvoudigen, veiligheidstesten verbeteren en uiteindelijk geavanceerde nucleaire geneeskundige instrumenten breder beschikbaar maken.
Bronvermelding: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Trefwoorden: radiotheranostiek, nanodeeltjes, PET‑beeldvorming, glioblastoom, gerichte radiotherapie