Clear Sky Science · nl
Versnelde en gelokaliseerde synucleïnopathie in een hybride muismodel: implicaties voor positronemissietomografie-studies
Waarom dit onderzoek ertoe doet
De ziekte van Parkinson staat vooral bekend om tremoren en bewegingsproblemen, maar diep in de hersenen begint ze met kleine veranderingen die moeilijk te zien zijn. Artsen hebben dringend manieren nodig om die veranderingen vroeg op te sporen en nieuwe geneesmiddelen snel te testen. Deze studie beschrijft een verfijnd muismodel dat in slechts enkele weken belangrijke kenmerken van Parkinson‑achtige hersenschade reproduceren en dat in een zeer specifieke hersenregio plaatsvindt, afgestemd op gebruik met geavanceerde hersenscans genaamd PET‑beeldvorming. 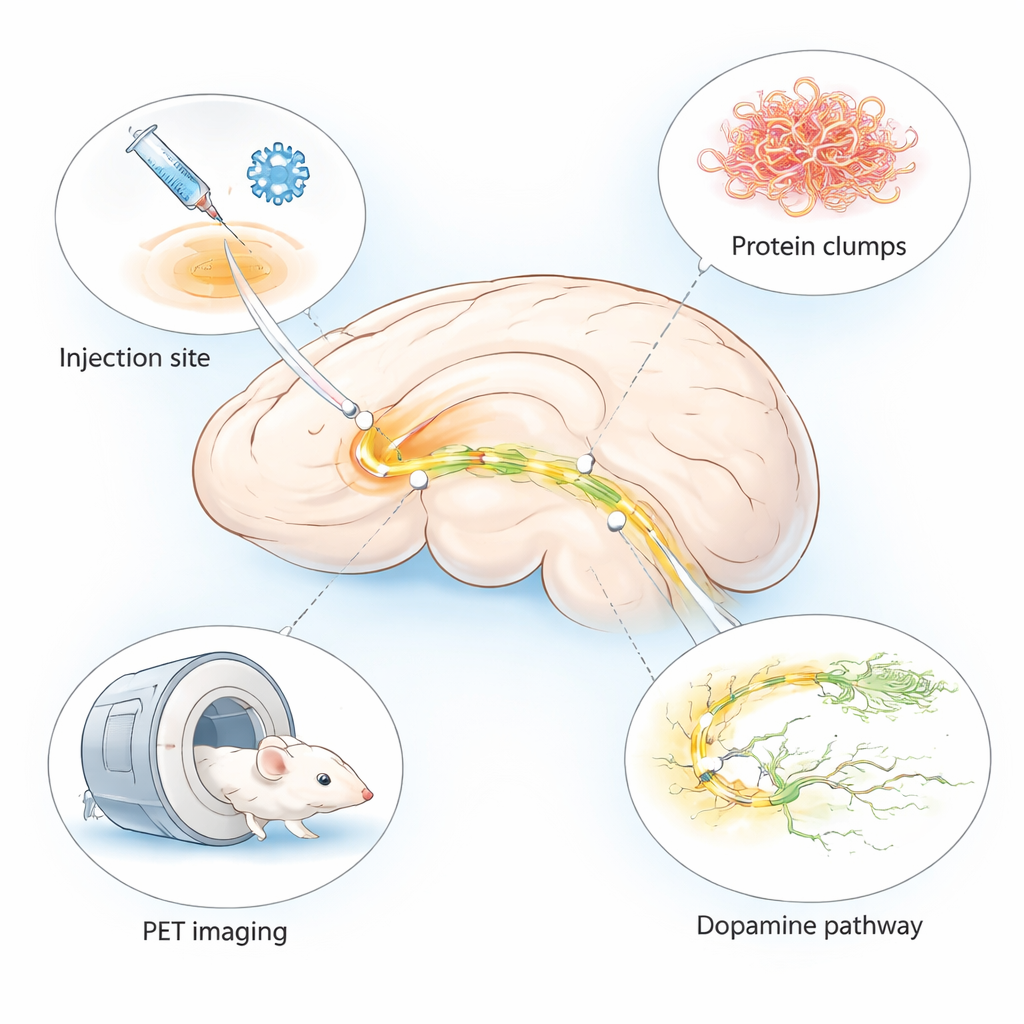
Een sneller, meer gefocust ziektmodel opbouwen
Veel bestaande diermodellen van de ziekte van Parkinson hebben maanden nodig voordat symptomen optreden of tonen niet het volledige scala aan hersenveranderingen die bij patiënten worden gezien. De auteurs combineerden twee gevestigde benaderingen in één "hybride" model. Ze injecteerden een onschadelijk virus dat hersencellen menselijke alfa‑synucleïne laat produceren — een eiwit dat samenklontert bij Parkinson — samen met vooraf gevormde fibrillen, die fungeren als zaden die verdere samenklontering op gang brengen. Beide werden toegediend in een kleine, bewegingsgerelateerde regio genaamd de substantia nigra aan één kant van de muizenhersenen. Dit ontwerp veroorzaakt lokale maar intense ziekteachtige veranderingen aan de geïnjecteerde kant, terwijl de andere kant relatief gezond blijft voor vergelijking.
Het volgen van eiwitklonten en stervende zenuwcellen
Al binnen twee weken na injectie vertoonden de muizen hoge niveaus van menselijke alfa‑synucleïne en diens abnormale, gefosforyleerde vorm in het doelgebied van de hersenen. Onder de microscoop zagen de onderzoekers structuren die leken op Lewy‑lichamen en Lewy‑neurieten, die kenmerkend zijn voor de ziekte van Parkinson. In de daaropvolgende weken namen deze abnormale afzettingen toe. Tegelijkertijd begonnen zenuwcellen die de boodschapperdopamine produceren — cruciaal voor soepele beweging — te verdwijnen. Merkers voor deze cellen daalden tegen week vijf tot ongeveer 60 procent van het niveau aan de onaangetaste kant, wat een duidelijke, progressieve achteruitgang van het dopaminesysteem bevestigt.
Ontsteking, vervagende synapsen en uitgeputte energiecentrales
De immuuncellen van de hersenen, microgliacellen genaamd, schakelden rond het beschadigde gebied ook over naar een sterk actieve, ontstekingsgedreven staat. Kleuringen voor meerdere ontstekingsgerelateerde eiwitten waren veel sterker nabij alfa‑synucleïneafzettingen dan aan de tegenovergestelde kant van de hersenen. Later in het proces detecteerde het team een verlies van synapsen — de kleine contactpunten waar zenuwcellen communiceren — en aanwijzingen dat mitochondriën, de energiecentrales van de cellen, niet goed werkten. Samen tonen deze bevindingen dat het model niet alleen eiwitklonten creëert; het legt ook de kettingreactie vast van ontsteking, falende verbindingen en energieproblemen die bijdragen aan het afsterven van zenuwcellen bij de ziekte van Parkinson. 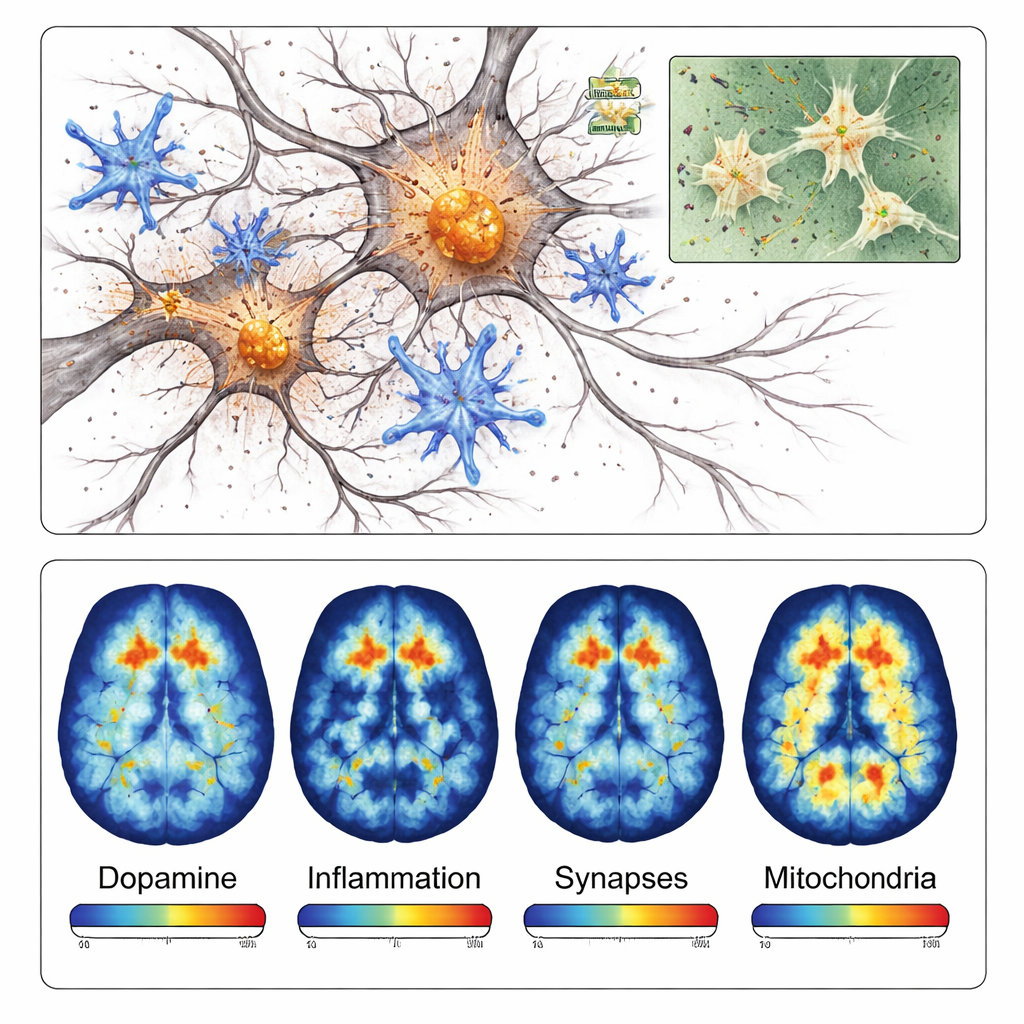
PET‑scanners aan het werk zetten
Aangezien dit model gelokaliseerd is en snel ontwikkelt, is het bijzonder goed geschikt voor positronemissietomografie (PET), een scanttechniek die specifieke moleculen in levende hersenen kan meten. De onderzoekers testten vier verschillende PET‑tracers die binden aan dopaminerge zenuwuiteinden, ontstoken microgliacellen, synaptische eiwitten en mitochondriale enzymen. In elk geval toonden PET‑scans lagere of hogere signalen aan de geïnjecteerde kant op manieren die overeenkwamen met de microscoopbevindingen. Zo liet de tracer die gericht is op dopamineroutes ongeveer 40 procent minder signaal zien aan de beschadigde kant, terwijl de ontstekingstracer meer dan 40 procent hoger signaal in het getroffen gebied aantoonde.
Wat dit betekent voor patiënten en toekomstige behandelingen
Dit nieuwe muismodel brengt binnen een korte tijdsperiode veel van de belangrijkste veranderingen samen die zich bij mensen met de ziekte van Parkinson over jaren ontwikkelen. Omdat de schade beperkt blijft tot een klein, goed omschreven gebied en met PET‑scans gevolgd kan worden, kunnen onderzoekers nieuw beeldvormingsmateriaal en potentiële therapieën efficiënter testen. Hoewel geen enkele muis de menselijke aandoening volledig kan nabootsen, biedt deze benadering een krachtig, praktisch instrument om de kloof tussen fundamenteel laboratoriumwerk en menselijke studies te overbruggen, en zo uiteindelijk te helpen bij het verfijnen van diagnose en het versnellen van de zoektocht naar betere behandelingen.
Bronvermelding: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Trefwoorden: Ziekte van Parkinson, alfa-synucleïne, synucleïnopathie, PET-beeldvorming, muismodel