Clear Sky Science · nl
Differentiaalvergelijkingsmodellen van SARS-CoV-2-replicatiedynamiek en efficiëntie van antivirale middelen
Waarom cijfers ertoe doen bij een nieuw virus
Toen COVID-19 verscheen, konden artsen zien wat het virus met patiënten deed, maar ze konden niet gemakkelijk voorspellen wie erg ziek zou worden of wanneer een geneesmiddel het beste gegeven moest worden. Dit overzichtsartikel beschrijft hoe onderzoekers virusmetingen van patiënten, dieren en celkweken omzetten in wiskundige “films” van de infectie in het lichaam. Deze modellen gebruiken vergelijkingen om te volgen hoe het virus zich vermenigvuldigt, hoe onze cellen en het immuunsysteem reageren, en hoe antivirale middelen en vaccins de uitkomst in ons voordeel kunnen veranderen.
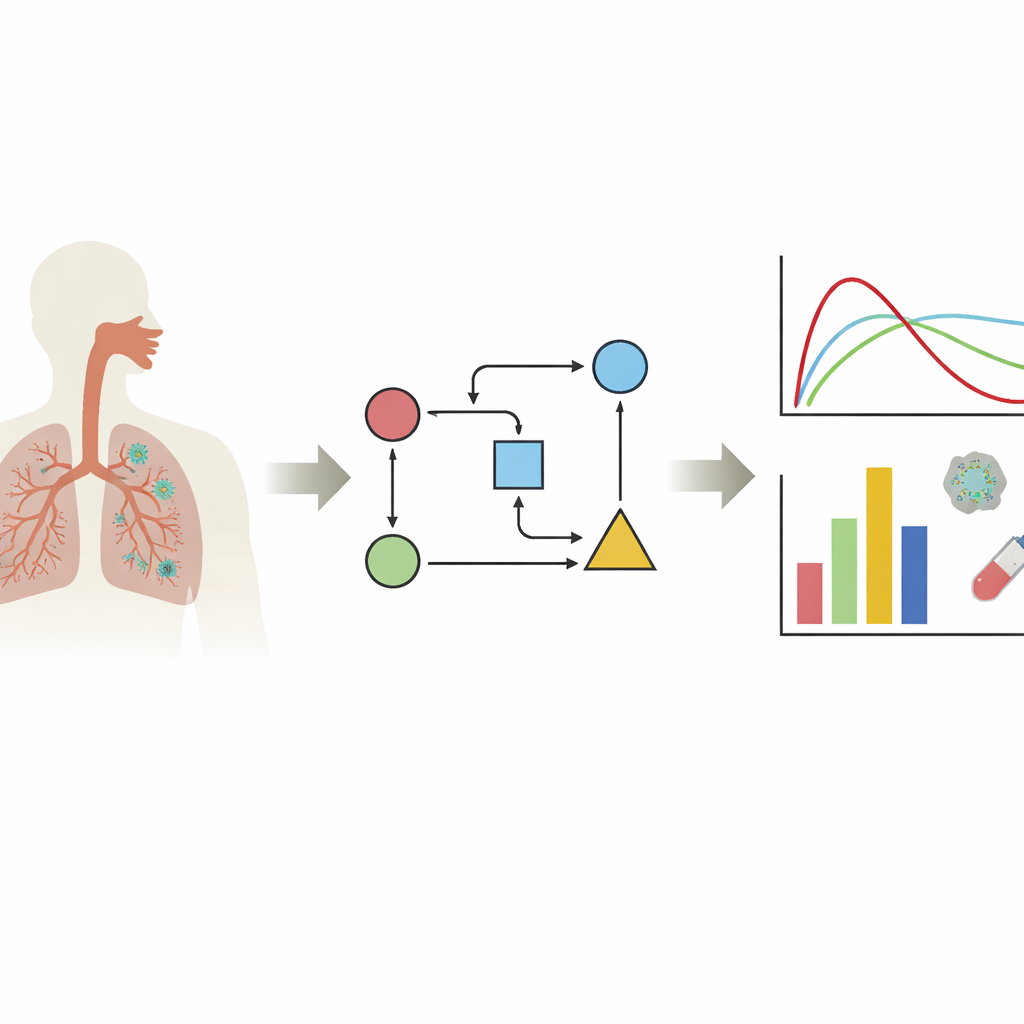
Het virus volgen in het lichaam
De auteurs richten zich op een familielijn van modellen die target cell–limited modellen worden genoemd. Eenvoudig gezegd volgen deze modellen drie hoofdrolspelers: gezonde cellen die geïnfecteerd kunnen worden, cellen die al geïnfecteerd zijn, en vrije deeltjes van het virus. Door werkelijke gegevens over virale niveaus in deze vergelijkingen te stoppen, kunnen onderzoekers verborgen kenmerken van de infectie schatten: hoe snel het virus cellen infecteert, hoe lang een geïnfecteerde cel virus produceert, en hoe snel het virus wordt opgeruimd. De review toont dat het meeste werk zich concentreert op de weefsels die het belangrijkst zijn voor COVID-19 — de neus en de hogere en lagere luchtwegen — terwijl slechts een paar modellen andere organen onderzoeken. Een belangrijke boodschap is dat virusgedrag er heel verschillend uit kan zien afhankelijk van welk weefsel, welke virusvariant en welke laboratoriumcelijn bestudeerd wordt, zodat er geen enkele “typische” infectiecurve is.
Wat we leren over het immuunsysteem
Veel modellen voegen lagen toe die de vroege verdedigingslinie van het immuunsysteem en de langzamere, meer gerichte reactie voorstellen. Studies die zich richten op de eerste verdedigingslinie suggereren dat een snelle, goed getimede activiteit van aangeboren immuuncellen en signaalmoleculen de infectie kan afremmen, maar zelden alleen kan uitroeien. Ander werk benadrukt de cruciale rol van T-cellen en antilichamen bij het uiteindelijk onder controle krijgen van het virus. De modellen vangen ook een duistere kant: als de gerichte immuunrespons te laat of verkeerd gericht is, kunnen dezelfde middelen die ons zouden moeten beschermen schadelijke “cytokinestormen” aanwakkeren, waarbij een overmaat aan ontstekingssignalen gezond weefsel beschadigt. In deze simulaties bepaalt de fijne balans tussen behulpzame en schadelijke immuunactiviteit vaak of de ziekte mild blijft of levensbedreigend wordt.
Wanneer medicijnen en vaccins het beste werken
Omdat vergelijkingen opnieuw en opnieuw kunnen worden uitgevoerd onder verschillende aannames, zijn ze krachtige instrumenten om behandelstrategieën op de computer te testen voordat ze bij mensen worden geprobeerd. Over vele studies heen komen de modellen overeen op één centraal punt: antivirale middelen werken het beste wanneer ze heel vroeg worden gegeven, vóórdat het virus zijn piek heeft bereikt en de meeste beschikbare cellen heeft geïnfecteerd. Behandelingen die verhinderen dat het virus zijn genetisch materiaal kopieert, komen bijzonder veelbelovend naar voren, vooral in combinatie met andere middelen die via verschillende mechanismen werken. Late behandeling heeft daarentegen in simulaties meestal weinig effect, tenzij meerdere sterke middelen samen worden gebruikt. Vaccinatie wordt consequent voorspeld beter te presteren dan alleen medicijnen, voornamelijk door het immuunsysteem voor te bereiden zodat het het virus snel herkent en hoge viraalniveaus kort houdt.
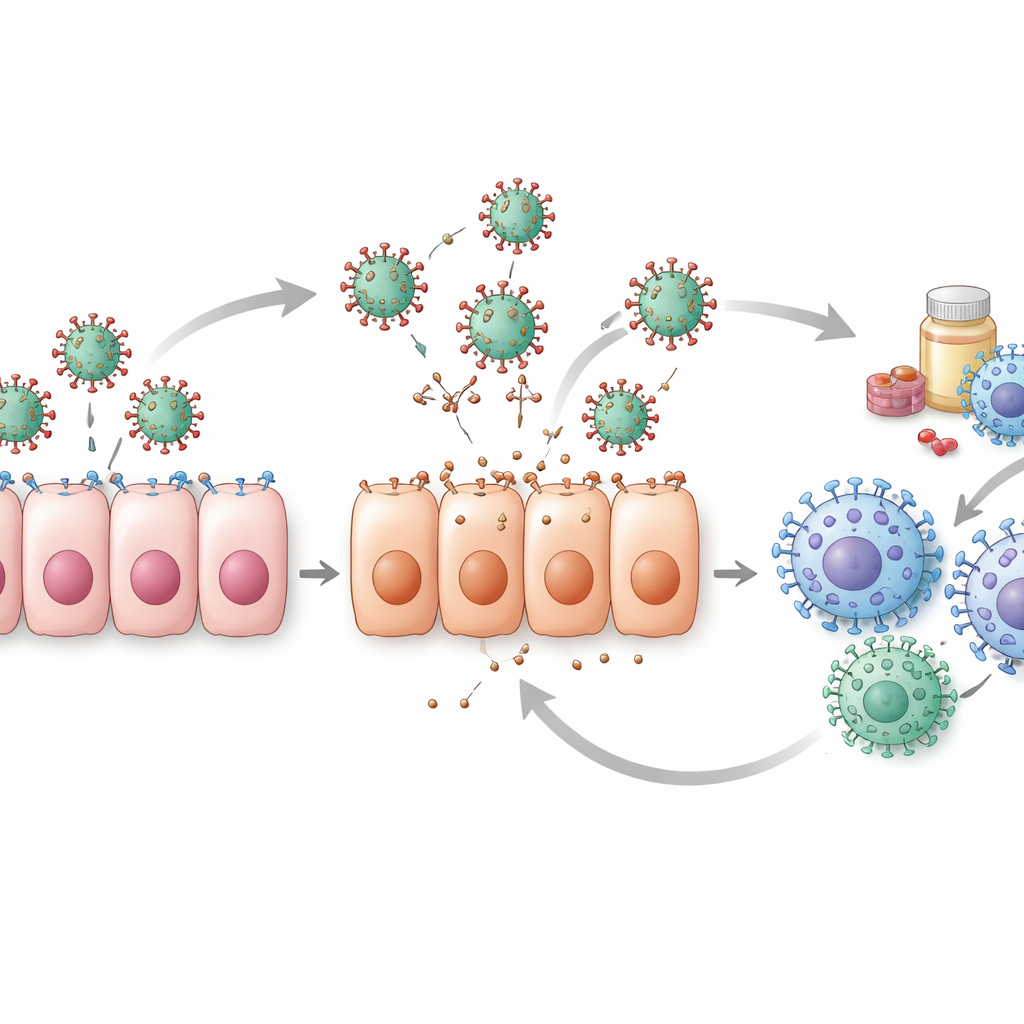
Verborgen uitdagingen in de gegevens
De review werpt ook licht op de zwaktes achter de cijfers. De meeste klinische datasets beginnen pas nadat mensen zich al ziek voelen, wat betekent dat modellen vaak de cruciale eerste dagen van de infectie missen wanneer viraalniveau’s het snelst stijgen. Zonder die vroege metingen kunnen verschillende combinaties van modelparameters dezelfde gegevens verklaren, waardoor het moeilijk is te weten welke verklaring juist is. Slechts een minderheid van de studies voert rigoureuze controles uit om te zien of hun parameterschattingen echt uniek en betrouwbaar zijn. Dierstudies en celkweekexperimenten helpen enkele hiaten op te vullen, vooral voor vroege tijdspunten, maar verschillen tussen soorten en laboratoriumsystemen beperken hoe direct die resultaten op mensen toepasbaar zijn.
Wat dit betekent voor de toekomst
Voor niet‑specialisten is de belangrijkste conclusie dat zorgvuldig opgebouwde wiskundige modellen ons begrip van hoe SARS-CoV-2 zich in het lichaam gedraagt en hoe timing, medicijncombinaties en eerdere vaccinatie uitkomsten beïnvloeden, sterk hebben verbeterd. De modellen zijn het erover eens dat vroege, sterke interventie — vooral via vaccinatie en tijdige antiviralia — het immuunsysteem de beste kans geeft om te winnen, terwijl vertraagde reacties, zowel van het lichaam als van de behandeling, gekoppeld zijn aan ernstigere ziekte. Tegelijk benadrukken de auteurs dat deze instrumenten alleen zo goed zijn als de gegevens die erin worden gevoed. Om ons voor te bereiden op toekomstige varianten of nieuwe virussen, pleiten zij voor rijkere, vroegere klinische bemonstering en bredere immuunmetingen, zodat de “cijfers achter infectie” snellere, nauwkeurigere beslissingen in echte uitbraken kunnen sturen.
Bronvermelding: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Trefwoorden: SARS-CoV-2 viraal dynamica, modellering binnen de gastheer, timing van antivirale therapie, immuunrespons, COVID-19 vaccinatie