Clear Sky Science · nl
Het oplosbare G-eiwit van respiratoir syncytieel virus bevordert virusverspreiding via TLR2-gemedieerde NLRP3-priming en pyroptose
Waarom dit longvirus voor iedereen van belang is
Respiratoir syncytieel virus, of RSV, staat vooral bekend als een winterse bedreiging voor zuigelingen, maar het dwingt ook veel oudere volwassenen en mensen met een verzwakt immuunsysteem tot ziekenhuisopname. Zelfs met nieuwe vaccins en beschermende antilichamen infecteert RSV mensen herhaaldelijk opnieuw en kan het ernstige longschade veroorzaken. Deze studie bekijkt een weinig bekend viraal eiwit, een oplosbare vorm van het RSV G-eiwit, en onthult hoe het op de achtergrond longcellen kan voorbereiden op explosieve ontsteking en het virus efficiënter door de luchtwegen kan laten verspreiden.
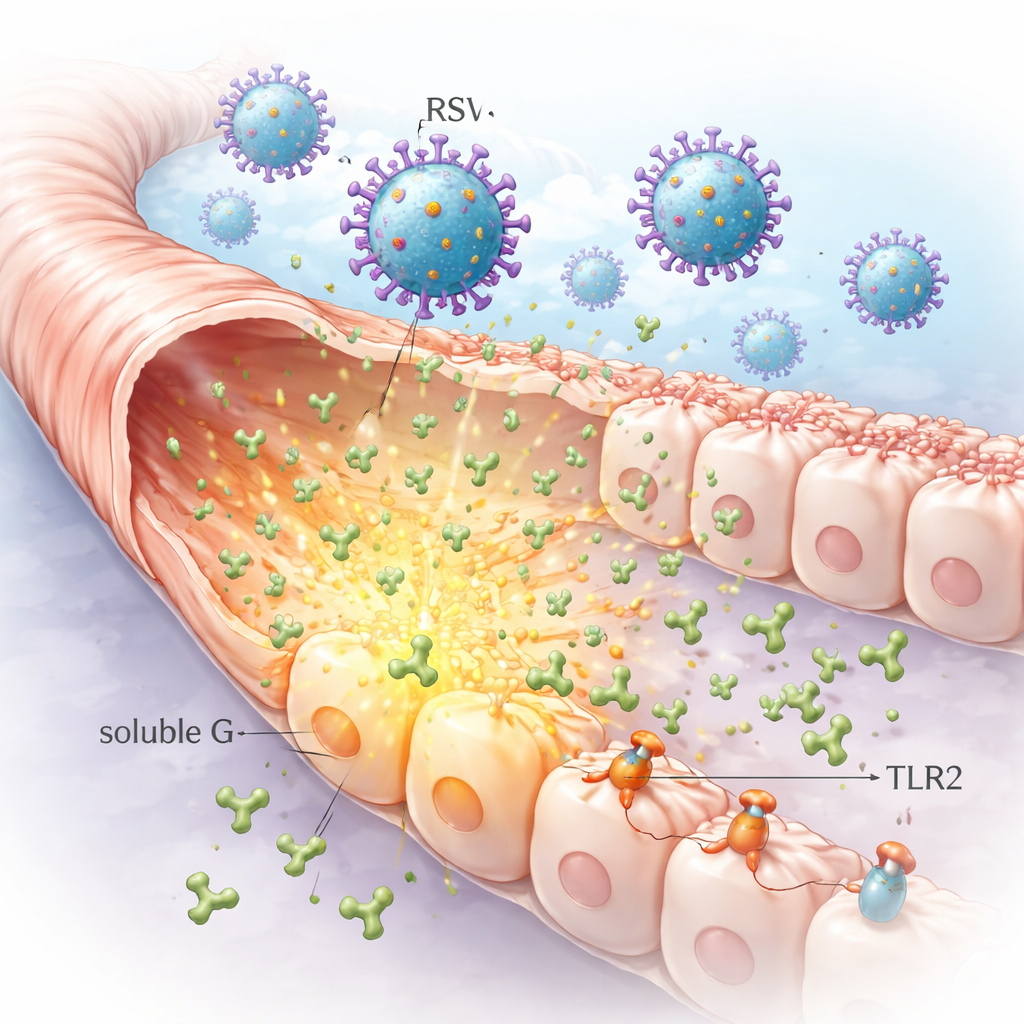
Een uitgescheiden viraal eiwit dat voor de infectie uitreist
RSV draagt een hechteiwit genaamd G op zijn oppervlak dat helpt bij het vasthechten aan cellen in de luchtwegen. Opmerkelijk genoeg geven geïnfecteerde cellen ook grote hoeveelheden van een vrij rondzwevende versie van dit eiwit af, bekend als oplosbaar G. De onderzoekers toonden aan dat longcellen die in het laboratorium geïnfecteerd zijn, zeer hoge niveaus van oplosbaar G in hun omgeving kunnen afgeven. Omdat deze vorm kan wegdiffunderen van de oorspronkelijke infectieplaats, kan het naburige cellen bereiken die nog niet geïnfecteerd zijn, en zo de voorwaarden creëren voor ruimere veranderingen in het longoppervlak dan het virus alleen zou veroorzaken.
Oplosbaar G als een tweevoudige sleutel tot celoppervlakken
Door microscopie, biochemische pull-downtests en enzymatische behandelingen te combineren, brachten de onderzoekers in kaart hoe oplosbaar G zich aan cellen hecht. Ze vonden dat het kan binden aan suikerketens genaamd glycosaminoglycanen, evenals aan een bekend RSV-receptor genaamd CX3CR1. Cruciaal is dat oplosbaar G ook bindt aan een patroonherkennend molecuul op immuun- en luchtwegcellen dat TLR2 heet. Een klein motief in het G-eiwit, bekend als CX3C, bleek belangrijk voor sterke binding aan CX3CR1 en voor robuuste aantrekking van TLR2. Dit betekent dat oplosbaar G eerst losjes op het celoppervlak kan worden gevangen en vervolgens meer specifieke receptoren kan activeren die bepalen hoe cellen op bedreigingen reageren.
Longcellen klaarmaken voor een ontstekingsachtige celdood
De activering van TLR2 door oplosbaar G bleek verre van onschadelijk. In reporter-immuuncellen en menselijke longcellijnen activeerde oplosbaar G de MyD88–NF-κB-signaleringsroute stroomafwaarts van TLR2, wat leidde tot de afgifte van ontstekingsboodschappers zoals IL-6 en IL-8. Tegelijkertijd verhoogde het de productie van componenten van een moleculair "alarmsysteem" genaamd het NLRP3-inflammasoom en van enzymen die reactieve moleculen genereren zoals stikstofoxide en zuurstofradicalen. Op zichzelf veroorzaakten deze veranderingen slechts milde schade. Maar wanneer geprimede cellen later met RSV werden geïnfecteerd, veroorzaakte de tweede slag volledige assemblage van het inflammasoom, activatie van het enzym caspase‑1, vorming van poriën in het celmembraan en een felle vorm van celdood die bekendstaat als pyroptose. Dit proces maakte gaten in de cellen, liet ontstekingsinhoud ontsnappen en ging gepaard met grotere hoeveelheden infectieus virus dat in de kweekvloeistof vrijkwam.
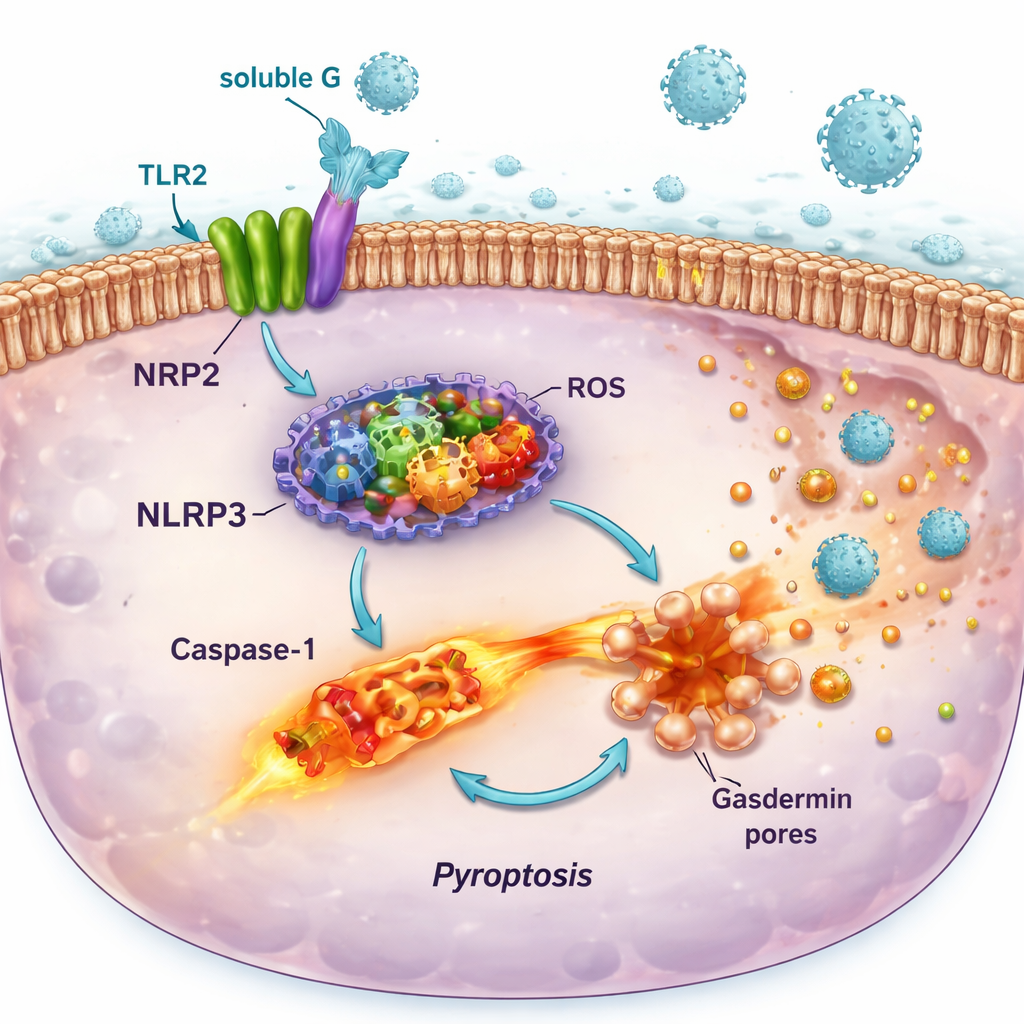
Hoe deze ketenreactie longziekte kan verergeren
Het pro-doodseffect van oplosbaar G was het sterkst in luchtwegepitheelcellen—de cellen die RSV bij voorkeur infecteert—en hing af van het NLRP3-inflammasoom, aangezien een specifieke NLRP3-remmer grotendeels het celoverleven herstelde. Daarentegen ondergingen bepaalde immuuncellen die rijk zijn aan TLR2 maar arm aan de CX3CR1-receptor onder dezelfde omstandigheden geen sterke lytische celdood. Dit patroon suggereert dat RSV oplosbaar G gebruikt om selectief de beschermende bekleding van de luchtwegen te verzwakken en te vernietigen, terwijl sommige immuuncellen behouden blijven en door kunnen gaan met het produceren van signaalstoffen. Het resultaat is een longomgeving met meer ontsteking, meer celfragmenten en meer kansen voor nieuwe virusdeeltjes om te ontsnappen en naburige cellen te infecteren.
Wat dit betekent voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat RSV niet uitsluitend afhankelijk is van directe schade door virale binnendringing. Door grote hoeveelheden oplosbaar G-eiwit vrij te geven, kan het nabijgelegen cellen via TLR2 "zachter maken", waardoor ze vatbaarder worden voor een inflammatoire celdood en viruslekkage. Dit werk identificeert meerdere stappen in die keten—oplosbaar G zelf, het CX3C-motief, TLR2 en het NLRP3-inflammasoom—als potentiële medicijntargets. In principe zouden therapieën die de interactie tussen oplosbaar G en TLR2 blokkeren, of die NLRP3-activiteit dempen, zowel longschade als virusverspreiding kunnen verminderen. Zulke benaderingen zouden op termijn bestaande RSV-vaccins en antilichamen kunnen aanvullen en betere bescherming kunnen bieden voor de jongsten en meest kwetsbare patiënten.
Bronvermelding: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Trefwoorden: respiratoir syncytieel virus, oplosbaar G-eiwit, TLR2-inflammasoom, pyroptose, longontsteking