Clear Sky Science · nl
Menopauzale hormoontherapie en het risico op neuropsychiatrische aandoeningen: een Mendeliaanse randomisatie-studie gericht op geneeswatervariabelen
Waarom dit onderzoek ertoe doet
Veel vrouwen vragen zich af of het innemen van hormonen rond de menopauze hun hersenen beschermt of juist risico’s zoals geheugenverlies, depressie of angst vergroot. Ook artsen zijn verdeeld, omdat eerdere onderzoeken tegenstrijdige resultaten hebben opgeleverd. Dit artikel gebruikt een op genetica gebaseerde benadering, vergelijkbaar in opzet met een langdurige gerandomiseerde studie, om een eenvoudige vraag te stellen: als de oestrogeenreceptoren in de hersenen worden beïnvloed zoals menopauzale hormoontherapie dat doet, verandert dan het risico op de ziekte van Alzheimer of veelvoorkomende psychische problemen?
De puzzel rond hormonen en de hersenen
Vrouwen lopen meer risico dan mannen op depressie, angst en de ziekte van Alzheimer. Een toonaangevende verklaring is dat oestrogeen, een belangrijk vrouwelijk geslachtshormoon, de hersenen levenslang helpt vormen en mogelijk beschermt—totdat de niveaus rond de middelbare leeftijd fluctueren of dalen. Tijdens de overgang naar de menopauze gebruiken veel vrouwen menopauzale hormoontherapie (MHT) om klachten zoals opvliegers en slaapproblemen te verlichten. Toch zijn de bevindingen over of MHT de hersengezondheid helpt of schaadt niet eensluidend: sommige studies vonden een verhoogd dementierisico, andere suggereerden een beschermend effect en veel studies vonden geen duidelijk effect. Deze inconsistenties kunnen voortkomen uit korte duur van trials, verschillende medicijnformuleringen en het feit dat vrouwen met ernstiger klachten vaker hormonen voorgeschreven krijgen.
Genen als natuurlijk experiment
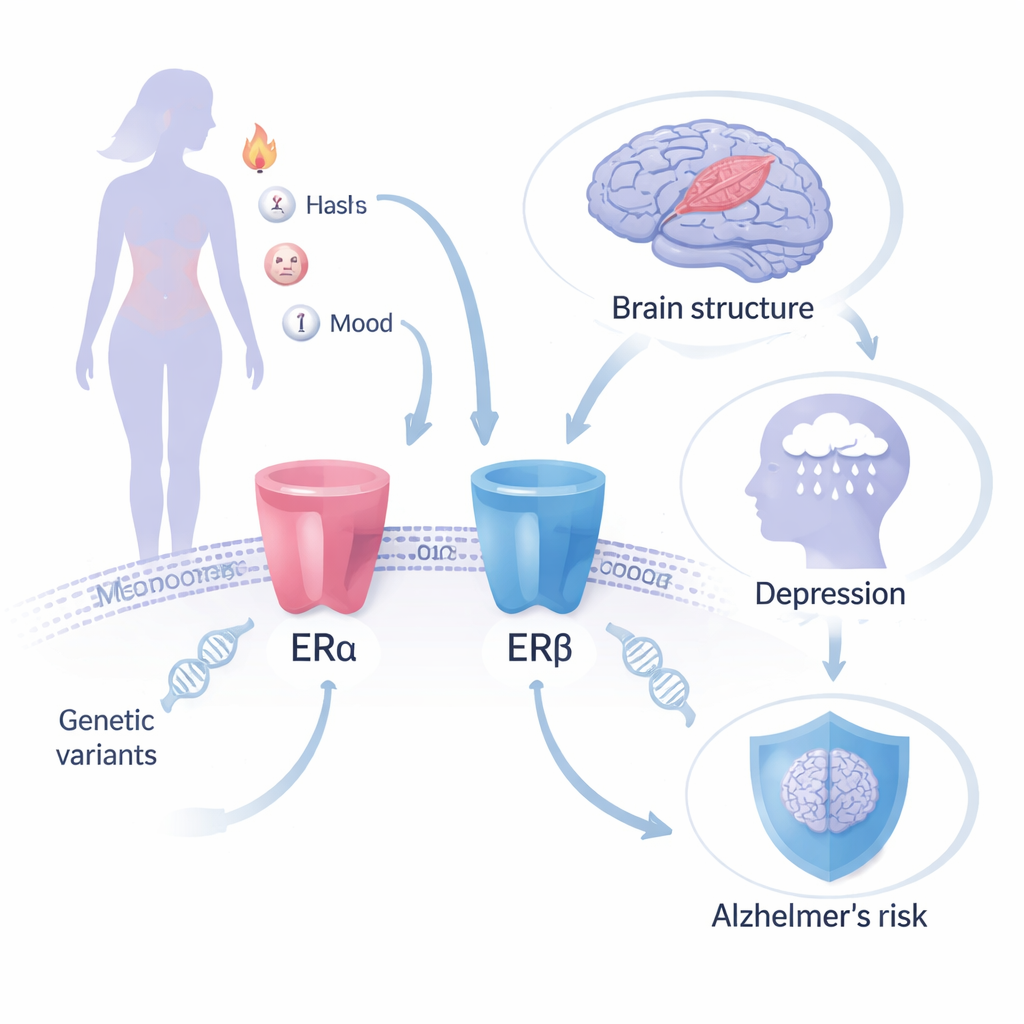
In plaats van vrouwen te volgen die hormoonpillen gebruiken, zetten de onderzoekers Mendeliaanse randomisatie in, een methode die natuurlijke genetische verschillen gebruikt als surrogaat voor een levenslange, willekeurig toegewezen “behandeling”. Ze richtten zich op twee eiwitten in het lichaam die oestrogeenreceptoren worden genoemd—ERα en ERβ—die door MHT worden aangesproken. Specifieke genetische varianten in de genen die deze receptoren coderen (ESR1 en ESR2) hebben bekende effecten op ‘downstream’ eigenschappen die veranderen wanneer oestrogeen werkzaam is, zoals botdichtheid, een bloedproteïne dat geslachtshormonen bindt, en hemoglobineniveaus. Door te volgen hoe deze receptor-gerelateerde varianten samenhangen met grote genetische datasets over de ziekte van Alzheimer, hersenstructuur, depressie en angst, kon het team inschatten hoe het manipuleren van elke receptor het risico op lange termijn voor hersen- en geestelijke gezondheid zou kunnen beïnvloeden.
Wat het genetische bewijs aantoonde
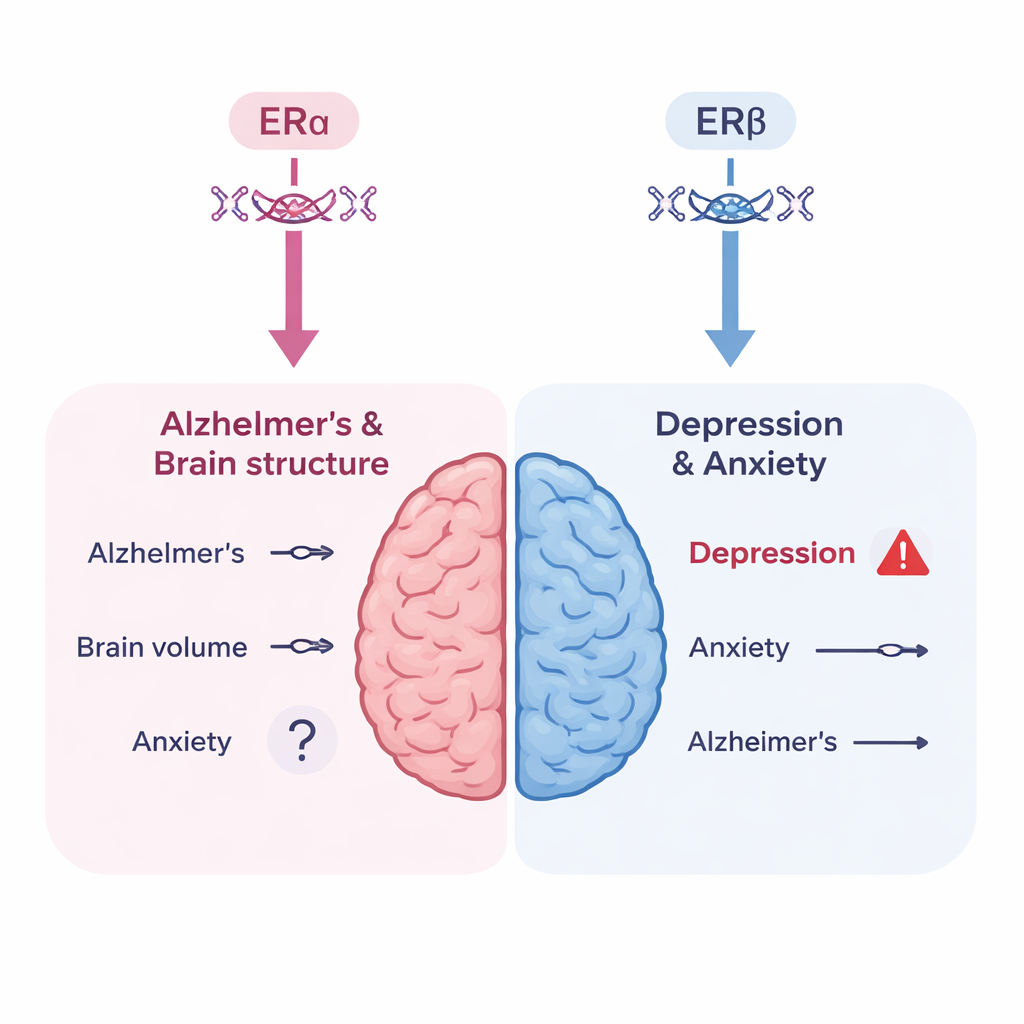
De auteurs bouwden drie genetische instrumenten: twee die ERα-activiteit vastleggen (via varianten gekoppeld aan botdichtheid en aan sex hormone–binding globulin) en één die ERβ-activiteit vastlegt (via een variant gekoppeld aan hemoglobine). Deze combineerden ze met enkele van de grootste beschikbare genome-wide associatiestudies van de ziekte van Alzheimer, MRI-maatregelen van de hersenen (totale grijze massa, hippocampusvolume en witte stof‑‘vlekken’ geassocieerd met veroudering), depressie en angst. Overall vonden ze geen overtuigend bewijs dat genetisch gesimuleerde veranderingen in een van beide oestrogeenreceptoren het risico op de ziekte van Alzheimer wezenlijk veranderden of deze hersenstructuurmaten beïnvloedden. Enkele zwakke signalen voor veranderingen in grijze massa of hippocampusvolume weerstonden de statistische correctie niet, wat suggereert dat die mogelijk door toeval verklaard worden in plaats van een echt biologisch effect.
Een alarmsignaal voor depressierisico
Het beeld was anders voor stemming. Toen de onderzoekers keken naar ERβ-activiteit, zoals vastgelegd door de hemoglobine‑gebaseerde genetische proxy, zagen ze een statistisch robuuste koppeling met een hoger risico op depressie. Deze bevinding past bij wat bekend is over waar ERβ het meest actief is in de hersenen—regio’s zoals de hippocampus en thalamus die sterk betrokken zijn bij stemmingsregulatie. De auteurs wijzen er echter op dat de hemoglobineproxy imperfect is: laag hemoglobine kan zelf bijdragen aan vermoeidheid en een sombere stemming, wat het beeld kan vervagen. Ze vonden geen sterk genetisch bewijs dat ERα-activiteit op zichzelf het depressierisico verhoogt, en slechts een suggestieve, niet-definitieve aanwijzing dat ERα mogelijk gerelateerd is aan angst. Belangrijk is dat genetische effecten die vanaf de geboorte gestaag werken niet identiek zijn aan het starten van hormoontherapie op middelbare leeftijd, dus deze resultaten moeten niet worden opgevat als een directe voorspelling voor een specifiek MHT‑regime.
Wat dit betekent voor vrouwen en hun artsen
Vertaald naar dagelijkse beslissingen suggereert deze studie dat het richten op oestrogeenreceptoren op manieren die lijken op MHT niet duidelijk het levenslange risico op de ziekte van Alzheimer verhoogt of verlaagt, en geen grote veranderingen in hersenstructuur veroorzaakt, althans in mensen van Europese afkomst. Tegelijkertijd benadrukt het resultaat dat ERβ koppelt aan depressie dat hormoonsensitieve hersencircuits verbonden zijn met stemming, en dat verschillende oestrogeenreceptoren verschillende implicaties voor de geestelijke gezondheid kunnen hebben. Het werk vervangt geen klinische trials, maar biedt een krachtig genetisch ‘realiteitscheck’ dat kan helpen toekomstige hormoontherapieën te verfijnen en onderzoek te sturen naar veiligere, meer op maat gemaakte behandelingen voor vrouwen die de menopauze doormaken.
Bronvermelding: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
Trefwoorden: menopauzale hormoontherapie, oestrogeenreceptoren, Ziekte van Alzheimer, risico op depressie, Mendeliaanse randomisatie