Clear Sky Science · nl
STAR (stroma-tumor AI risk) beoordeling: associatie van AI-afgeleide tumor-stroma verhouding met patiëntoverleving biedt toegevoegde prognostische waarde boven KELIM bij epitheliale eierstokkanker
Waarom de "buurt" rond een tumor ertoe doet
Als we aan kanker denken, zien we vaak een massa slechte cellen voor ons. Maar tumoren bestaan in een drukke omgeving van ondersteunend weefsel, bloedvaten en immuuncellen, het zogeheten stroma. Deze studie stelt een eenvoudige maar krachtige vraag: kunnen we de balans tussen tumorcellen en dit omliggende weefsel — gemeten met kunstmatige intelligentie (AI) op routine‑microscooppreparaten — gebruiken om te voorspellen welke patiënten met eierstokkanker waarschijnlijk betere of slechtere uitkomsten hebben, nog voordat de behandeling begint?
Een nieuwe manier om standaardbiopreparaten te lezen
Vrouwen met epitheliale eierstokkanker krijgen meestal weefsel verwijderd tijdens een operatie of biopsie. Die monsters worden gekleurd en onder de microscoop onderzocht in elk ziekenhuis. De onderzoekers concentreerden zich op een kenmerk dat tumor–stroma verhouding (TSP) heet: welk deel van de afbeelding bestaat uit ondersteunend weefsel vergeleken met kankercellen. In eerder werk schatten pathologen deze verhouding met het blote oog en vonden dat tumoren rijk aan stroma vaak agressiever gedrag vertonen en resistent zijn tegen standaard platinum‑gebaseerde chemotherapie. In de huidige studie gebruikte het team een deep‑learning AI‑systeem om TSP automatisch te meten op gedigitaliseerde snedes, met als doel een handmatige, enigszins subjectieve taak om te zetten in een snelle en reproduceerbare meting die direct bij de diagnose beschikbaar is.
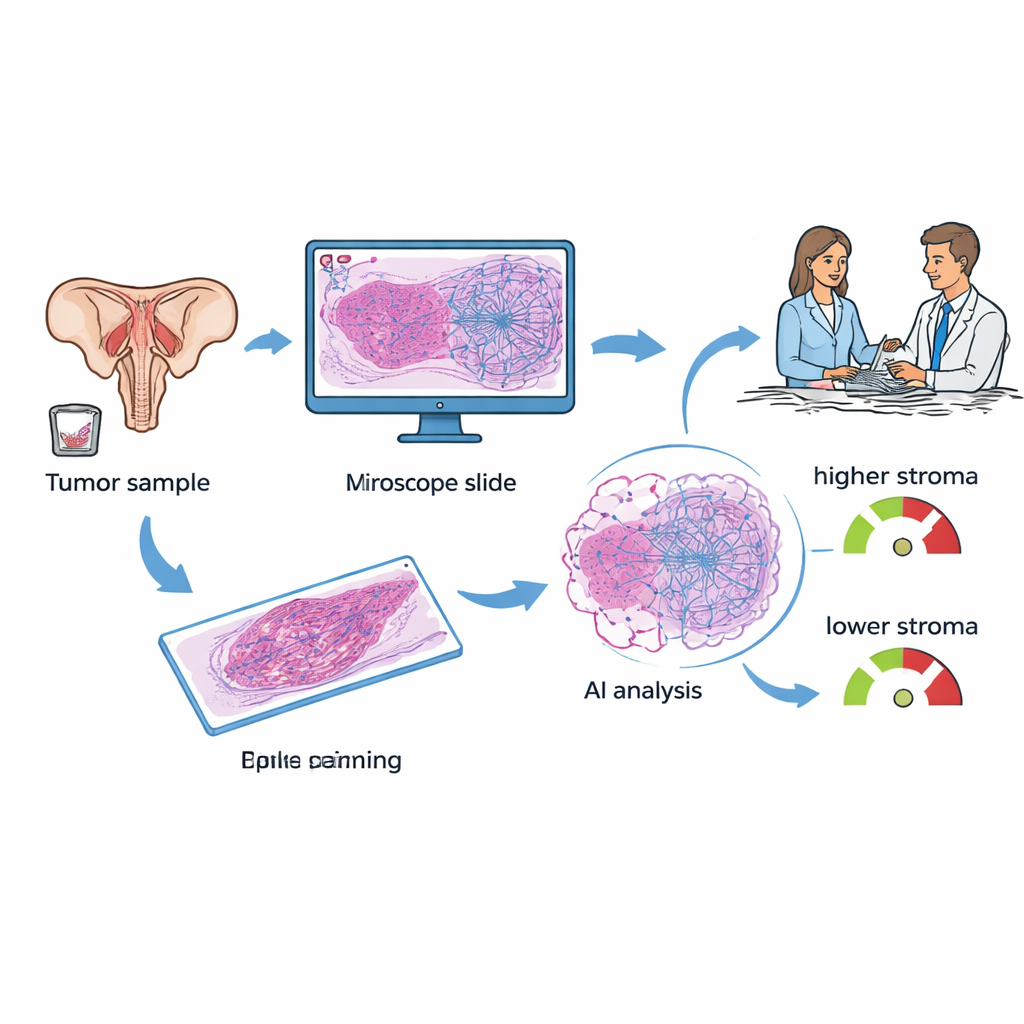
AI‑weefselanalyse vergeleken met een bloedgebaseerde score
Tegenwoordig is een veelbesproken instrument bij eierstokkanker KELIM, een score gebaseerd op hoe snel een bloedmarker genaamd CA‑125 daalt tijdens de eerste 100 dagen van chemotherapie. KELIM is goedkoop en bruikbaar, maar kan pas worden berekend na enkele weken behandeling, en niet alle patiënten hebben voldoende vroege bloedmetingen om de score te genereren. De onderzoekers verzamelden gegevens van 89 vrouwen die in één kankercentrum waren behandeld en zowel weefselsnedes als ten minste drie CA‑125‑metingen hadden. Ze berekenden KELIM voor elke patiënt, lieten een patholoog tumorgebieden op de snedes labelen, en lieten vervolgens het AI‑model TSP schatten, waarbij elk geval werd gecategoriseerd als "stroma‑laag" (minder dan 50% stroma) of "stroma‑hoog" (50% of meer).
AI komt overeen met experts en signaleert hoger risico
De beoordeling van de AI kwam nauw overeen met die van ervaren pathologen: in 94% van de gevallen stemde de geautomatiseerde TSP‑classificatie overeen met de handmatige, een niveau van concordantie dat als uitstekend wordt beschouwd. Toen het team naar de uitkomsten van patiënten keek, bleek dat vrouwen met door AI geclassificeerde stroma‑hoge tumoren significant slechtere totale overleving hadden dan degenen met stroma‑lage tumoren. Statistisch gezien verdubbelde een hoge TSP bijna het sterfterisico tijdens de follow‑up, en dit effect bleef bestaan zelfs nadat rekening was gehouden met de KELIM‑score. Daarentegen hing KELIM in deze real‑world groep samen met resistentie tegen platina‑middelen, maar was niet duidelijk gekoppeld aan de totale overleving.
Wat dit kan betekenen voor behandelingskeuzes
Aangezien TSP kan worden gemeten op routinepreparaten die bij de diagnose zijn genomen, biedt AI‑gebaseerde TSP een manier om risico in te schatten voordat chemotherapie start, mogelijk maanden eerder dan KELIM. Een hoge TSP‑uitslag kan artsen waarschuwen dat een tumor waarschijnlijk agressiever en moeilijker te behandelen is, wat kan leiden tot intensievere monitoring, eerder overwegen van aanvullende therapieën of andere chirurgische strategieën. De methode is ook relatief goedkoop: ze is gebaseerd op bestaande pathologiebeelden en een softwaremodel in plaats van nieuwe laboratoriumtesten. De auteurs stellen dat geautomatiseerde TSP naast andere markers, zoals genetische testen en CA‑125‑trends, gebruikt kan worden om de prognose te verfijnen zonder een grote extra last voor patiënten of pathologieteams.
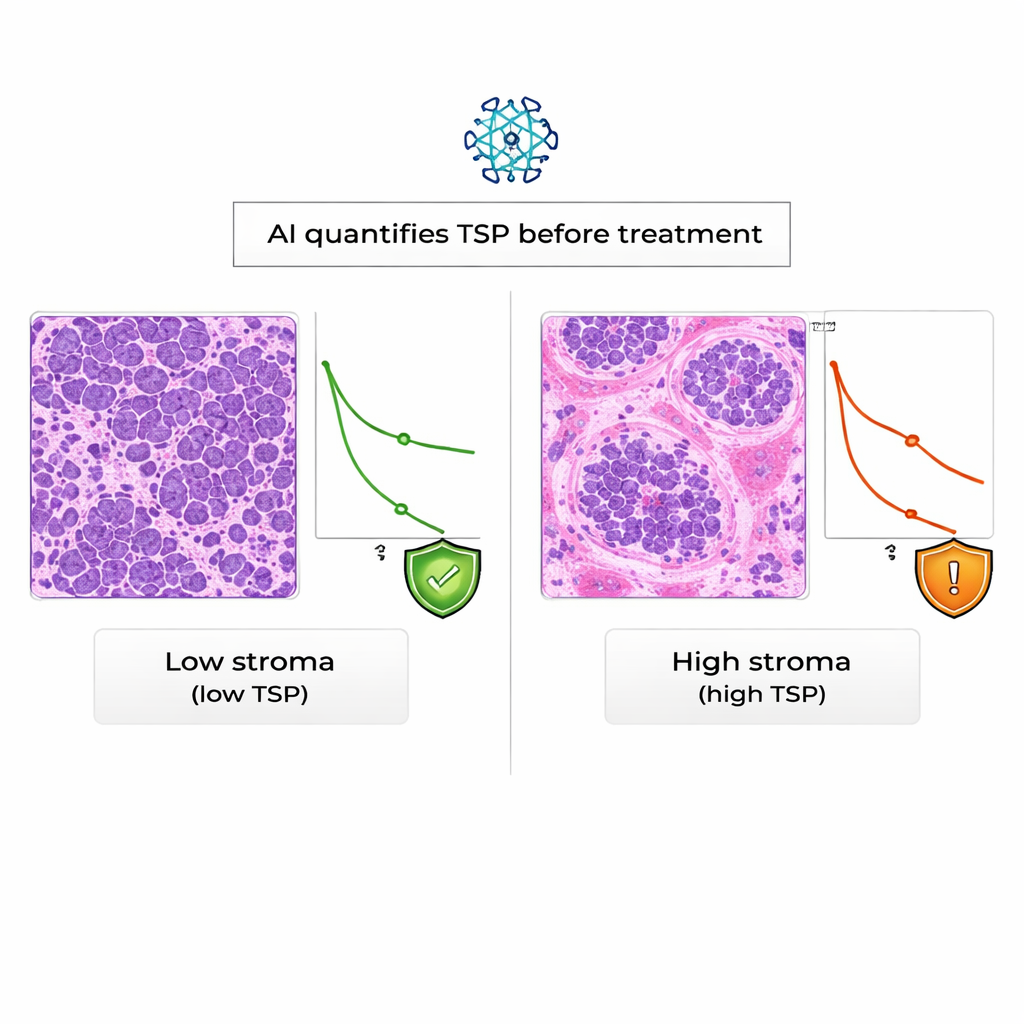
Vooruitblik: slimmer, eerder advies voor patiënten
Voor niet‑specialisten is de kernboodschap dat niet alle eierstokkankers gelijk zijn, en dat het ondersteunende weefsel rond de tumor belangrijke aanwijzingen bevat over het gedrag van de ziekte. Deze studie toont aan dat AI die aanwijzingen betrouwbaar kan lezen op standaardbiopreparaten en dat een stroma‑rijke tumor doorgaans geassocieerd is met een slechtere overleving, onafhankelijk van bestaande bloedgebaseerde scores. Hoewel grotere en meer diverse studies nodig zijn voordat deze aanpak routinezorg wordt, heeft AI‑afgeleide TSP potentie als vroegwaarschuwingssignaal dat artsen kan helpen behandelingsplannen op maat te maken en patiënten vanaf het begin duidelijkere verwachtingen te geven.
Bronvermelding: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Trefwoorden: eierstokkanker, kunstmatige intelligentie, tumormicro‑omgeving, prognostische biomarker, digitale pathologie