Clear Sky Science · nl
Genomische inventarisatie onthult opkomst van een multiresistente dominante lijn bij Proteus mirabilis-populaties
Waarom deze ziekenhuisbacterie voor u van belang is
Voor veel mensen zijn urineweginfecties een af en toe optredende, pijnlijke ergernis. Maar in ziekenhuizen en verzorgingshuizen worden sommige infecties veroorzaakt door taaie bacteriën die aan katheters blijven kleven, meerdere antibiotica weerstaan en zich geruisloos tussen mensen en dieren verspreiden. Deze studie volgt één dergelijke schuldige, Proteus mirabilis, wereldwijd en gebruikt zijn DNA als een reisdagboek om te laten zien hoe één moeilijk te behandelen familielijn in de loop van de afgelopen eeuw stilletjes dominant is geworden.
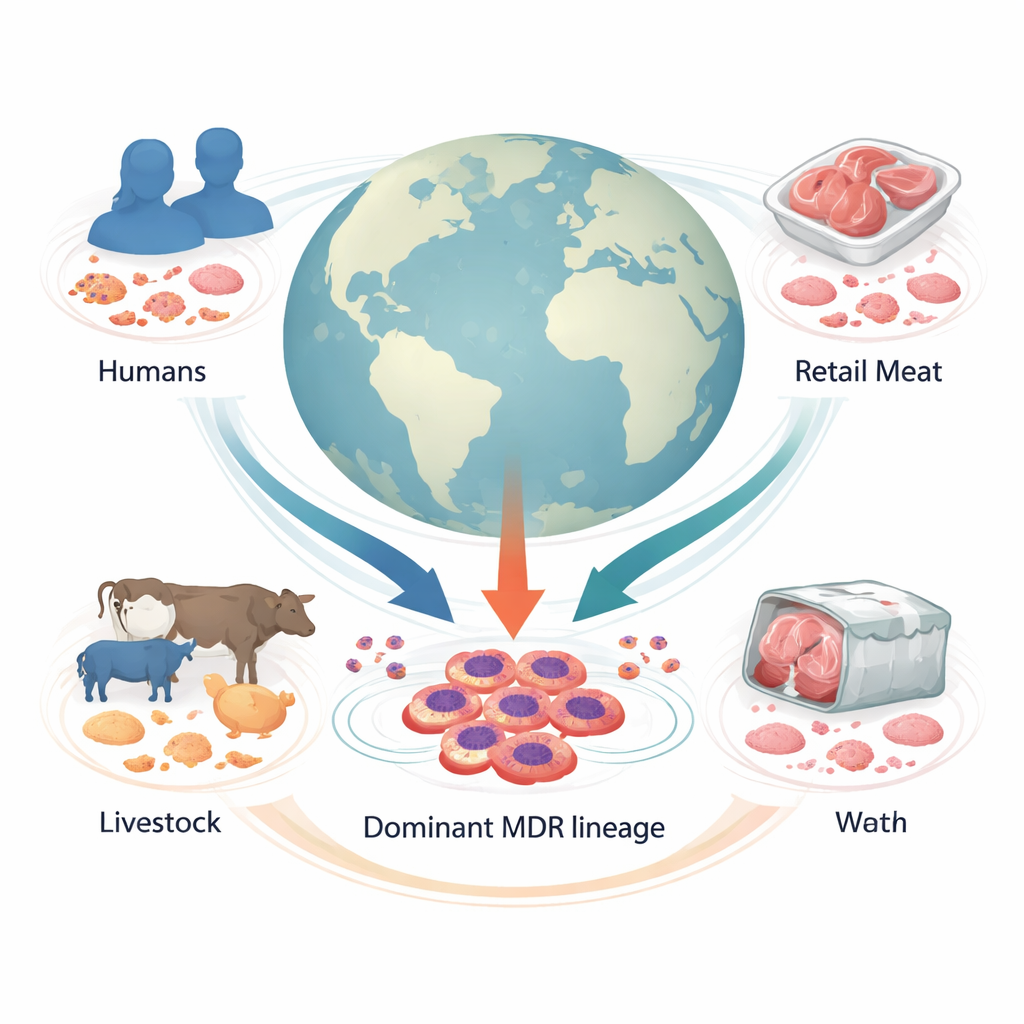
Een wereldomspannende blik op een verborgen bedreiging
De onderzoekers stelden genomen samen van 1.142 Proteus mirabilis-monsters die in 34 landen waren verzameld van mensen, vee, verhandelbaar vlees en andere omgevingen. Door volledige genomen te vergelijken, splitsten ze de bacteriën in 178 genetische families. Eén viel op: “Cluster-1,” een grote lijn die verantwoordelijk was voor één op de vijf van alle monsters en stammen uit ziekenhuizen op meerdere continenten omvatte. De meeste van deze stammen kwamen van mensen, maar een aanzienlijk deel was ook afkomstig van landbouwdieren en vlees, wat aangeeft dat deze lijn zich over soorten en via de voedselketen verplaatst.
Een lijn gewapend met vele medicijnschilden
Bij het scannen van de genomen op antibioticaresistentiegenen droeg Cluster-1 duidelijk meer ballast. Gemiddeld droegen de leden bijna 18 resistentiegenen elk, veel meer dan andere lijnen. Daartoe behoorden genen die enkele van onze krachtigste antibiotica uitschakelen, zoals carbapenems, die vaak als reddingsmiddelen worden bewaard. Veel van deze resistentiegenen bevinden zich binnen een groot DNA-“eiland” genaamd PmGRI1, dat tussen bacteriën kan springen. Sommige versies van dit eiland dragen meer dan 20 resistentiegenen tegelijkertijd, waardoor Proteus in feite een lopende apotheek van verdedigingsmiddelen wordt en artsen weinig behandelingsopties overblijven.
Kleverige eigenschappen die de bacterie helpen zich vast te houden
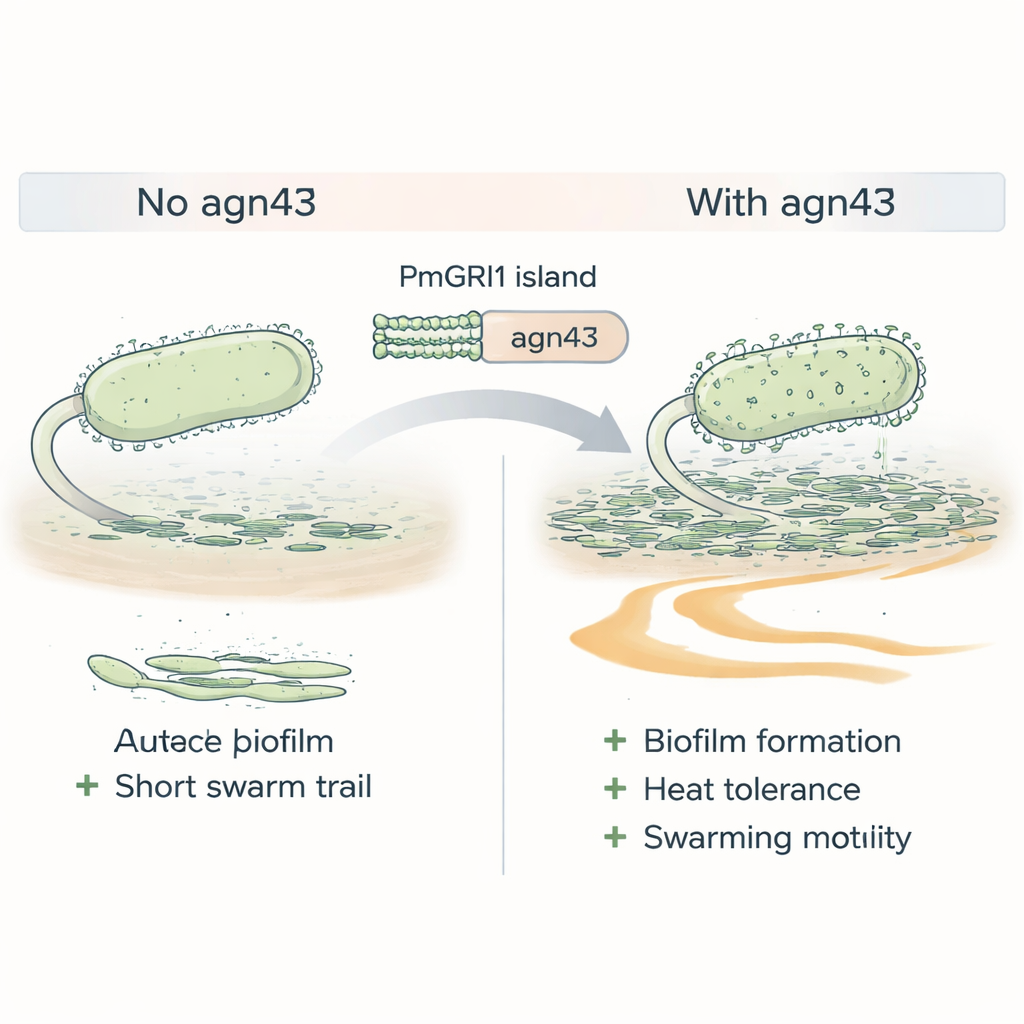
Resistentie alleen garandeert geen succes; bacteriën moeten ook goed kunnen overleven in het lichaam en de ziekenhuisomgeving. Cluster-1-stammen waren verrijkt met genen die gelinkt zijn aan het vasthechten aan cellen en het vormen van biofilms—slijmerige gemeenschappen die bacteriën beschermen tegen medicijnen en het immuunsysteem. Een opvallend gen op het PmGRI1-eiland, genaamd agn43, codeert voor een oppervlakteeiwit dat werkt als moleculair klittenband en helpt cellen samen te klonteren. Toen de wetenschappers agn43 verwijderden in een Cluster-1-stam, vormde de mutant zwakkere biofilms, verdroeg hij hittebelasting minder goed en zwermde hij minder efficiënt over oppervlakten—allemaal eigenschappen die normaal gesproken Proteus helpen om urinekatheters te koloniseren en zich door de urinewegen te verspreiden.
Hoe en waar deze superlijn zich verspreidde
Door genetische verschillen te combineren met isolatiedata reconstrueerden de onderzoekers een tijdlijn voor Cluster-1. Ze schatten dat de meest recente gemeenschappelijke voorouder rond 1910 verscheen, decennia voordat moderne antibiotica wijdverbreid werden gebruikt. De lijn splitste later in twee medisch belangrijke takken: één voornamelijk in China die een carbapenem-afbrekend gen draagt genaamd blaKPC-2, en een andere voornamelijk in de Verenigde Staten die een verwant gen draagt, blaIMP-27. Vanaf het einde van de jaren tachtig breidde Cluster-1 zich snel uit en werd herhaaldelijk gedetecteerd bij verplaatsingen tussen landen en tussen mensen, vee en vlees, wat zijn epidemische potentieel benadrukt.
Wat dit betekent voor patiënten en de volksgezondheid
Voor leken is de boodschap dat een bepaalde familie van Proteus mirabilis zich heeft ontwikkeld tot een zeer succesvolle ziekenhuisbacterie door twee voordelen te combineren: een dikke pantsering van antibioticaresistentiegenen en extra “kleverigheid” die helpt beschermende films te vormen en te blijven bestaan op katheters en weefsels. Deze combinatie maakt infecties moeilijker te behandelen en gemakkelijker te verspreiden. Het werk benadrukt de noodzaak van nauwgezette genetische monitoring van deze lijn zowel in ziekenhuizen als in de landbouw, strengere infectiepreventie rondom katheters en zorgvuldig antibioticagebruik om de opkomst en wereldwijde circulatie van zulke multiresistente stammen te vertragen.
Bronvermelding: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Trefwoorden: antibioticaresistentie, urineweginfectie, ziekenhuisinfecties, bacteriële genomica, biofilm