Clear Sky Science · nl
Synergie tussen fag en meropenem tegen OXA-48-producerende Klebsiella pneumoniae klinische isolaten
Waarom piepkleine virussen falende antibiotica kunnen redden
Ziekenhuizen over de hele wereld worstelen met infecties die niet langer reageren op onze sterkste antibiotica. Een van de ergste daders is de bacterie Klebsiella pneumoniae, die longontsteking, bloedbaaninfecties en urineweginfecties kan veroorzaken. Deze studie onderzoekt of zorgvuldig geselecteerde virussen die bacteriën aanvallen — zogenoemde fagen — kunnen samenwerken met een krachtig antibioticum, meropenem, om zeer resistente stammen uit te roeien die momenteel levens van patiënten bedreigen.
Een sluipende ziekenhuiskiemen in opkomst
Klebsiella pneumoniae is een belangrijke ziekenhuis-superbug geworden omdat veel stammen geleerd hebben resistent te raken tegen carbapenems, een familie antibiotica die als laatste redmiddel wordt bewaard. Deze bacteriën dragen vaak resistentiegenen op kleine DNA-cirkels die plasmiden worden genoemd, en die ze onderling kunnen uitwisselen als ruilkaartjes. Een van die plasmiden, bekend als pOXA-48, codeert voor een enzym dat carbapenems afbreekt, waardoor middelen als meropenem grotendeels nutteloos worden. Naarmate deze plasmiden zich verspreiden via hoog-risico bacteriële klonen door Europa en daarbuiten, worden standaardbehandelingen minder betrouwbaar en worden zelfs routinematige medische ingrepen gevaarlijker.
Fagen inzetten als precieze aanvallers
Aangezien nieuwe antibiotica traag verschijnen, wenden onderzoekers zich tot fagtherapie — het gebruik van virussen die specifiek bacteriën infecteren en doden. In deze studie richtte het team zich op een lytische faag genaamd vB_Kpn_2-P4, die een breed scala klinische Klebsiella-isolaten kon infecteren die in Spaanse ziekenhuizen waren verzameld. In laboratoriumtesten kon deze faag bacteriën aanvallen die verschillende carbapenem-resistentiemechanismen droegen. Zoals vaak gebeurt met zowel antibiotica als fagen, overleefde en groeide echter een deel van de bacteriële cellen uiteindelijk terug, wat de noodzaak onderstreept van combinatiestrategieën in plaats van vertrouwen op één enkel wapen.
Als geneesmiddel en virus beter samenwerken
Vervolgens testten de onderzoekers hoe meropenem en de faag zich gedroegen wanneer ze samen werden gebruikt. Ze lieten twaalf resistente bacteriële isolaten groeien en stelden ze bloot aan alleen meropenem, alleen faag, of aan beide tegelijk, en volgden de groei gedurende vele uren. Terwijl alle isolaten onder de testvoorwaarden meropenem konden verdragen, kwam er een opvallend patroon naar voren: bij stammen die het OXA-48-plasmide droegen, veroorzaakte de combinatie van faag plus hoge dosis meropenem een dramatische instorting van het bacteriële aantal, gevolgd door geen detecteerbare hergroei. Bij lagere meropenemniveaus lieten deze OXA-48-stammen nog steeds een sterke daling in bacteriële belasting zien. Ter vergelijking: stammen met andere resistentie-enzymen toonden dit krachtige gezamenlijke effect niet, wat suggereert dat een specifiek kenmerk van het OXA-48-plasmide de bacteriën uniek kwetsbaar maakt wanneer ze tegelijk met beide bedreigingen worden geconfronteerd.
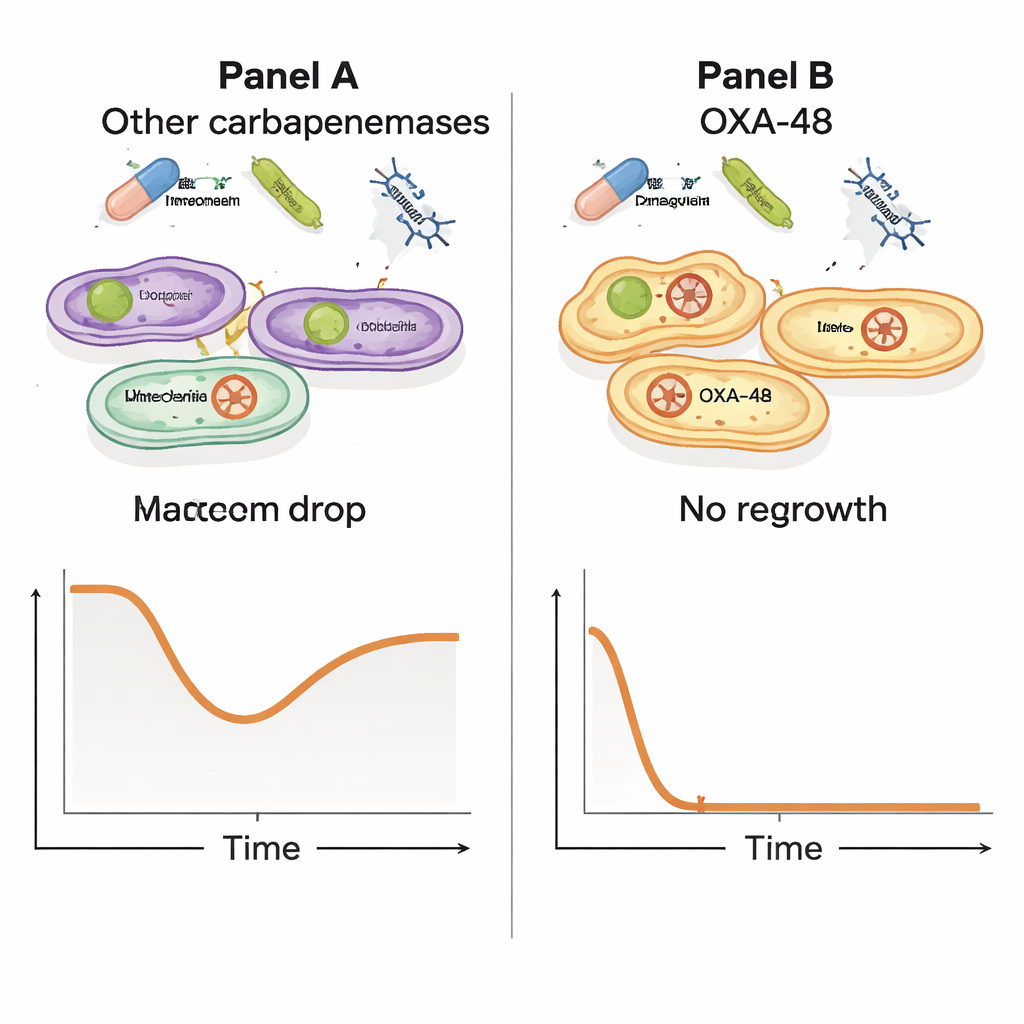
Het verborgen genetische hulpje volgen
Om te begrijpen waarom alleen de OXA-48-producers deze synergie toonden, vergeleek het team de genomen van de verschillende bacteriële isolaten. Ze identificeerden tientallen genen die met de synergistische reactie geassocieerd waren, bijna allemaal gegroepeerd op het pOXA-48-plasmide. Belangrijk is dat toen ze bacteriën isoleerden die resistentie tegen de faag hadden ontwikkeld, deze overlevenden nog steeds een intact OXA-48-gen droegen; ze hadden het plasmide niet simpelweg weggeworpen om te ontsnappen. Dit wijst op een subtieler beeld waarin het plasmide dat drugresistentie verleent ook verborgen kosten voor de biologie van de bacterie met zich meebrengt — kosten die dodelijk worden wanneer faag en antibioticum samen toeslaan en de balans tegen de verwekker doen kantelen.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat de genetische trucjes die bacteriën gebruiken om onze geneesmiddelen te ontwijken, soms tegen hen kunnen worden gebruikt. In dit geval lijkt een specifiek resistentieplasmide bepaalde Klebsiella-stammen buitengewoon gevoelig te maken voor een gecombineerde aanval door een afgestemde faag en meropenem. Hoewel dit werk in laboratoriumomstandigheden is uitgevoerd en er meer onderzoek nodig is in diermodellen en patiënten, suggereert het dat het matchen van de juiste faag met het juiste resistentieprofiel antibiotica kan doen herleven die hun kracht leken te hebben verloren. In plaats van antibiotica te vervangen, zouden fagen slimme bondgenoten kunnen worden die ons helpen superbugs te slim af te zijn die ooit onverslaanbaar leken.
Bronvermelding: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Trefwoorden: fagtherapie, antibioticaresistentie, Klebsiella pneumoniae, OXA-48-plasmide, meropenem-synergie