Clear Sky Science · nl
Wereldwijde reactie op blootstelling aan antibiotica onthult een cruciale rol voor nucleotidemetabolisme in hoge niveaus van β-lactam-tolerantie
Waarom sommige bacteriën onze beste antibiotica van zich afschudden
Antibiotica horen schadelijke bacteriën uit te schakelen, maar veel infecties blijven hardnekkig bestaan of keren terug na behandeling. Dit artikel onderzoekt één onderbelichte reden: sommige bacteriën kunnen zich ingraven en tijdelijk zelfs zeer hoge doses krachtige middelen zoals penicilline overleven. Door bloot te leggen hoe deze microben hun interne chemie anders inrichten om de aanval te doorstaan, wijzen de onderzoekers op nieuwe manieren om de effectiviteit van bestaande antibiotica te herstellen.
Een heimelijke overlevingstruc in infecties
Bij blootstelling aan beta-lactamantibiotica zoals penicilline sterven veel gevaarlijke gramnegatieve bacteriën niet simpelweg. In plaats daarvan kunnen ze hun stijve celwand verliezen en veranderen in fragiele, ronde lichamen die sferoplasten worden genoemd. In deze vorm stoppen ze met delen maar blijven ze levend en metabolisch actief. Zodra het medicijn weg is, bouwen ze hun wand opnieuw op, herstellen ze hun normale staafvorm en kunnen ze de infectie opnieuw aanwakkeren. Omdat deze “tolerantie” een opstap is naar volledige antibioticaresistentie en behandelingsfalen, is het cruciaal te begrijpen hoe sferoplasten overleven voor toekomstige geneeskunde.
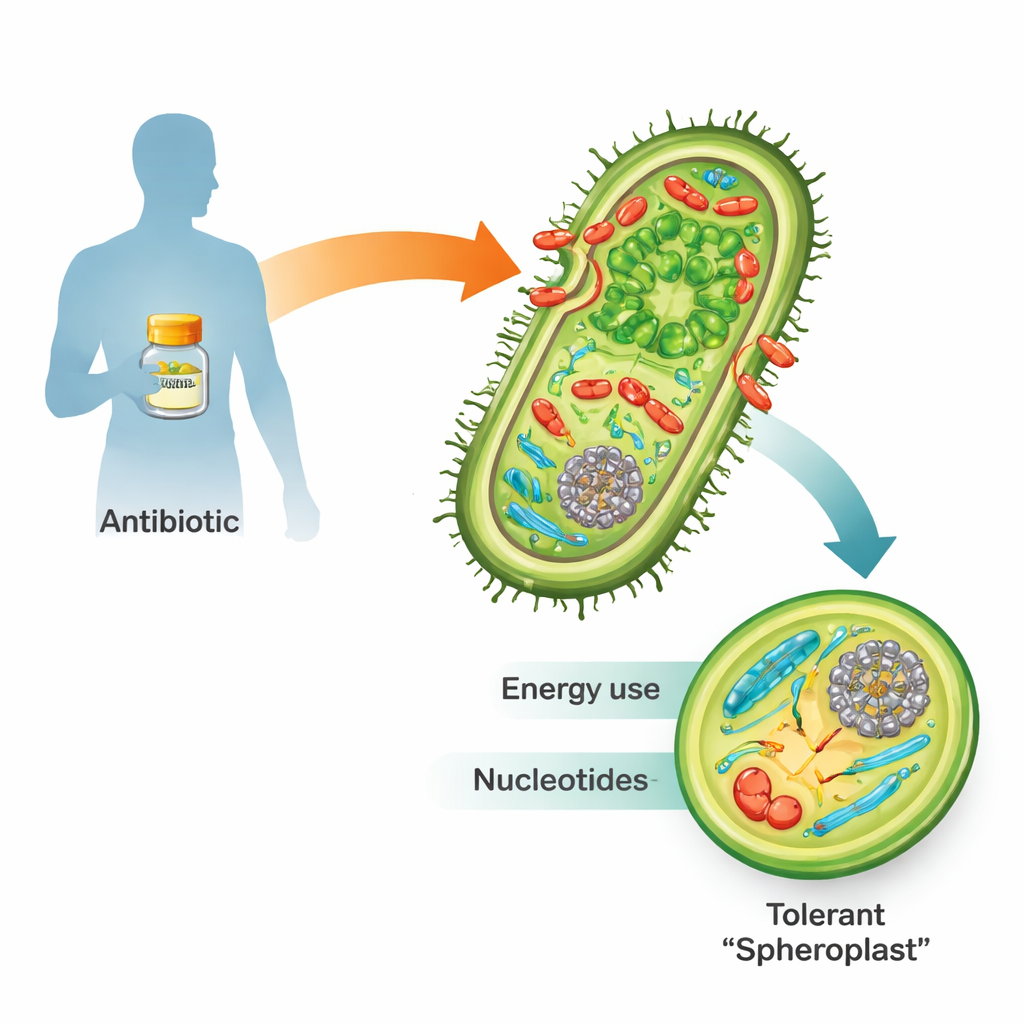
In het noodbericht van de cel luisteren
Het team gebruikte Vibrio cholerae, de bacterie die cholera veroorzaakt, als model omdat ze uitzonderlijk tolerant is voor beta-lactams en gemakkelijk genetisch te manipuleren is. Ze dompelden de bacteriën onder in tien keer de minimale dodelijke dosis penicilline en volgden de reactie in de tijd met twee krachtige instrumenten. Transcriptomics hield bij welke genen aan- of uitgingen, terwijl metabolomics honderden kleine moleculen mat die de cel aandrijven en opbouwen. Samen creëerden deze “multi-omics”-technieken een tijds-resolved kaart van hoe een tolerante cel haar interne werking herstructureert tijdens een medicijnaanval.
Metabole omleiding en een verborgen zwakke plek
De gegevens onthulden ingrijpende veranderingen in kernroutes. Genen voor de opbouw van de celwand werden sterk geactiveerd, wat past bij de poging van de cel om schade te herstellen en zich voor herstel voor te bereiden. Hitte-shock- en stressresponsystemen laaiden ook op, waarschijnlijk om verkeerd gevouwen of geoxideerde eiwitten te verwerken die door antibioticum-geïnduceerde stress ontstaan. Tegelijkertijd verschoof het centrale koolstofmetabolisme: bepaalde stappen van de TCA-cyclus (de belangrijkste energiegenerator van de cel) werden versterkt, terwijl belangrijke glycolyse-intermediairen zoals glucose-6-fosfaat en fructose-6-fosfaat dramatisch uitgeput raakten. Deze intermediairen voeden normaal zowel energieproductie als celwandopbouw, wat erop wijst dat voortdurende, verspillende “futile cycling” van wandmateriaal bronnen uitputte.
Nucleotiden onder druk
De meest opvallende verandering betrof nucleotiden, de bouwstenen van DNA, RNA en vele energiedragende moleculen. De niveaus van veel nucleotiden en hun voorlopers kelderden in penicilline-behandelde cellen, zelfs terwijl de genen voor hun de novo-synthese sterk werden geactiveerd. Tegelijkertijd werden genen die betrokken zijn bij het “recyclen” van nucleotiden naar beneden bijgesteld, alsof de cel probeerde te sparen van het weinige dat nog over was. Deze patronen suggereerden dat sferoplasten onder zware nucleotide-stress staan. Toen de onderzoekers opzettelijk routes interfereerden die nucleotide-voorlopers aanleveren — zoals de pentosefosfaatafvoer — of de nucleotideproductie blokkeerden met een ander middel, trimethoprim, doodde de combinatie met beta-lactams veel meer bacteriën dan elk middel afzonderlijk. Deze sterke synergie werd niet alleen gezien in Vibrio cholerae maar ook in hoogtolerante klinische stammen van Klebsiella pneumoniae en Escherichia coli.
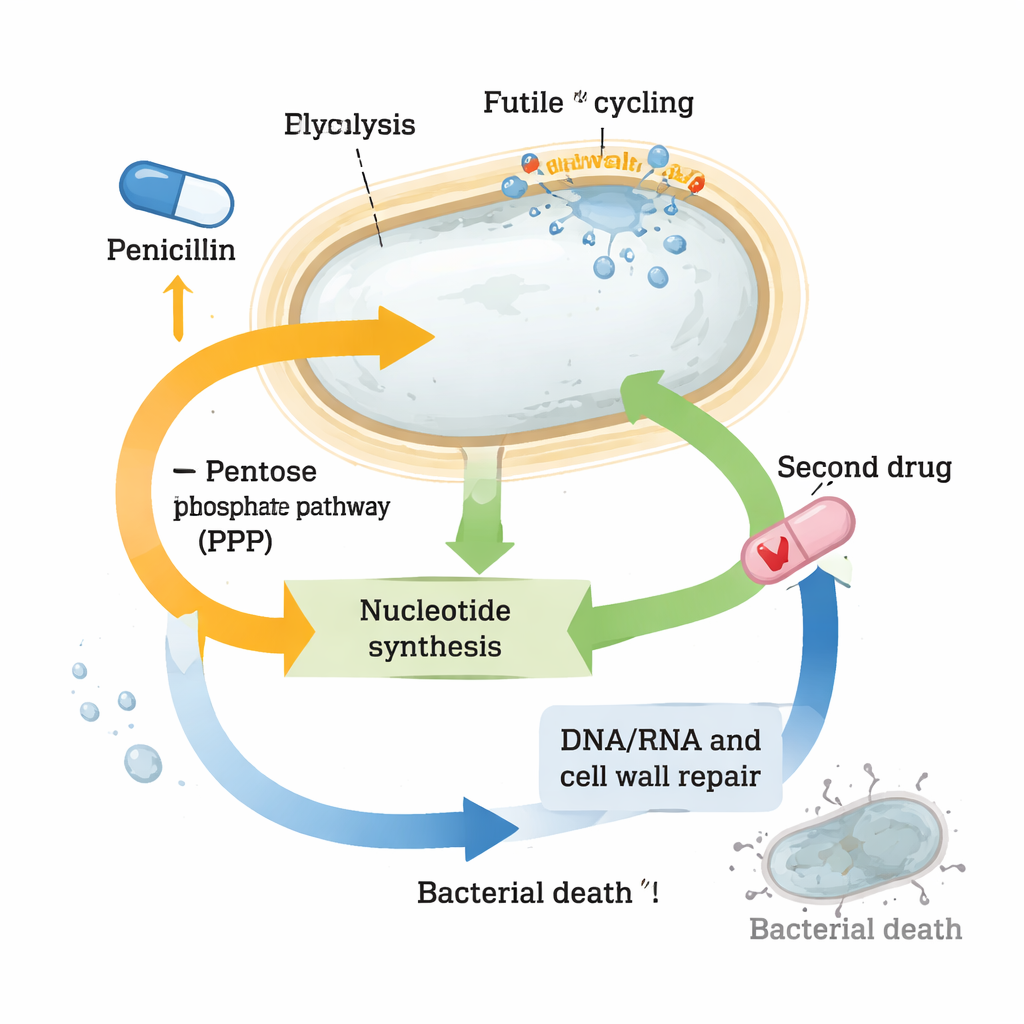
Survivalchemie omzetten in een therapeutisch voordeel
Ondanks ingrijpende herinrichting van hun metabolisme slagen tolerante sferoplasten erin hun energievaluta, ATP, relatief stabiel te houden en catastrofale schade te vermijden, wat hen helpt langdurige antibioticablootstelling te overleven. Maar het werk toont aan dat ze daarbij hun nucleotidevoorraden tot het randje brengen. Die hachelijke balans creëert een kwetsbaarheid: een kleine extra aanslag op het nucleotidemetabolisme met een tweede middel doet hun verdediging instorten en herstelt de krachtige bactericide werking. Voor niet-specialistische lezers is de kernboodschap dat sommige bacteriën antibiotica overleven niet omdat de middelen hun doel missen, maar omdat de cellen snel hun chemie herbedraden om de klap te doorstaan. Door de zwakke schakels in deze overlevingsbedrading — hier het nucleotidemetabolisme — te vinden en te benutten, kunnen onderzoekers oude antibiotica omvormen tot krachtige combinatietherapieën die zelfs zeer tolerante ziekteverwekkers te slim af zijn.
Bronvermelding: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Trefwoorden: antibiotica-tolerantie, beta-lactam antibiotica, nucleotidemetabolisme, bacteriële persistentie, drugcombinaties