Clear Sky Science · nl
Modaliteiten verbinden met AI: een overzicht van AI‑vorderingen in multimodale biomedische beeldvorming
Meer zien dan het blote oog
De moderne geneeskunde steunt sterk op beelden — van röntgenfoto’s en MRI‑scans tot microscoopslices van weefsel — om te begrijpen wat er in het lichaam gebeurt. Deze review legt uit hoe kunstmatige intelligentie (AI) verschillende soorten medische beelden kan samenweven tot één rijker beeld van ziekte. Voor een niet‑specialistische lezer is de aantrekkingskracht duidelijk: deze ontwikkelingen kunnen eerder kanker opsporen, zorgen voor nauwkeurigere diagnoses en behandelingen afstemmen op het individu in plaats van op de gemiddelde patiënt.
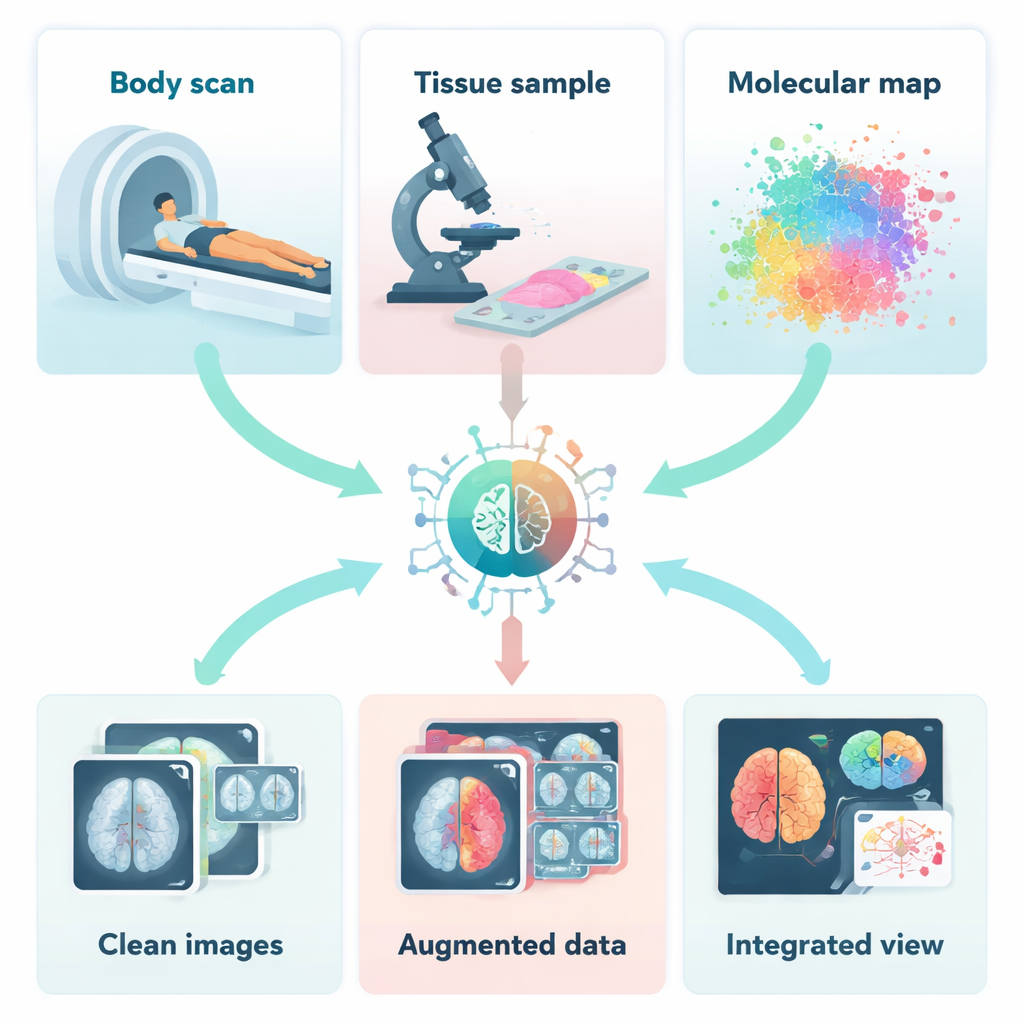
Waarom één beeld niet langer genoeg is
Elke beeldvormingstechniek toont slechts een deel van het verhaal. Radiologische middelen zoals CT, MRI en echografie onthullen de vorm en structuur van organen, terwijl nucleaire scans zoals PET laten zien hoe actief een tumor is. Onder de microscoop zien pathologen hoe cellen zijn gerangschikt, en spectroscopische methoden lezen de chemische vingerafdrukken van weefsels uit. Optische technieken zoals optische coherentie‑tomografie kunnen inzoomen op fijne lagen in het oog of de huid. Op zichzelf kunnen deze “eenzijdige” momentopnamen belangrijke aanwijzingen missen. Gecombineerd kunnen ze echter koppelingen leggen tussen hoe een tumor eruitziet, hoe hij zich gedraagt en welke moleculen hem aansturen, waardoor artsen een completer beeld van de ziekte krijgen.
Hoe AI medische beelden schoonmaakt en aanvult
Voordat verschillende beelden gecombineerd kunnen worden, moeten ze worden opgeschoond, uitgelijnd en soms zelfs helemaal gegenereerd. De auteurs beschrijven hoe AI helpt ruis en bewegingsonscherpte uit scans te verwijderen, details te herstellen in low‑dose CT‑ of PET‑beelden en artefacten te corrigeren die anders artsen en computers zouden misleiden. Deep learning‑systemen kunnen uit voorbeelden leren hoe een schoon beeld eruit hoort te zien en nieuwe scans dienovereenkomstig herstellen. Andere AI‑modellen genereren realistische synthetische beelden om kleine datasets aan te vullen of ontbrekende scantypen in te vullen. Dit is bijzonder waardevol bij zeldzame ziekten, waar vaak maar weinig echte voorbeelden beschikbaar zijn om diagnostische hulpmiddelen op te trainen.
Verschillende gezichtspunten samenvoegen tot één verhaal
De kern van de review is hoe AI meerdere beeldbronnen daadwerkelijk fuseert. Op het meest basale niveau leggen pixelgebaseerde methoden scans zoals MRI en PET over elkaar zodat structuur en activiteit in één scherper beeld zichtbaar zijn. Geavanceerdere benaderingen extraheren sleutelpatronen of “features” uit elke modaliteit en combineren die patronen in plaats van de ruwe beelden, waardoor het proces robuuster wordt tegen verschillen in resolutie en uitlijning. Laat‑fase of “decision‑level” fusie gaat verder: afzonderlijke AI‑modellen analyseren verschillende beelden en stemmen vervolgens of middelen hun voorspellingen. Hiërarchische systemen combineren meerdere van deze ideeën en stapelen verschillende fusiefasen, zodat ze binnen één raamwerk alles kunnen verwerken, van kleine cellulaire details tot orgaanbrede veranderingen.
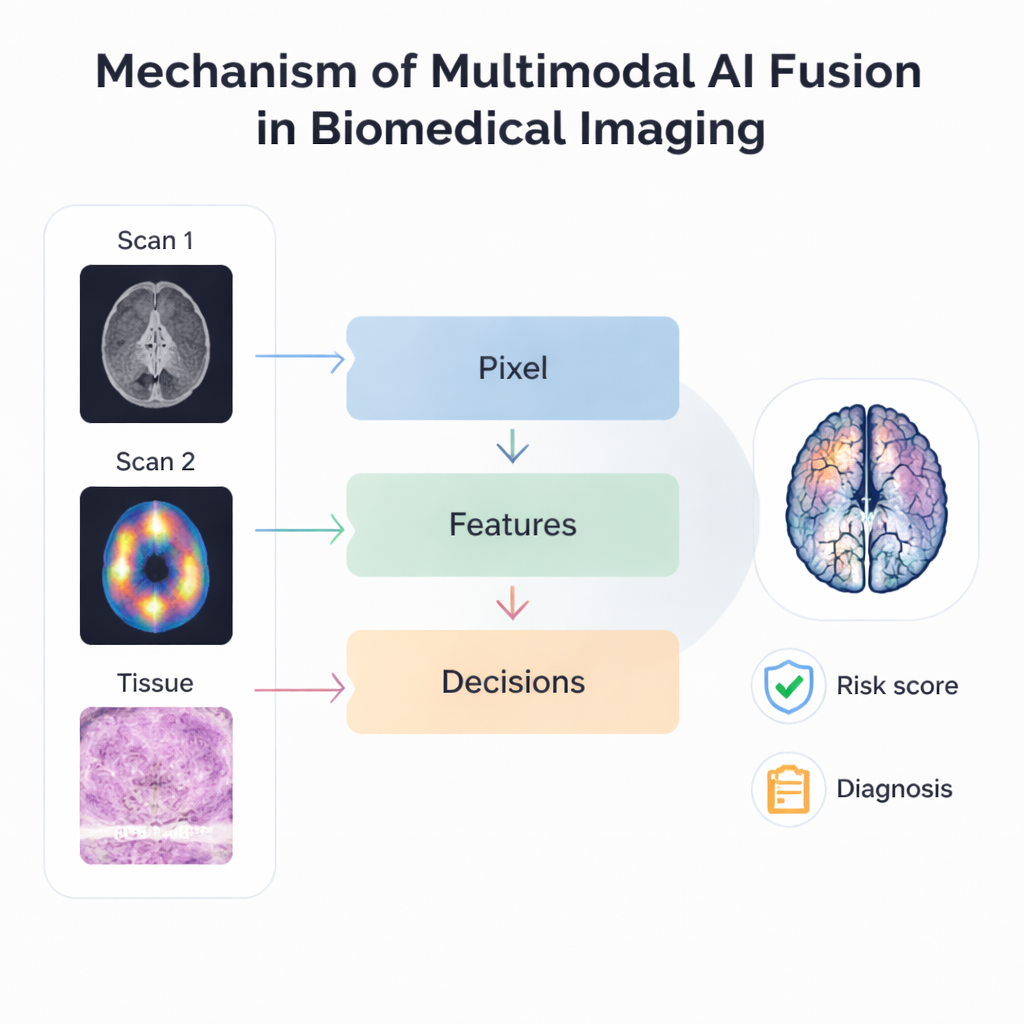
Van betere beelden naar betere zorg
Deze fusietechnieken worden al in veel klinische scenario’s uitgeprobeerd. Het combineren van meerdere MRI‑sequenties verbetert de segmentatie van hersentumoren, terwijl het samenvoegen van mammografie, echografie en MRI borsttumordetectie en risicovoorspelling versterkt. Het koppelen van digitale pathologiedias aan radiologiebeelden helpt de genetica van tumoren en het overlevingsperspectief van patiënten te voorspellen zonder extra tests. AI ondersteunt ook “data‑gedreven beeldvorming”, waarbij subtiele patronen in scans worden gecorreleerd met genactiviteit of patiëntuitkomsten, wat belooft nauwkeurigere prognoses en betere therapiekeuze. Nieuwe foundation‑modellen en multimodale grote taalmodellen streven ernaar te generaliseren over taken en beeldtypes en zelfs beelden met geschreven klinische notities te verbinden, op weg naar universele tools die zich kunnen aanpassen aan veel ziekten en ziekenhuizen.
Vertrouwen, rechtvaardigheid en de weg vooruit
Ondanks de opwinding benadrukken de auteurs dat belangrijke uitdagingen blijven bestaan. Medische beelden variëren sterk tussen ziekenhuizen, machines en patiëntengroepen, wat AI kwetsbaar of bevooroordeeld kan maken als dat niet zorgvuldig wordt aangepakt. Veel krachtige modellen gedragen zich als zwarte dozen, waardoor het voor clinici moeilijk is te zien waarom een bepaalde beslissing is genomen. De review bespreekt inspanningen om te laten zien welke gebieden van elk beeld de voorspellingen het meest beïnvloeden en om eerlijke, transparantere systemen te ontwerpen. Ook worden ethische kwesties rond privacy, gegevensdeling en de forse rekencapaciteit van grote modellen genoemd. Vooruitkijkend voorzien de auteurs gespecialiseerde AI‑"agenten" die continu beeldvorming, draagbare sensoren en medische dossiers monitoren, clinici realtime assisteren en helpen bij het coördineren van langdurige zorg. Voor patiënten komt het erop neer dat het combineren van veel soorten medische beelden met AI kan betekenen: snellere antwoorden, meer gepersonaliseerde behandelingen en uiteindelijk betere uitkomsten — mits deze technologieën verantwoordelijk worden ontwikkeld en ingezet.
Bronvermelding: Doan, L.M.T., Shahhosseini, K., Verma, S. et al. Bridging modalities with AI: a review of AI advances in multimodal biomedical imaging. Commun Eng 5, 30 (2026). https://doi.org/10.1038/s44172-026-00602-x
Trefwoorden: multimodale biomedische beeldvorming, medische AI, beeldfusie, radiologie en pathologie, precisiemedicijn