Clear Sky Science · nl
Multi-contrast magnetische deeltjesbeeldvorming voor tomografische pH-monitoring met stimuli-responsieve hydrogel
Waarom het meten van zuurgraad diep in het lichaam belangrijk is
Artsen weten dat subtiele veranderingen in zuurgraad—uitgedrukt als pH—vaak problemen signaleren voordat andere symptomen zichtbaar zijn. Ontstoken weefsels, geïnfecteerde implantaten en groeiende tumoren kunnen allemaal hun lokale pH verschuiven, maar het is tegenwoordig moeilijk om dat veilig en nauwkeurig diep in het lichaam te meten. Dit artikel presenteert een proof-of-concept beeldvormingstechniek die klinici op termijn zou kunnen toestaan pH zonder naalden of straling diep in het lichaam te “zien”, met behulp van kleine magnetische deeltjes ingebed in slimme gels.
Een nieuwe manier om magnetische deeltjes te zien
Magnetic particle imaging (MPI) is een opkomende medische beeldvormingstechniek die niet direct naar anatomie kijkt. In plaats daarvan detecteert het alleen speciaal ontworpen magnetische nanodeeltjes die in het lichaam zijn geïnjecteerd of geïmplanteerd. In tegenstelling tot MRI, waarbij weefsel het signaal creëert en contrastmiddelen dat signaal slechts aanpassen, vormen bij MPI de deeltjes zelf de volledige signaalbron. Dat maakt het mogelijk ze zeer precies te tellen en te volgen. In de afgelopen jaren hebben onderzoekers MPI ontwikkeld tot een soort “multi-contrast” instrument, waarbij veranderingen in de omgeving van de deeltjes—zoals temperatuur of viscositeit—het signaal op meetbare manieren veranderen. Het huidige werk voegt een andere cruciale omgevingsfactor aan die lijst toe: pH.
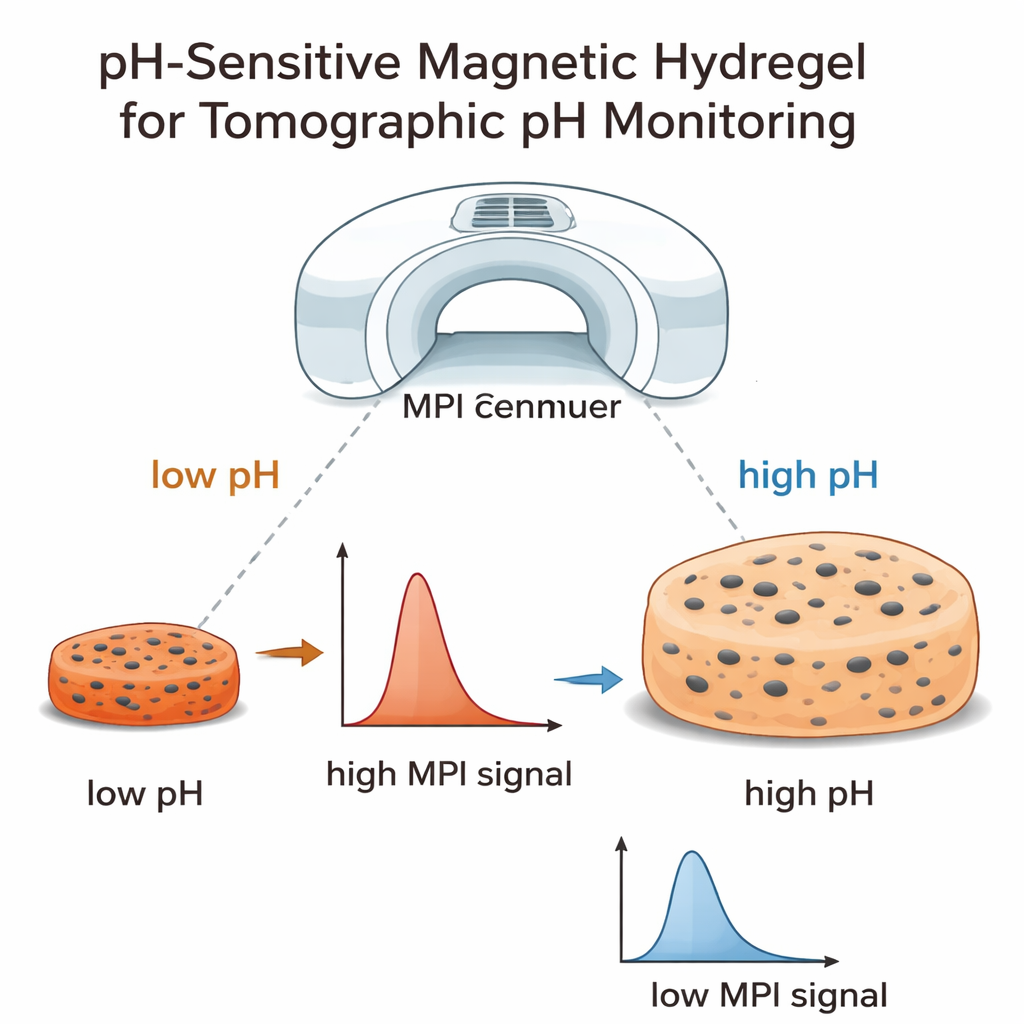
Slimme gels die uitzetten bij zuurgraad
Het sleutelbestanddeel in deze studie is een zacht, waterminnend materiaal dat bekendstaat als een hydrogel. Het team gebruikte een synthetische hydrogel die chemische groepen bevat die lading kunnen winnen of verliezen afhankelijk van de pH. Bij lage pH (zuurder) zijn deze groepen minder geladen en blijft de gel relatief compact. Bij hogere pH (basischer) worden ze sterk geladen en stoten ze elkaar af, waardoor de gel dramatisch opzwelt, meer water opneemt en in volume met meerdere honderden procenten toeneemt. Door deze gels te weken in een oplossing van superparamagnetische ijzeroxide-nanodeeltjes veranderden de onderzoekers ze in kleine magnetische pH-sensoren. In zure oplossingen liggen de deeltjes dicht opeengepakt in een klein volume; in basische oplossingen zet de gel uit en verspreiden de deeltjes zich.
Hoe uitzetting het magnetische signaal verandert
Om te testen hoe uitzetting beïnvloedt wat een MPI-scanner zou waarnemen, gebruikte het team eerst een aanvullende techniek genaamd magnetic particle spectrometry. Ze maten de magnetische respons van droge gels en gels die waren opgezwollen bij verschillende pH-waarden. Naarmate de pH toenam en de gels opzwollen, werd het gemeten signaal zwakker en werd het frequentiespectrum van het signaal smaller. Met andere woorden, hoe meer de gel uitzette, hoe minder sterke “harmonischen” de detector oppikte. Dit gedrag weerspiegelt waarschijnlijk veranderingen in hoe de deeltjes met elkaar en met het gelframewerk interacteren naarmate hun onderlinge afstand toeneemt. Belangrijk is dat het effect reproduceerbaar was en een duidelijke, statistisch significante trend toonde: in het medisch relevante zure bereik leidde een hogere pH tot meer uitzetting en een lager magnetisch signaal, met een redelijk lineaire relatie.
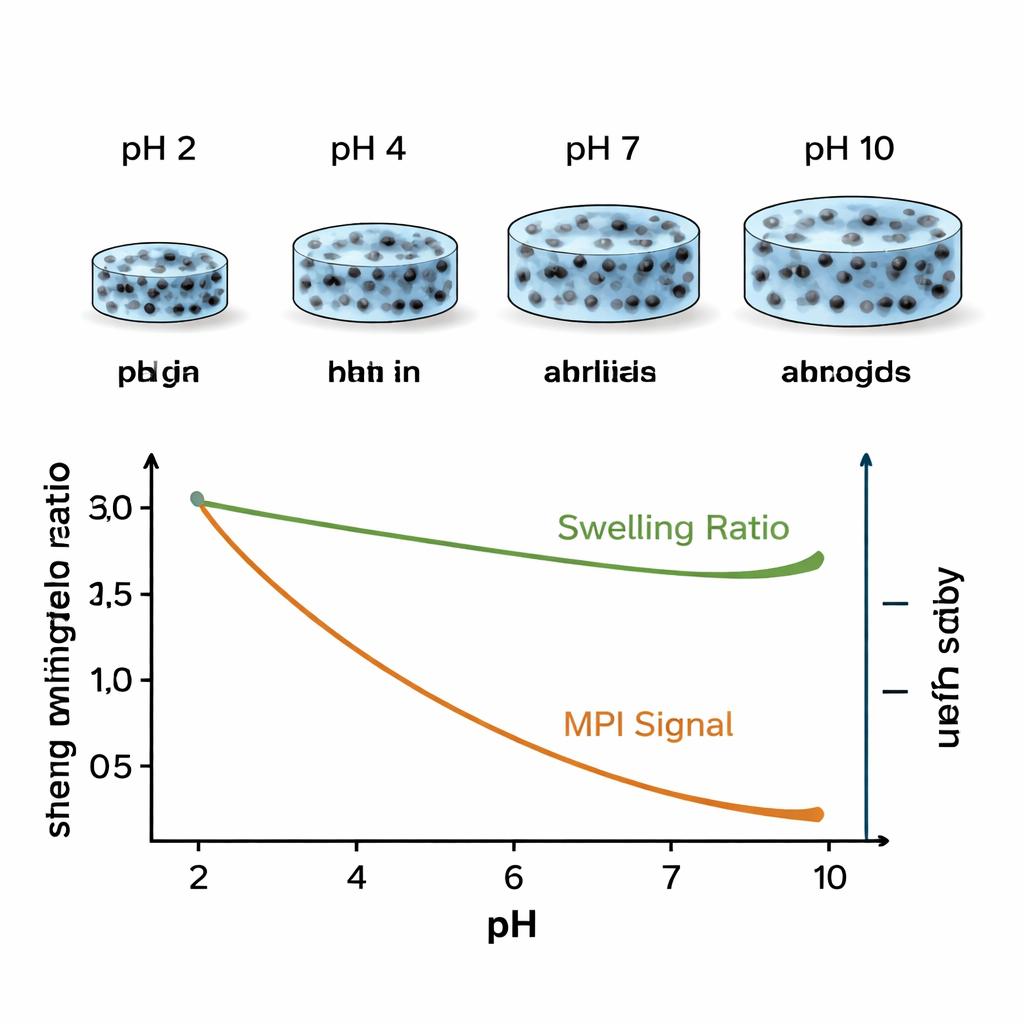
Signaalveranderingen omzetten in pH-kaarten
Vervolgens toonden de onderzoekers aan dat deze signaalverschillen kunnen worden omgezet in beelden die pH-waarden onderscheiden. Ze plaatsten meerdere gelplekken in een 3D-geprint houder en lieten ze opzwellen in oplossingen met verschillende pH-niveaus. Met een preklinische MPI-scanner verkregen ze beelden en namen ze tegelijkertijd afzonderlijke “systeemmatrices” op voor gels gehouden bij specifieke referentie-pH-waarden. Door de beelden te reconstrueren met meerdere kanalen—elk afgestemd op een referentie-pH—konden ze verschillende kleuren toewijzen aan verschillende pH-responsen. In deze multikleurbeelden lichtten gels in zuurdere oplossingen sterk op in de overeenkomende kanalen, terwijl gels in basischere oplossingen zwakker leken of bij zeer hoge pH bijna verdwenen omdat hun signaal te klein was met de huidige opstelling. Dit bevestigde dat MPI, althans voor goed gescheiden pH-waarden zoals 2, 4 en 7, pH ruimtelijk kan onderscheiden.
Waar dit naartoe kan leiden in de geneeskunde
Samengevat laat dit werk zien dat pH-responsieve magnetische hydrogels onzichtbare chemische zuurgraad kunnen omzetten in een magnetisch signaal dat MPI-scanners kunnen detecteren en scheiden. De auteurs demonstreren dat, in zure bereiken die belangrijk zijn voor ziekten, geluitzetting en verandering in het magnetische signaal de pH op een voorspelbare manier volgen en als verschillende kleuren in een beeld kunnen worden weergegeven. Hoewel dit een vroege laboratoriumstudie is met millimetergrote pleisters, legt het de basis voor toekomstige geminiaturiseerde sensoren die geïnjecteerd of geïmplanteerd kunnen worden om ontstekingen, infecties of tumorumgevingen niet-invasief te monitoren. Met verdere verfijning om de gevoeligheid rond normale lichaams-pH te verbeteren en kleine pH-verschuivingen te detecteren, zou deze benadering “chemisch zicht” aan MPI kunnen toevoegen, waardoor klinici niet alleen zien waar weefsels zich bevinden, maar ook hoe ziek ze mogelijk zijn op basis van hun lokale zuurgraad.
Bronvermelding: Kluwe, B., Ackers, J., Graeser, M. et al. Multi-contrast magnetic particle imaging for tomographic pH monitoring using stimuli-responsive hydrogels. Commun Eng 5, 33 (2026). https://doi.org/10.1038/s44172-026-00586-8
Trefwoorden: magnetic particle imaging, pH-detectie, slimme hydrogel, nanodeeltjes beeldvorming, niet-invasieve diagnostiek