Clear Sky Science · nl
Vermindering van epicardiale activatie en myofibroblast‑rijkdom via de Fbln2–Nupr1b‑as stimuleert hartregeneratie in zebravissen
Waarom sommige harten zichzelf kunnen genezen
Wanneer iemand een hartaanval heeft, wordt de beschadigde spier meestal dichtgeplakt met een stijve littekenstructuur die nooit volledig verdwijnt. Zebravissen, kleine gestreepte siervissen, doen iets opmerkelijks: zij groeien hun hartweefsel opnieuw en ruimen na verloop van tijd het grootste deel van het litteken op. Deze studie stelt een ogenschijnlijk eenvoudige vraag met grote medische implicaties: hoe weet een genezend hart wanneer het littekenweefsel moet opbouwen en wanneer het moet worden verwijderd zodat nieuwe spier kan groeien? Door dit evenwicht bij zebravissen te ontcijferen, wijst het werk op strategieën die het op een dag mogelijk zouden kunnen maken dat beschadigde menselijke harten zichzelf herstellen in plaats van falen.
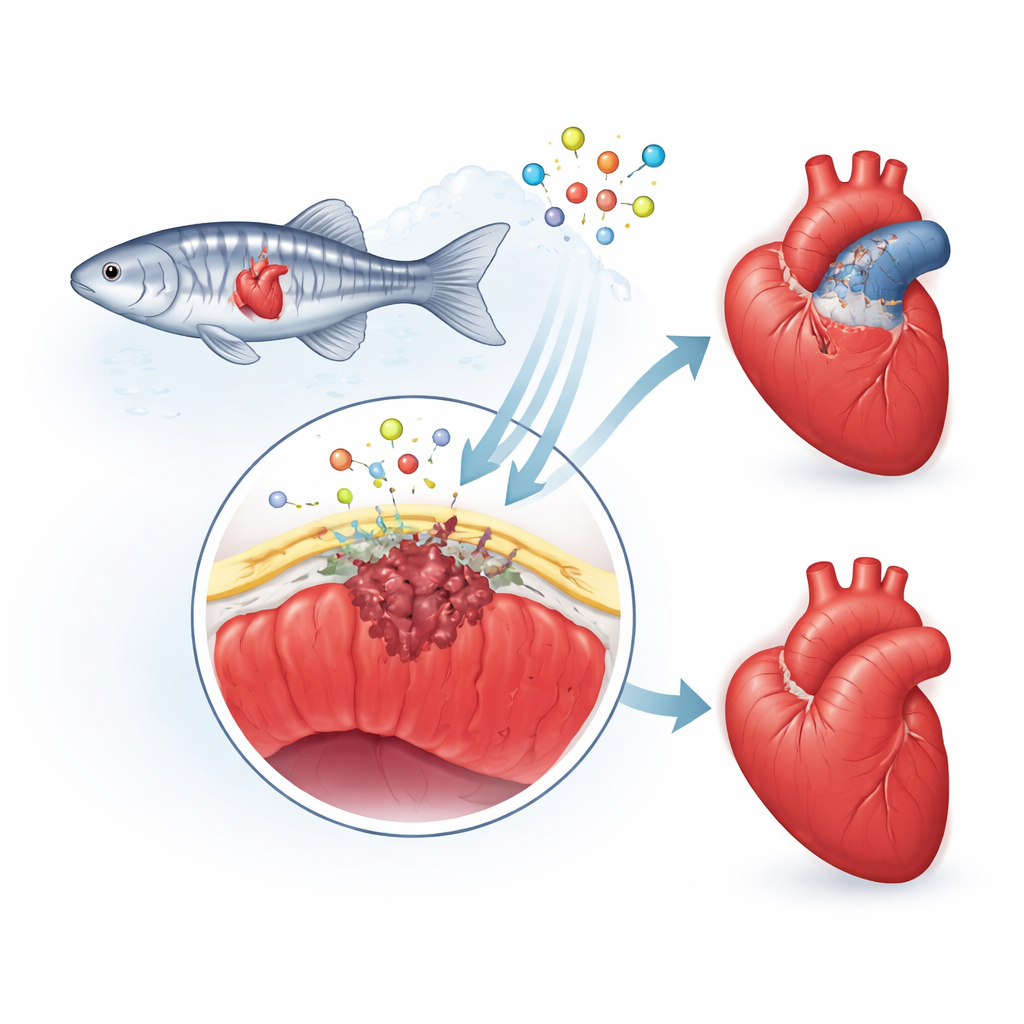
De beschermende buitenlaag van het hart
De onderzoekers richten zich op het epicardium, een dunne ‘huid’ die het hart bedekt. Na een verwonding wordt deze laag actief, veranderen de cellen van identiteit en dringen sommige de beschadigde zone binnen. Daar worden ze ondersteunende cellen en littekenvormende cellen, en ze geven chemische signalen af die de groei van nieuwe bloedvaten en hartspier aansturen. Bij mensen slaat deze reparatiereactie vaak door, waardoor een dik, blijvend litteken achterblijft. Bij zebravissen is het litteken echter tijdelijk en wordt het geleidelijk afgebroken naarmate gezond spierweefsel terugkeert. Het team vermoedde dat een eiwit genaamd fibuline‑2 (Fbln2), dat in het omliggende skelet van het hart zit, helpt het tempo en de intensiteit van deze epicardiale respons te bepalen.
Een moleculaire dimmer voor littekenvorming
Met behulp van genbewerking in zebravissen creëerden de wetenschappers twee typen dieren met verschillende Fbln2‑niveaus: één stam met verlaagde Fbln2 en een andere waarin het eiwit volledig ontbrak. Ze beschadigden de vis harten met een vriesprobe, als model voor een hartaanval, en volgden het herstel over weken tot maanden. Toen de Fbln2‑niveaus werden verlaagd, nam de vroege celdeling in hartspier en bloedvatbekleding af, maar het vezelige litteken dat zich vormde was kleiner en gemakkelijker te herbouwen. Na drie maanden waren deze harten goed geregenereerd en bevatten ze weinig collageen, het belangrijkste littekenmateriaal. Daarentegen vertoonden vissen die volledig geen Fbln2 hadden een sterkere onderdrukking van een belangrijke groei‑en‑littekenvormingsroute, de TGFβ‑signaalfamilie, en hadden ze veel minder littekenvormende cellen direct onder het epicardium. Hun vroege littekens waren ook kleiner—maar later slaagden deze harten er niet in collageen te verwijderen en eindigden ze met grote, blijvende littekens en slechte regeneratie.
Nadere blik op veranderingen in epicardiale toestand
Om te zien hoe epicardiale cellen zich gedroegen op enkel‑celniveau, gebruikte het team single‑cell RNA‑sequencing kort na de verwonding. Ze identificeerden meerdere epicardiale cel “toestanden”, waaronder rustige cellen, pas geactiveerde cellen, gestresste cellen die zich aanpassen aan lage zuurstof, en cellen die zich actief delen. Bij vissen met normaal Fbln2 vorderden epicardiale cellen soepel van rustig naar geactiveerd naar rijpere toestanden. Bij vissen met verlaagd of afwezig Fbln2 stokte deze progressie: cellen bleven hangen in vroege stadia en de meer volwassen geactiveerde groepen waren ondervertegenwoordigd, vooral bij de dieren met volledig verlies. Meerdere genen die normaal gesproken aanzetten tijdens epicardiale activatie en als reactie op TGFβ‑signalering werden omlaag geregeld, wat wijst op Fbln2 als een tuner van deze route die bepaalt hoe sterk het epicardium zich inzet voor het vormen en herbouwen van littekenweefsel.
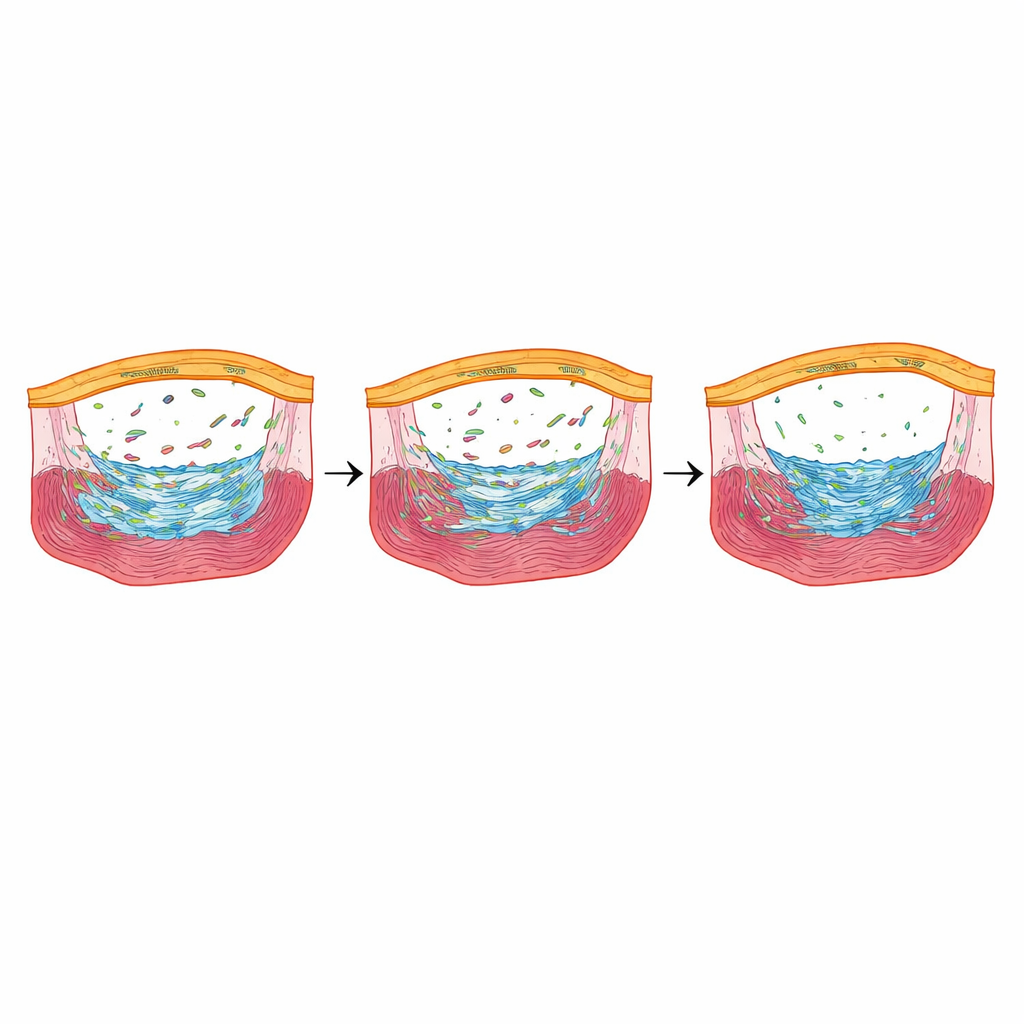
Een stressresponder die herstel fijn afstemt
Onder de genen die het scherpst werden gereduceerd toen Fbln2 werd verlaagd, stak er één uit: nupr1b, een stress‑responsieve regulator die actief is in epicardiale cellen tijdens vroege genezing. Toen de onderzoekers nupr1b verwijderden, toonden zebravissen minder epicardiale littekenvormende cellen en verminderde deling van hartspiercellen, en ze behielden grote collageenafzettingen maanden na de verwonding—vergelijkbaar met vissen die volledig Fbln2 misten. Opmerkelijk was dat, wanneer ze nupr1b kort heractiverden uitsluitend in epicardiale cellen van vissen met verlaagd Fbln2, het aantal littekenvormende cellen en de proliferatie van hartspiercellen terugkeerde, en late littekenvorming toenam. Het chemisch blokkeren van TGFβ‑receptoren verminderde nupr1b‑niveaus, waardoor nupr1b geplaatst wordt stroomafwaarts van een Fbln2–TGFβ‑signaleringas.
Wat dit betekent voor het genezen van het menselijke hart
Samen onthullen deze bevindingen een “epicardiale Fbln2–Nupr1b‑as” die zebravissen helpt balanceren tussen te weinig en te veel fibrose. Het iets dempen van deze as tempert de vroege littekenuitbarsting en bevordert efficiënte littekenverwijdering, terwijl het volledig uitschakelen de regeneratie ontspoort en een rigide litteken achterlaat. Voor de menselijke geneeskunde is de les dat het doel niet is om littekenvorming volledig te blokkeren, maar om deze af te stemmen—zorgen voor voldoende structuur om ruptuur te voorkomen, terwijl littekenweefsel tijdelijk blijft en kan worden vervangen door gezond spierweefsel. Het begrijpen en uiteindelijk benutten van dit zebravis‑controlesysteem zou toekomstige therapieën kunnen informeren die het beschadigde menselijke hart aanzetten tot echte regeneratie in plaats van chronische littekenvorming.
Bronvermelding: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Trefwoorden: cardiale regeneratie, fibrose, zebravis, epicardium, TGF‑beta signalering