Clear Sky Science · nl
Integratieve genomische en literatuurbeoordeling van desmogleïne‑2-gerelateerde aritmogene cardiomyopathie met validatie in een Italiaanse cohort
Waarom dit hartgen belangrijk is voor families
Veel plotselinge hartproblemen bij jonge en verder gezonde mensen zijn niet willekeurig—ze zijn (ten minste deels) in hun DNA vastgelegd. Dit artikel onderzoekt een belangrijk hart-“lijm”-eiwit genaamd desmogleïne‑2 en laat zien hoe kleine veranderingen in het bijbehorende gen de hartspier kunnen verzwakken, het elektrische ritme kunnen ontregelen en het risico op gevaarlijke gebeurtenissen kunnen verhogen. Door grote genetische databases te combineren met een zorgvuldig gevolgde Italiaanse patiëntengroep geven de onderzoekers duidelijkere antwoorden voor families die willen weten wat een testuitslag voor dit gen echt betekent.
De mechanische lijm van het hart
Hartspiercellen moeten stevig aan elkaar vastklampen terwijl ze miljoenen keren slaan in een leven. Desmogleïne‑2 maakt deel uit van een microscopische, klinknagelachtige structuur die aangrenzende cellen vergrendelt zodat ze als een team kunnen trekken. De auteurs leggen uit hoe dit eiwit zich uitstrekt van de buitenkant van de cel, waar het een bijpassende partner op de volgende cel vastgrijpt, tot de binnenkant, waar het zich haakt aan een ondersteunend geraamte. Omdat desmogleïne‑2 het enige lid van zijn familie is dat in hartcellen voorkomt, kan ernstige schade daaraan niet door een vervanger worden gecompenseerd, wat het hart extra kwetsbaar maakt.
Betekenisvolle genetische veranderingen scheiden van achtergrondruis
Moderne sequencing detecteert duizenden verschillen in het desmogleïne‑2-gen binnen de populatie, maar de meeste veroorzaken geen ziekte. Het team beoordeelde systematisch 115 gepubliceerde studies en maakte gebruik van twee grote openbare databases die samen meer dan 5.000 varianten vermeldden. Met algemeen aanvaarde regels uit de medische genetica herclassificeerden zij elke wijziging op basis van de waarschijnlijkheid dat deze schadelijk is. Ze ontdekten dat echt schadelijke varianten clusteren in specifieke regio’s van het eiwit—met name de buitenste segmenten die calcium nodig hebben om een stijve brug tussen cellen te vormen, een korte sequentie die geknipt moet worden voor rijping van het eiwit, en het binnenste deel dat zich vastklampt aan een ander belangrijk harteiwit. Veel andere veranderingen bleven “onzeker”, maar een subset toonde sterke aanwijzingen van relevantie en werd gemarkeerd voor nadere opvolging.
Wat de Italiaanse patiëntengroep onthult
Om te zien hoe deze genetische patronen zich in echte mensen uiten, bestudeerden de onderzoekers 95 personen in Italië die varianten in desmogleïne‑2 droegen en grondig werden beoordeeld met beeldvorming, ritmetests en langdurige follow‑up. Ongeveer de helft voldeed aan strikte criteria voor aritmogene cardiomyopathie, een aandoening waarbij delen van de hartspier geleidelijk worden vervangen door litteken- en vetweefsel, wat het risico op gevaarlijke ritmestoornissen verhoogt. Onder familieleden die een variant droegen, toonde slechts ongeveer vier op de tien daadwerkelijk tekenen van ziekte, wat onderstreept dat een positieve genentest geen garantie voor ziekte is maar wel het belang van zorgvuldige monitoring aangeeft. Degenen met duidelijke ziekte hadden een merkbare last van ernstige ritmevenementen, terwijl harttransplantaties en sterfgevallen minder frequent waren maar toch voorkwamen.
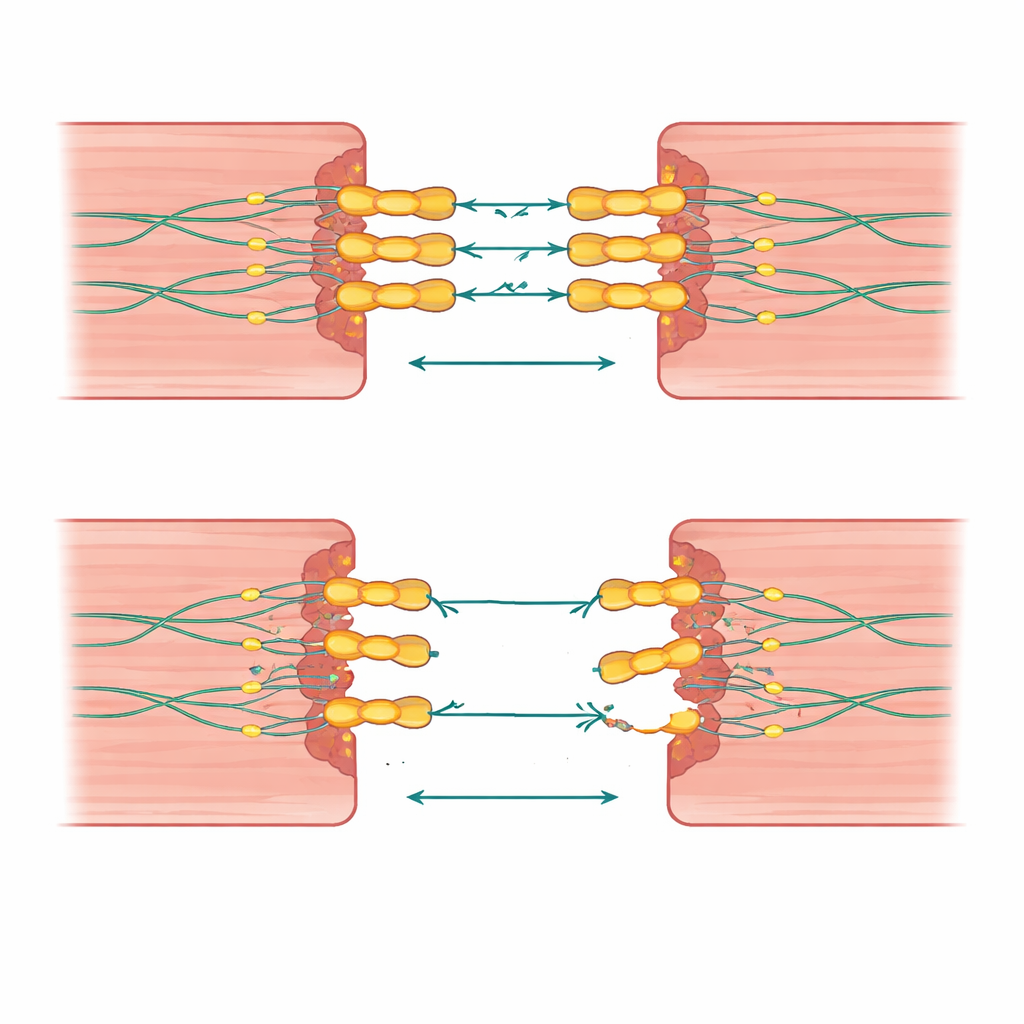
Als één klap niet genoeg is
Een opvallend inzicht uit dit werk is dat het aantal en de combinatie van genetische veranderingen ertoe doen. Mensen die twee foutieve kopieën van desmogleïne‑2 erfden, of één desmogleïne‑2‑variant plus een verandering in een verwant hart‑lijmgen, werden doorgaans op jongere leeftijd ziek en vertoonden uitgebreidere schade aan beide zijden van het hart. Sommige families droegen grote deleties of duplicaties die niet alleen desmogleïne‑2 weghaalden of verdubbelden maar ook aangrenzende genen, wat deze afwijkingen opnieuw koppelt aan agressieve ziektebeelden en clusters van plotselinge sterfgevallen. In tegenstelling daarmee hadden veel familieleden met slechts één verandering milde of geen symptomen, wat suggereert dat achtergrondgenen en levensfactoren zoals inspanning het evenwicht tussen stille risico’s en duidelijke ziekte kunnen bepalen.
Van eiwitstructuur naar patiëntrisico
Om de DNA-code aan fysieke effecten te koppelen, gebruikte het team geavanceerde 3D-eiwitmodellen om te bekijken hoe specifieke substituties de desmogleïne‑2‑scaffold kunnen verzwakken. Veranderingen die calciumbindingslussen vervormden of sleutelhechtingspunten braken, werden voorspeld het eiwit te destabiliseren en de cel‑tot‑cel‑hechting te verzwakken. Deze structurele aanwijzingen werden geïntegreerd in het classificatiesysteem, wat hielp sommige grensgevallen te verplaatsen richting meer waarschijnlijk schadelijk of meer waarschijnlijk onschadelijk. Deze brug tussen moleculair modelleren en klinische data brengt genetische testen verder dan puur codelezen naar een functioneler begrip.
Wat dit betekent voor patiënten en families
Voor families die worden getroffen door aritmogene cardiomyopathie biedt deze studie zowel voorzichtigheid als richting. Ze laat zien dat niet elke desmogleïne‑2‑variant een vonnis tot ernstige hartaandoening is, maar dat bepaalde patronen—vooral meerdere hits of veranderingen in kritische regio’s van het eiwit—gekoppeld zijn aan eerdere en ernstigere problemen. De auteurs pleiten ervoor dat dragers van deze varianten niet als “gezond tenzij het tegendeel bewezen is” afgedaan moeten worden, maar levenslang gevolgd dienen te worden met op maat gemaakte ritme‑controles en beeldvorming. Hun integratieve aanpak—die big‑data genetica, gedetailleerde familystudies en eiwitstructuur combineert—wijst de weg naar preciezere risicoinschattingen en zekerder counseling wanneer een desmogleïne‑2‑verandering op een genetische test verschijnt.
Bronvermelding: Pinci, S., Celeghin, R., Martini, M. et al. Integrative genomic and literature assessment of desmoglein 2-related arrhythmogenic cardiomyopathy with Italian cohort validation. Commun Med 6, 145 (2026). https://doi.org/10.1038/s43856-026-01416-w
Trefwoorden: aritmogene cardiomyopathie, desmogleïne‑2, erfelijke hartaandoening, genetisch risico, plotselinge hartdood