Clear Sky Science · nl
Selectieve blokkade van latente activatie van TGF-β1 onderdrukt weefselfibrose met goede veiligheid
Waarom verborgen littekens ertoe doen
Veel chronische ziekten beschadigen onze organen langzaam door stug littekenweefsel aan te leggen, een proces dat fibrose wordt genoemd. Dit littekenweefsel kan normaal functioneren in de lever, nieren, longen en zelfs rond tumoren geleidelijk verstikken; rond tumoren kan het bovendien de werking van moderne kankerimmunotherapieën verminderen. Het eiwit TGF-β1 staat centraal in dit verhardingsproces, maar het overal uitschakelen in het lichaam bleek gevaarlijk. Deze studie beschrijft een nieuw antilichaam, SOF10 genoemd, dat is ontworpen om alleen de schadelijke activatie van TGF-β1 te blokkeren terwijl essentiële rolletjes behouden blijven, en dat veelbelovende voordelen laat zien in diermodellen van leverziekte, nierfalen en kanker.
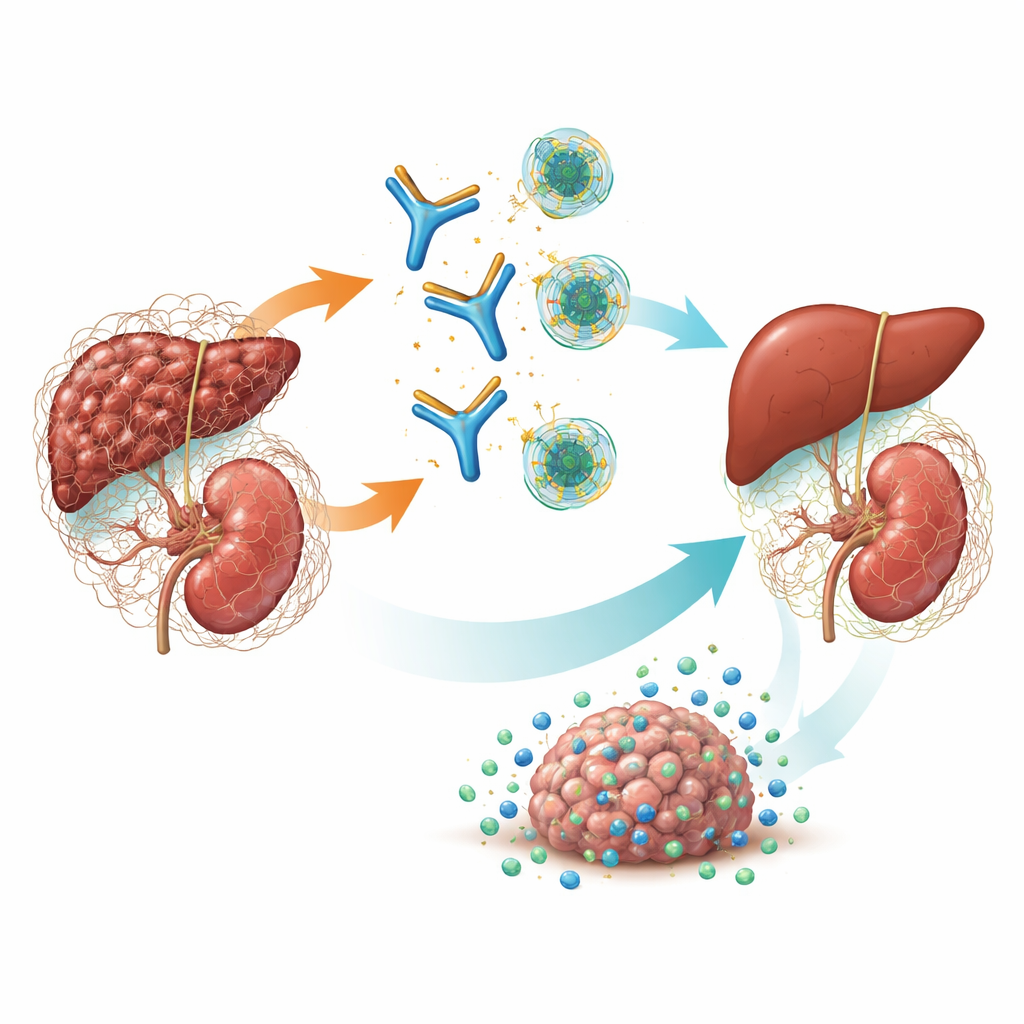
Een hoofdschakelaar voor verharding en kanker
TGF-β is een krachtig signaalmolecuul dat helpt regelen hoe cellen groeien, genezen en met het immuunsysteem omgaan. Bij chronische ziekte drijft één vorm—TGF-β1—fibroblasten ertoe overtollig bindweefsel te produceren, wat leidt tot verharding en falen van organen. Het vormt ook een immuunsuppressieve, fibrotische omhulling rond tumoren die immuuncellen en medicijnen weghoudt van kankercellen. Eerdere geneesmiddelen probeerden alle drie de TGF-β-vormen tegelijk te remmen, maar deze ‘pan-blokkade’ veroorzaakte ernstige bijwerkingen zoals schade aan hartkleppen, bloedingen en huidtumoren. Genetische studies en eerdere modellen wezen erop dat TGF-β1 de belangrijkste dader is bij fibrotische nierschade en veel solide tumoren, wat de mogelijkheid opleverde dat het zorgvuldig richten op alleen deze isoform zowel effectief als veiliger zou kunnen zijn.
TGF-β1 in zijn inactieve vorm vergrendelen
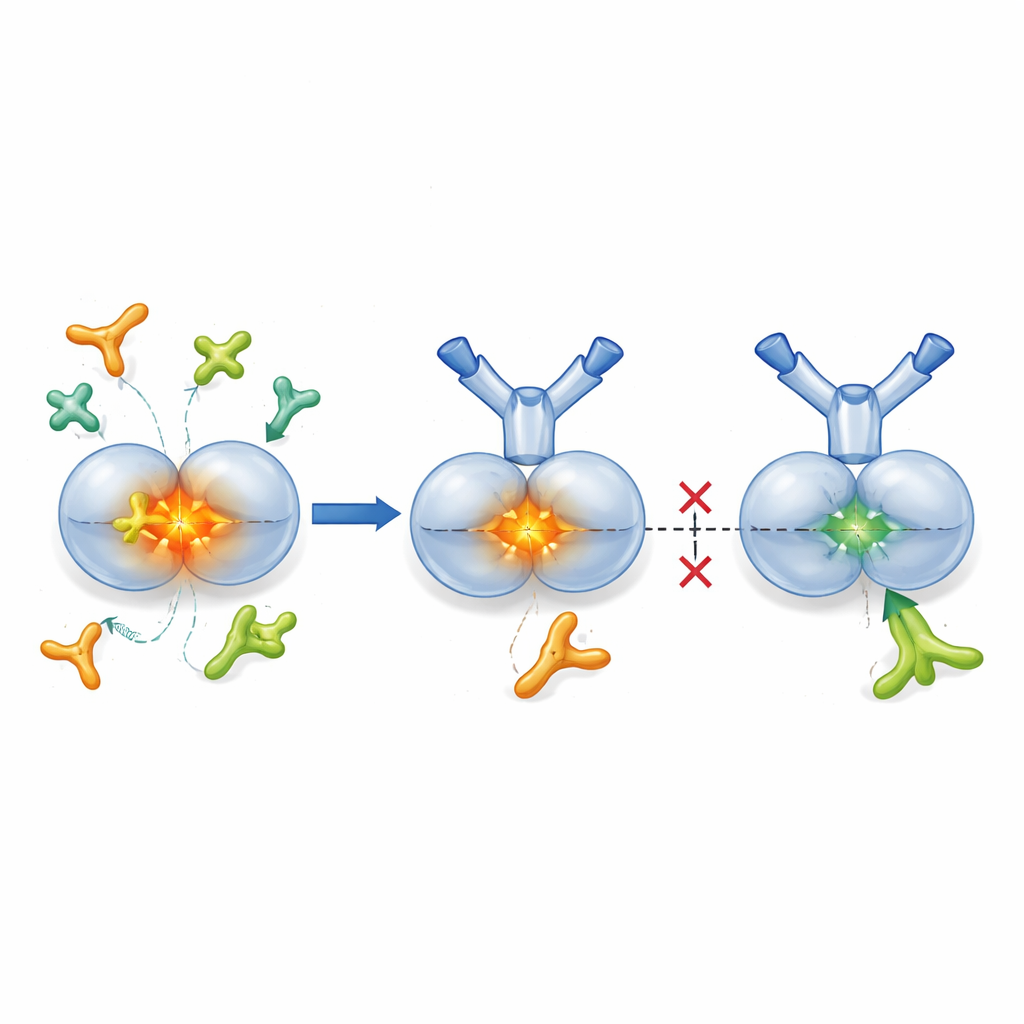
TGF-β1 wordt normaal geproduceerd in een ‘latente’ verpakking, waarbij de actieve kern is omhuld door een partner-eiwit dat het inactief houdt totdat het nodig is. Enzymen genaamd proteasen en bepaalde celoppervlakte-hechtmoleculen, integrinen, kunnen dit pakket openen en actief TGF-β1 vrijgeven in nabijgelegen weefsel. De onderzoekers ontwierpen SOF10, een gehumaniseerd antilichaam dat alleen bindt aan de latente vorm van TGF-β1, niet aan het actieve hormoon of andere isoformen. Structurele studies met röntgendiffractie toonden aan dat SOF10 zich in de interface tussen de twee helften van het latente complex klemt en het stabiliseert als een klem. In laboratoriumtests verhinderde dit dat proteasen en één integrine (αvβ8) actief TGF-β1 vrijmaakten, terwijl een andere integrine (αvβ6)—belangrijk voor het behoud van immuunbalans in gezonde weefsels—grotendeels ongemoeid bleef. In feite dempt SOF10 selectief de schadelijke activeringsroutes terwijl een cruciaal homeostatisch pad gespaard blijft.
Leveren en nieren beschermen tegen langzame schade
Om te onderzoeken of deze selectieve klem rond TGF-β1 daadwerkelijk littekenvorming kon beperken, testte het team SOF10 in verschillende muismodellen. In een snel dieet-geïnduceerd model van vetleverziekte dat uitgroeit tot leverfibrose, verlaagde SOF10-behandeling de expressie van TGF-β–responsieve genen en collageenproducerende genen in de lever, en verlaagde het hydroxyproline, een chemische marker voor opgehoopt littekenweefsel. In twee verschillende niermodellen—een chirurgisch obstructiemodel dat interstitiële fibrose aanjaagt en een genetisch model van Alport-syndroom dat zowel glomerulaire littekenvorming als nierfalen ontwikkelt—verminderde SOF10 de fibrotische genactiviteit, verlaagde het collageengehalte en verkleinden zichtbaar de gelittekende gebieden onder de microscoop. In het chronische Alport-model toonden bloedtesten verbeterde nierfunctie, en deze voordelen waren vergelijkbaar met die van een breder TGF-β–blokkerend antilichaam, maar zonder andere TGF-β-isoformen te blokkeren.
Het immuunsysteem in tumoren bevrijden
Aangezien fibrotisch weefsel rond tumoren zowel als fysieke barrière als immuinaire remming kan functioneren, vroegen de onderzoekers of SOF10 de respons op checkpointremmers kon verbeteren. In muismodellen van borstkanker en darmkanker die normaal slecht reageren op anti–PD-L1-therapie, vertraagde de toevoeging van SOF10 de tumorgroei aanzienlijk, terwijl SOF10 of anti–PD-L1 alleen weinig effect hadden. Tumoren van combinatie-behandelde dieren bevatten meer dodelijke CD8 T-cellen en meer van de toxische enzymen die zij gebruiken om kankercellen te vernietigen. Fibroblasten uit deze tumoren lieten lagere activiteit zien in collageen- en matrix-opbouwende routes maar hogere activiteit in interferon- en antigeenpresentatieroutes, een verschuiving naar een meer immuunsupportief stroma. Deze veranderingen weerspiegelden sterk wat gezien was bij brede TGF-β-blokkade, wat suggereert dat gericht remmen van latente TGF-β1 alleen het tumor-milieu op vergelijkbare wijze kan herprogrammeren.
Veiligheidssignalen bij dieren
Aangezien eerdere pogingen om TGF-β breed te blokkeren op veiligheidsproblemen stuitten, voerde het team 13-weekse toxiciteitsstudies uit in muizen en cynomolgusapen, waarbij ze herhaaldelijk hoge doses SOF10 gaven. Het middel gedroeg zich als een typisch antilichaam in de bloedbaan en over een ruime dosisrange waren er geen tekenen van schade aan belangrijke organen, bloedceltellingen of hart- en longfunctie. De hoogste geteste doses—tot 200 mg/kg elke twee weken bij muizen en 100 mg/kg bij apen—werden aangeduid als niveaus zonder waargenomen schadelijke effecten. Dit veiligheidsprofiel ondersteunt het idee dat het sparen van TGF-β2, TGF-β3 en αvβ6-gemedieerde activatie de risico’s vermindert die gezien werden bij eerdere, minder selectieve benaderingen.
Wat dit voor patiënten kan betekenen
Samengevat wijzen de bevindingen erop dat het vergrendelen van TGF-β1 in zijn inactieve omhulsel—in plaats van het volledig uitschakelen van alle TGF-β-signalen—littekenvorming in meerdere organen kan verminderen, de nierfunctie kan verbeteren en hardnekkige tumoren kwetsbaarder kan maken voor immunotherapie, allemaal met bemoedigende veiligheid in dierproeven. Hoewel humane onderzoeken nodig zijn om deze voordelen te bevestigen en langetermijneffecten te volgen, kunnen SOF10 en vergelijkbare strategieën een nieuwe manier openen om chronische fibrotische ziekten en bepaalde kankers te behandelen, door schadelijke verharding te dempen terwijl de herstel- en immuun-balancerende rollen die onze weefsels nodig hebben behouden blijven.
Bronvermelding: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Trefwoorden: fibrose, TGF-beta1, monoklonaal antilichaam, nier- en leverziekten, kankerimmunotherapie