Clear Sky Science · nl
Genomische karakterisering en subclustering van Escherichia coli klonaal complex 38 tonen gastheer-geassocieerde genetische markers
Waarom dit belangrijk is voor het dagelijks leven
Antibioticaresistente infecties zijn geen ver-van-mijn-bed ziekenhuisprobleem meer—ze raken steeds vaker voedsel, dieren, reizen en het gemeenschapsleven. Deze studie richt zich op een specifieke groep Escherichia coli-bacteriën, aangeduid als klonaal complex 38 (CC38), die ernstige bloedbaan- en urineweginfecties kunnen veroorzaken en vaak bestand zijn tegen onze belangrijkste antibiotica. Door te traceren waar deze bacteriën vandaan komen en hoe ze zich verplaatsen tussen mensen, dieren en de omgeving, laten de onderzoekers aanwijzingen zien die gezondheidsautoriteiten kunnen helpen gevaarlijke stammen te stoppen voordat ze zich wijd verspreiden.
Een nadere blik op een lastig bacterieel geslacht
Niet alle E. coli zijn schadelijk, maar sommige lijnen zijn herhaalde veroorzakers van ernstige aandoeningen. CC38 is recentelijk naar voren gekomen als één van deze problematische groepen, als tweede na een bekende risicolijn (ST131) bij Deense bloedbaaninfecties. Het team onderzocht 242 resistente E. coli CC38 van Deense patiënten, 83 afkomstig van voedsel en boerderijdieren, en meer dan 2.300 verwante genomen verzameld wereldwijd. Ze gebruikten whole-genome sequencing—het in wezen lezen van het DNA van elke bacterie—om in kaart te brengen hoe de verschillende takken van deze familie verwant zijn, welke resistentiegenen ze dragen en in welke gastheren ze de neiging hebben te leven.
Het spoor volgen van ziekenhuizen naar boerderijen en voedsel
Toen de onderzoekers E. coli CC38 uit Denense patiënten vergeleken met die uit pluimvee, vee en voedsel, vonden ze twee hoofdgroepen in Denemarken. De ene groep bestond voornamelijk uit humane infecties, terwijl de andere bacteriën uit pluimvee, andere boerderijdieren en voedingsproducten bevatte. Belangrijk is dat er geen bijna-identieke DNA-overeenkomsten waren tussen humane en dierlijke isolaten, wat suggereert dat er tijdens de studieperiode geen duidelijke voedselgerelateerde uitbraken in Denemarken plaatsvonden. Statistische modellen die naar aanvullende DNA-segmenten kijken, gaven echter aan dat sommige humane geassocieerde subgroepen waarschijnlijk pluimvee-origin hebben, wat wijst op eerdere of indirecte overspilling van kippen naar mensen.
Een wereldwijde stamboom met twee grote takken
Bij uitbreiding naar een wereldwijde dataset van 2.638 genomen bouwde het team een globale “stamboom” voor CC38. Twee grote takken staken eruit. De ene was sterk verbonden met pluimvee en droeg matige niveaus van medicijnresistentie samen met veel eigenschappen die gelinkt zijn aan ernstige ziekte. De andere werd gedomineerd door humane-geassocieerde subgroepen die verschilden in resistentie, ziektepotentieel en voorkeursgasten. Sommige subgroepen waren duidelijk mensgericht en sterk resistent, terwijl andere gemengde patronen lieten zien en opdoken in mensen, pluimvee, wilde dieren, water en gezelschapsdieren. Dit mozaïek weerspiegelt het vermogen van CC38 om zich aan te passen aan verschillende omgevingen en gastheersoorten, wat de beheersing bemoeilijkt.
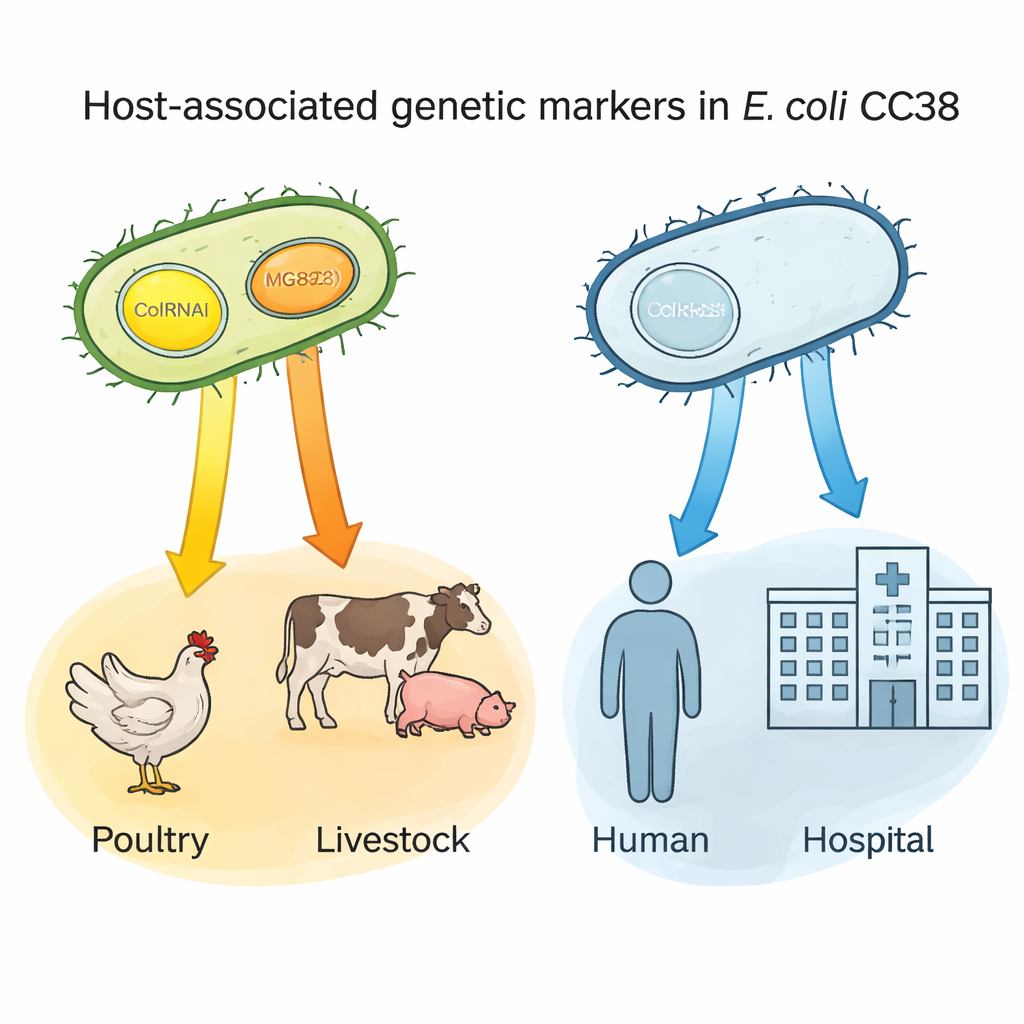
Kleine DNA-cirkels als gastheer “naamplaatjes”
Een belangrijke ontdekking betrof twee kleine DNA-fragmenten—plasmiden genaamd ColRNAI en Col(MG828)—die tussen bacteriën kunnen bewegen. Deze plasmiden kwamen vaak voor in CC38 van pluimvee en andere boerderijdieren, maar waren zeldzaam in de voornamelijk menselijke subgroepen. Met behulp van statistische analyse toonden de auteurs aan dat het dragen van één van deze plasmiden sterk voorspelde dat een isolate uit pluimvee afkomstig was; het samen voorkomen van beide was bijzonder kenmerkend voor lijnen die verbonden zijn met vee en bepaalde voedselbronnen. Omdat deze plasmiden ook vaak resistentie-eigenschappen dragen, kunnen ze fungeren als genetische “naamplaatjes” die bacteriën markeren die waarschijnlijk uit dierlijke reservoirs komen, en kunnen ze helpen te traceren hoe resistente stammen de voedselketen binnendringen en mensen bereiken.
Wat dit betekent voor het beschermen van de gezondheid
Voor niet-specialisten is de belangrijkste boodschap dat schadelijke, medicijnresistente E. coli zich niet beperken tot ziekenhuizen of patiënten: ze vormen onderling verbonden populaties die zich uitstrekken over mensen, pluimvee, vee, wilde dieren, voedsel en de omgeving. Deze studie laat zien dat binnen één belangrijke lijn, CC38, sommige takken sterk aan dieren gekoppeld zijn en andere aan mensen, en dat specifieke mobiele DNA-elementen kunnen helpen onthullen waar een stam waarschijnlijk vandaan komt. Het gebruik van deze genetische markers in routinematige surveillance kan vroegtijdig waarschuwen wanneer dier-geassocieerde resistente bacteriën in mensen beginnen te verschijnen. Dit ondersteunt op zijn beurt een “One Health”-benadering—waarbij menselijke, dierlijke en omgevingsgezondheid als onderdelen van hetzelfde systeem worden gezien—om slimmer, gerichter beleid te ontwerpen om infecties te voorkomen en de verspreiding van antibioticaresistentie te vertragen.
Bronvermelding: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Trefwoorden: antimicrobiële resistentie, Escherichia coli, zoönotische overdracht, pluimvee en vee, genomische surveillance